Перинатальные инфекции у беременных. Виды перинатальных инфекций. Клинический протокол из акушерской помощи "Перинатальные инфекции"
– группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии , неонатологии, педиатрии.

Причины внутриутробных инфекций
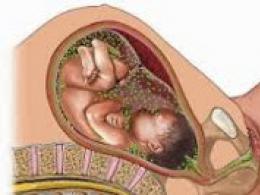
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза , кордоцентеза , биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи , герпеса , цитомегалии , гепатита В и , Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки , синегнойная палочки , протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности , может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты , эндоцервициты , ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы , преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
На тяжесть клинических проявлений внутриутробной инфекции влияют сроки инфицирования и вид возбудителя. Так, если инфицирование происходит в первые 8-10 недель эмбриогенеза, беременность обычно заканчивается самопроизвольным выкидышем. Внутриутробные инфекции, возникшие в раннем фетальном периоде (до 12 недели гестации), могут приводить к мертворождению или формированию грубых пороков развития. Внутриутробное инфицирование плода во II и III триместре беременности проявляется поражением отдельных органов (миокардитом , гепатитом , менингитом , менингоэнцефалитом) либо генерализованной инфекцией.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа , листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
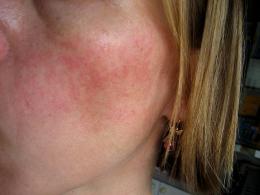
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии , с пренатальной гипотрофией , увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией , гидроцефалией . С первых дней жизни у них отмечается желтуха , элементы пиодермии , розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром , респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией , омфалитом , миокардитом или кардитом, анемией , кератоконъюнктивитом , хориоретинитом , геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта , глаукома , врожденные пороки сердца , кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов , остеомиелита .
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит , косоглазие , атрофия зрительных нервов . Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения , эпилепсия , слепота .
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности . Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности , эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом , гепатомегалией , желтухой, пневмонией, тромбоцитопенией , геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных .
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия , глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови). обнаруживает признаки.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
прививки против краснухи , должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственногоЗаражение плода во время развития в организме беременной может привести к различным инфекционным заболеваниям, объединённым общим названием - внутриутробная инфекция.. Ребёнок может заразиться раз
личными возбудителями инфекционных заболеваний во время родов (при прохождении по инфицированным родовым путям) или после рождения (через материнское молоко и другие биологические жидкости). Инфекционные заболевания, развившиеся вследствие этих причин, получили название неонатальных инфекций (интра- и постнатальные). У многих новорождённых, заразившихся во время или после родов, инфекция может протекать бессимптомно. Однако у некоторых из них, особенно у недоношенных, развиваются выраженные клинические проявления заболевания с тяжёлым течением. Перинатальные инфекции - инфекционные заболевания, возникшие вследствие инфицирования плода во время внутриутробного развития, во время рождения или после рождения.
В последние годы отмечают значительное увеличение частоты врождённых инфекций, причём преимущественно вирусной этиологии. Вирусные инфекции вызывают до 80% врождённых пороков развития у детей, среди них ведущее место занимают поражения ЦНС, а также врождённые пороки сердца и почек. Многочисленные научные данные свидетельствуют об этиологической связи врождённых пороков развития у детей с вирусными инфекциями, перенесёнными во время беременности, или с трансплацентарной передачей вирусов от беременной с персистентной формой инфекции.
К наиболее распространённым перинатальным инфекциям относят герпетическую, ЦМВ-, парвовирусную и токсоплазменную инфекции, краснуху, хламидиоз. Своевременная диагностика и лечение этих инфекций у женщин - актуальная проблема современной клинической практики.
Вирусологическое обследование новорождённых и беременных позволяет диагностировать вирусную инфекцию у подавляющего большинства обследованных (до 98%).
Ранняя и своевременная диагностика вирусной инфекции у беременных и врождённой инфекции у детей позволяет выработать оптимальную терапевтическую тактику ведения, рационально применять препараты с противовирусной направленностью с целью снижения вероятности возникновения у детей пороков развития.
При подозрении на внутриутробную инфекцию чаще всего проводят обследование беременных на наличие маркёров герпетической, ЦМВ-, пар-вовирусной, хламидийной и токсоплазменной инфекций, а также краснухи. Отрицательные результаты исследований в большинстве случаев позволяет исключить возможность инфицирования плода. Если есть подозрение на интра- и постнатальную инфекцию, необходимо проводить параллельное исследование крови матери и ребёнка. При этом возможны различные ситуации, вызывающие у врачей затруднения при интерпретации результатов. Наиболее часто встречающиеся из них приведены в табл..
При использовании в оценке данных, приведённых в табл., необходимо учитывать, что выявление у новорождённого только АТ IgG малоинформативно из-за транспланцентарного проникновения материнских АТ в его организм при внутриутробном развитии. Поэтому для исключения инфицированности необходимо определять АТ IgG в динамике у ребёнка в 1, 3, 6 и 11-12 месяцев, а при появлении клинических признаков заболевания использовать методы прямого обнаружения возбудителя (ПЦР, обнаружение Аг методом РИФ или ИФА).
В части случаев при обследовании новорождённых на наличие внутриутробных инфекций возможен ложноотрицательный результат серологического
исследования вследствие влияния высокой концентрации материнских АТ класса IgG, «маскирующих» наличие АТ IgM у ребёнка, или иммунологической толерантности (неспособность организма к иммунному ответу и синтезу АТ). В связи с этим при наличии клинических проявлений заболевания необходимо использовать методы прямого обнаружения возбудителя.
Таблица Интерпретация результатов лабораторного обследования матери и ребёнка
Наличие АТ у матери и ребёнка к одному и тому же возбудителю (возбудителям)
Обнаружение АТ у матери и их отсутствие у новорождённого при наличии у него клинической картины заболевания, а также при обследовании ребёнка, родившегося от инфицированной матери
Обнаружение высоких титров АТ IgG у ребёнка вскоре после рождения
Обнаружение у ребёнка АТ и/или возбудителей (Аг) при отсутствии АТ у матери
Титр специфических АТ IgG в сыворотке крови ребёнка превышает титр аналогичных АТ у матери (при отсутствии АТ IgM и IgA) Наличие АТ IgM и/или IgA (для хламидиоза) у ребёнка Появление АТ IgM и/или IgA (для хламидиоза) наряду с АТ IgG или только IgG у ранее серонегативного ребёнка (сероконверсия)
Наличие АТ IgM указывает на врождённую инфекцию. Если повышен титр АТ IgG, необходимо провести исследование АТ в динамике через 1-2 мес. При необходимости следует использовать методы прямого обнаружения возбудителя (ПЦР, обнаружение Аг методом РИФ или ИФА)
Использовать методы прямого обнаружения возбудителя (ПЦР, обнаружение Аг методом РИФ или ИФА) у ребёнка или исследовать титр АТ в динамике в течение первого года жизни, так как инфицирование исключить нельзя (может быть иммунологическая толерантность, когда не происходит синтеза АТ)
Повышенное содержание АТ IgG свидетельствует скорее о пассивном иммунитете, полученном от матери, чем о врождённой инфекции. Для уточнения ситуации необходимо исследовать титр АТ IgM или следить за динамикой АТ IgG (если ребёнок не инфицирован, их титр к возрасту 4-6 мес резко снижается) Внутриутробное инфицирование или инфицирование во время родов; возможно заражение ребёнка через молоко матери или при переливании крови и её компонентов; в отдельных случаях не исключено инфицирование медперсоналом. Ситуация возможна у женщин, лечившихся по поводу инфекции, в случае наступления беременности на фоне лечения или в первые месяцы после лечения Результаты исследования не могут свидетельствовать об инфицировании ребёнка. Необходимо исследовать титр АТ в динамике и использовать методы прямого обнаружения возбудителя (ПЦР, обнаружение Аг методом РИФ или ИФА) Свидетельствует об инфицировании ребёнка (АТ IgM через плаценту не проникают) Свидетельствует о первичной инфекции
Пособие для врачей и интернов
Ярославская Государственная Медицинская Академия
Кафедра акушерства и гинекологии
Факультет повышения квалификации и профессиональной подготовки специалистов здравоохранения
А в т о р ы:
д.м.н. M.Б.Охапкин, к.м.н. М.В.Хитров, И.Н.Ильяшенко
(кафедра акушерства и гинекологии Ярославской Государственной медицинской академии — зав. каф. проф. М. Б. Охапкин.)
Р е ц е н з е н т:
доцент В.П.Киселев, заведующий кафедрой детских инфекционных болезней педиатрического факультета ЯГМА.
Методическое пособие утверждено Методической комиссией по последипломному образованию Ярославской Государственной медицинской академии.
ВИРУСЫ.
I. Краснуха
Краснуха (рубелла, немецкая корь) относится к воздушно-капельным инфекциям и передается через носо-глоточный секрет. Хотя это заболевание характерно для детского возраста, но более половины всех заболевших в последние годы приходится на возраст более 9 лет, а в возрасте 20-29 лет заболевают 19-31% пациентов, в возрасте 30 лет или старше- 9-31%. К репродуктивному возрасту 75-85% женщин (половина — в субклинической форме) уже болели краснухой и имеют пожизненный иммунитет к этому заболеванию .
Вакцинация против краснухи была введена с 1969 г. и её частота значительно снизилась: до 1:100 000 населения (по данным США). Проблемой является заболеваемость К. беременных в ранних сроках. Риск уродств у плода при заболевании матери в I триместре беременности составляет около 20% (до 50% на 1 месяце и 10% на 3-ем месяце беременности). Возможными уродствами являются: катаракта, открытый артериальный проток, глухота, через несколько лет возможно заболевание сахарным диабетом.
Вирус выделяется из крови и глотки через 7-10 дней после заражения и его выделение продолжается около 1 недели. Заболевание сопровождается сыпью, которая начинается с лица на 16-18 день после заражения, артралгиями, лимфоаденопатией, повышением температуры тела. Но для диагноза заболевания наличия клинической картины недостаточно. Для подтверждения инфекции используются различные серологические тесты.
Реакция торможения гемагглютинации (антитела Ig G). От 5 до 15% переболевших К. имеют антитела в высоких титрах: 1:256. В то же время доказательством иммунитета к К, является титр 1:8-1:16. Подъем титра антител к К при повторном тесте в 4 раза и более свидетельствует об острой инфекции. В последние годы торможение гемагглютинации заменено рядом других тестов ввиду их большей точности и дешевизны: латекс агглютинация, флюоресцирующие антитела, пассивная гемагглютинация, гемолиз в геле, энзимные иммунные тесты.
Исследование специфичного для К Ig M подтверждает «свежую» инфекцию (может исчезать из крови менее, чем через 4-5 недель).
Введение иммуноглобулина G не предупреждает ни виремию, ни последующее заболевание, но лишь смягчает его симптомы, поэтому и не рекомендуется после контакта с заболевшим К., как рутинная процедура. Только для женщин, отказавшихся прервать беременность, введение Ig G может быть мерой профилактики инфекции у плода.
Таблица 1. Риск инфицирования плода.
| СРОК БЕРЕМЕННОСТИ (НЕД) | ИНФИЦИРОВАНИЕ ПЛОДА (%) |
| <11 | 90 |
| 11-12 | 30 |
| 13-14 | 20 |
| 15-16 | 10 |
| > 16 | 5 |
Резервуаром инфекции являются дети дошкольного и младшего школьного возраста . Вакцинация живой вакциной приводит к появлению иммунной защиты в 95% случаев. Недавно вакцинированные лица могут выделять вирус К., но их контакт с «чувствительными» к вирусу беременными не представляет для них опасности. Женщин, чувствительных к вирусу (без антител), рекомендуется вакцинировать, при этом желательно отложить беременность на 90 дней. Если все же вакцина введена при беременности, в первые её 3 месяца, вирус в тканях плода обнаруживается только в 3% случаев и не вызывает уродств (1,7%). Вакцинация возможна в ранний послеродовый период и не является препятствием для грудного всармливания. Не рекомендуют вакцинацию при повышении температуры тела и при иммуносупрессии.
II. Цитомегалия.
Возбудитель — ДНК содержащий вирус, относящийся к группе вирусов герпеса. В настоящее время считается наиболее частой причиной внутриутробной инфекции. По современным данным, 0,5-2,5% всех новорожденных имеют вирус при рождении и еще 3-5% всех новорожденных получают его в перинатальный период. Тератогенный потенциал не установлен. Уродства , такие как катаракта или пороки сердца, встречаются редко . Характерные для заболевания крупные клетки с ядрами, содержащими включения, т.н. симптом «совиных глаз» (патогномоничный, но редко встречающийся у инфицированных лиц), известны с начала 20 века, но сам вирус выделен лишь в 1956 г. После выделения культуры вируса установлено, что большинство случаев инфицирования протекает без клинических проявлений.
Эпидемиология . Чувствительными к инфицированию ЦМВ к своему репродуктивному возрасту остаются около 40% женщин: 45% женщин с высоким социально-экономическим статусом и 15% с низким. Наибольшая сероконверсия отмечается в возрасте 15-35 лет. Ежегодно 2% женщин с высоким СЭС и 6% с низким, инфицируются ЦМВ.
Факторами риска ЦМВ инфекции являются : низкий СЭС, повторные беременности, старший возраст, первая беременность до 15 лет и число половых партнеров. Отсутствие факторов риска повышает вероятность инфицирования ЦМВ при беременности: 1,6-2,2% беременных «чувствительных» к ЦМВ инфицируются во время беременности. Контагиозность ЦМВ невысока, поэтому для заражения нужен тесный контакт с носителем вируса: половой, бытовой (дети). Дети, посещающие дошкольные учреждения инфицируются в 25-80% и выделяют вирус около 2 лет после заражения. Если один из членов семьи инфицируется ЦМВ, он заражает половину членов семьи.
В 90% случаев инфекция у взрослых протекает субклинически, но в 10% появляется симптоматика, сходная с мононуклеозом: лейко-, лимфоцитоз, нарушения функции печени, гектическая лихорадка, недомогание, не встречаются гепатоспленомегалияи желтуха. Серьезные осложнения инфекции у взрослых редки и наблюдаются лишь при состоянии иммунодефицита или при медикаментозной иммуносупрессии, более вероятны они для плода, особенно с низкой массой при рождении (менее 1200,0). У заболевших вирус постоянно выделяется во внешнюю среду и может длительно представлять опасность для заражения: при внутриутробном заражении-4 года, при заражении в родах-2 года, у взрослых выделяется периодически (реинфекция, реактивация, состояния иммуносупрессии). Беременные с бессимптомно протекающей инфекцией выделяют вирус: шейка матки- 3-18%, мочевыводящие пути- 3-9%, грудное молоко- до 27%, глотка- 1-2%, в целом- 2-28%. Частота выделения вируса нарастает с течением беременности: в 1 триместре- 2,6%, в 3 триместре- 7,6%. При этом содержание в крови антител к ЦМВ остается постоянным.
Внутриутробное инфицирование ЦМВ обычно происходит трансплацентарно , хотя возможна и восходящая инфекция из шейки матки. Около 1% (0,5-2,5) всех новорожденных при рождении выделяют ЦМВ (чаще из мочи). Еще 3-5% всех новорожденных получают ЦМВ во время родов и позже (шеечный секрет, трансплацентарная трансфузия, материнское молоко). При наличии у матери ЦМВ инфекции в половых путях на момент родов 30-50% новорожденных будут инфицированы. При наличии ЦМВ в молоке матери 2/3 новорожденных будут инфицированы в течение 3 месяцев.
При наличии у матери антител к ЦМВ врожденное инфицирование отмечается у 1,4-1,9% новорожденных. При инфицировании матери ЦМВ впервые в период беременности внутриутробно инфицируются до 46-50% плодов, чаще встречаются осложнения для новорожденного (7-8% против 25-35%): нейро — сенсорные нарушения- 5-13%, клиническая симптоматика инфекции- 0-11-18%, задержка умственного развития- 0-13%, двусторонняя потеря слуха- 0-8% .
Несмотря на высокую частоту ЦМВ у матери, у плода и новорожденного уровень инфицированности ниже в 3-4 раза. Наиболее тяжелые последствия врожденной ЦМВ инфекции наблюдаются при заражении плода в 1 и 2 триместрах беременности. При его заражении в 3 триместре, новорожденный не имеет симптомов инфекции, но в его сыворотке крови обнаруживается Ig M. Отсутствие симптомов инфекции при рождении ещё не означает дальнейшего благополучия, постоянный и прогрессирующий характер инфекции может привести к патологии ЦНС и неврологическим осложнениям, представляющим главные последствия инфекции.
При наличии симптомов ЦМВ (примерно 10% инфицированных) у новорожденного смертность достигает 20-30%, а 90% выживших новорожденных имеют поздние осложнения заболевания: судороги, спастическая диплегия, атрофия зрительного нерва, слепота, глухота, отставание в умственном развитии. Но и у инфицированных новорожденных без симптомов заболевания (90%) также возможны поздние осложнения: отставание в умственном развитии (микроцефалия или гидроцефалия)-2%, глухота- 7%, хореоретинит- 1%, но значительно реже-10%. У половины новорожденных с симптоматикой заболевания она является типичной, хотя и напоминает проявления других известных инфекций: гепатоспленомегалия, желтуха, тромбоцитопеническая пурпура, микроцефалия, глухота, хореоретинит, атрофия зрительного нерва, кальцинаты ткани мозга (перивентрикулярные или в субэпендимальной зоне), задержка роста.
Диагноз инфицированным ЦМВ беременным , как правило, не ставится ввиду отсутствия клиники заболевания. Для подтверждения диагноза используются серологические методы: непрямая гемагглютинация, непрямая иммунофлуоресценция, иммуносорбция (ELISA), демонстрирующие наличие сероконверсии. Так как, по меньшей мере около 40% взрослых имеют антитела к ЦМВ, единичный результат не указывает на актуальность инфекции: давняя или «свежая», острая. Наличие специфического Ig M указывает на заражение в ближайшие 4-8 месяцев. Изоляция вируса в культуре (может потребовать от 2 до 6 недель) не различает первичную и возвратную инфекцию, но выделение вируса из мочи или шейки матки подтверждает бессимптомное вирусоносительство, т. к. при возвратной инфекции уровень антител в организме больного не меняется. У новорожденных клинические проявления ЦМВ инфекции ввиду их неспецифичности не являются достаточными для диагноза заболевания, для постановки которого требуются лабораторные исследования. Серологические тесты рассматриваются как вспомогательные, а наиболее точным считается изоляция вируса в культуре клеток. Материал для исследования может быть получен из мочи, носоглотки, конъюнктивы, спиномозговой жидкости.
Пренатальный диагноз возможен с использованием УЗИ, амниоцентеза, кордоцентеза. При УЗИ наиболее часто можно обнаружить микро- и гидроцефалию, кистозные изменения или очаги кальцификации (некроз) в перивентрикулярной зоне мозга, ткани печени, плаценты, задержку роста плода, маловодие, асцит у плода, перикардиальный или плевральный выпот, гипоэхогенный кишечник, водянку плода. В крови плода, полученной кордоцентезом, возможно определение повышенного уровня специфичного Ig M (чувствительность 69%), обнаружение анемии, тромбоцитопении, гипербилирубинемии, повышение трансаминаз печени. Возможно культивирование АЖ, куда вирус выделяется почками плода, проведение ПЦР. При отрицательном результате исследования, но при высоком риске инфицирования матери, оно повторяется через 4-8 недель.
Лечение . Специфического лечения не существует. Возможно применение ганцикловира и фоскарнета при ЦМВ ретините у ВИЧ инфицированных (СПИД). Ведется работа над вакциной, т.к. антитела к ЦМВ, хотя и не уничтожают вирус и не исключают внутриутробного заражения (у большей части новорожденных, инфицированных внутриутробно, матери имели антитела к ЦМВ ), все же значительно снижают риск инфекции, и её тяжелых последствий для плода и новорожденного.
Скрининг на ЦМВ инфекцию не рекомендуется:
а) дорого, б) большинство случаев врожденной ЦМВ инфекции регистрируется у женщин с антителами к вирусу, в) наиболее вероятный исход беременности, осложненной ЦМВ инфекцией — рождение нормального ребенка .
Изоляция ЦМВ инфицированных пациентов , в т. ч. и новорожденных не требуется . Необходимо ограничиться стандартными мерами контроля за распространением инфекционных заболеваний.
III. Варицелла-зостер (ветрянка).
Возбудитель — ДНК содержащий вирус группы герпеса. Относится к «детским» инфекциям. Очень заразен, но у большинства населения (более 90%) встречается до репродуктивного возраста. Характерны типичные поражения кожи: макуло-папулезная сыпь, переходяшая в везикулезную, далее- в пустулезную с образованием корок и расчесов. Процесс самоограничен. Заболевание взрослых- реактивация латентной вирусной инфекции, проявляющейся болезненной везикулезной сыпью по ходу нервов, характерная для лиц пожилого возраста и состояний иммуносупрессии.
Путь распространения- воздушно-капельный, для заражения необходим тесный контакт. Инкубационный период- 10-20 дней (13-17). У детей гипертермия и сыпь появляются одновременно. У взрослых недомогание и гипертермия появляются раньше сыпи на несколько дней. Сыпь начинается с лица и головы, переходит на туловище, конечности поражаются редко. Её развитие сопровождается зудом. Новые высыпания появляются через 2-5 дней, все элементы сыпи существуют одновременно.
Контагиозность: 1-2 суток до сыпи и до отпадения корок. Осложнения включают вторичную бактериальную инфекцию кожи, а также энцефалит, менингит, миокардит, гломерулонефрит, артрит (редко). Очень серьезным осложнением является пневмония, повышающая риск смертности: у взрослых до 5-10%, у детей — реже. На рентгенограмме легких характерны распространенные узелковые перибронхиальные инфильтраты, возможны признаки респираторного дистресса.
Заболеваемость среди беременных низка: 0,5-0,7 случаев на 1000. Беременные болеют не чаще и не тяжелее небеременных женщин, но при пневмонии (9-22%) смертность может достигать 14-30-42%. Лечение проводится ацикловиром 10-15 мг / кг в/в * 3 раза в сутки 7 дней, или 800 мг * 5 раз per os.
У 2/3 беременных, отрицающих заболевание ветрянкой в прошлом, обнаруживаются антитела к вирусу. В тех случаях, где анамнез неясен, антитела обнаруживаются в 90%. При известном контакте беременной с больным В. необходимо определить наличие антител к вирусу (ИФА, ELISA). При их отсутствии необходимо введение специфичного иммуноглобулина в пределах 96 часов от имевшегося контакта: 125 ЕД / 10 кг массы тела (до 625 ЕД) в / м.
Впервые поражение плода при заболевании беременной В. описаны LaForet и Lynch в 1947 г. При заболевании в ранних сроках беременности описаны аборты, мертворождение и уродства: рубцы кожи, гипоплазия конечностей, атрофия коры мозга, умственная отсталость, задержка роста, микрофтальмия, катаракта. Уродства встречаются очень редко : около 1%, но смертность новорожденных в этих случаях достигает 25%. Исследуя различные части плодного яйца можно выявить вирус В. у плода, но невозможно точно установить степень его поражения. Оптимальным методом оценки возможных последствий инфекции является УЗИ до 20 недель беременности , где возможно выявить наличие многоводия, водянки плода, гипоэхогенные очаги в печени, деформации конечностей, часто сопутствующих поражению ЦНС плода.
Антитела матери (Ig G), даже если сероконверсия имела место при беременности, защищают плод. Наибольший риск заболевания новорожденного существует при инфицировании матери за 2 дня до родов и в пределах 5 дней после родоразрешения . При инфицировании матери за 4-5 дней до родов уровень врожденной инфекции у новорожденных составляет 10-20%, а смертность- 20-30%. При инфицировании матери более чем за 5 дней до родов новорожденные рождались с легкими формами инфекции или без её проявлений. Если роды при инфицировании беременной не удается задержать на 5-7 дней, необходима пассивная иммунизация новорожденного непосредственно после родов: 125 ЕД в/м. Иммунизация не предохраняет новорожденного от инфицирования (до 60% инфицируются), но предотвращает летальный исход заболевания. Существует мнение о необходимости иммунизации новорожденного при инфицировании матери в период недели до и после родов.
Разрабатывается вакцина для детей раннего возраста. Её применение позволит покончить с вирусом В., как источником заболеваемости для беременных. Герпес зостер , являясь реактивацией латентной инфекции при наличии антител к вирусу В., не представляет угрозы для здоровья плода и новорожденного .
IV. Корь (рубеола).
Возбудитель- РНК содержащий вирус, относящийся к парамиксовирусам. Заболевание характерно для детского возраста, наиболее заразно среди всех детских инфекций, сопровождающихся сыпью. Клинические проявления: гипертермия, конъюнктивит, кашель, макулопапулезная сыпь, обычно появляющаяся через 1-2 дня после появления патогномоничных пятен Коплика-Филатова в полости рта. Передается воздушно-капельным путем. Инкубационный период: 10-14 дней, наибольшая контагиозность в период продрома и стадию катаральных явлений (заболевают 3/4 от контактировавших с больным). Подъем заболеваемости К. имеет периодичность в 2-3 года (до начала вакцинации). Живая вакцина против кори применяется с 1963 г. Как осложнения возможны отит, круп, энцефалит (1:1000), миокардит. Заболеваемость К. среди беременных низка . До начала вакцинации она составляла 0,4-0,6/10000. У беременных осложнения редки , наиболее опасным в отношении летальности является бактериальная пневмония.
Для плода риск осложнений (аборт, уродства) не доказан, или очень мал . При наличии клинических проявлений кори у новорожденного в первые 10 дней жизни, следует считать инфекцию врожденной, при появлении клиники заболевания на 14 день или позже-приобретенной постнатально. При врожденной кори смертность доношенных новорожденных до начала применения антибиотиков составляла 20-30% (недоношенных-56%). При антибактериальной терапии и современных методах реанимации смертность значительно ниже.
Лечение при неосложненной К.-симптоматическое, при отите, пневмонии- следует назначать антибиотики с учетом чувствительной флоры. Для профилактики заболевания у неболевших беременных и новорожденных применяется пассивная иммунизация: иммунный сывороточный глобулин (коревой) в дозе 0,25 мл/кг массы в период 6 дней от контакта. Для новорожденных от матерей, заболевших корью за 1 неделю до или после родов, рекомендуется иммунизация в той же дозе. Хотя риск для плода существует лишь теоретически, не рекомендуется использовать живую вакцину при беременности или в пределах 3 месяцев до зачатия (минимальный период от вакцинации до беременности — 1 месяц).
V. Свинка.
Возбудитель- вирус той же группы, что и возбудитель кори. Острая генерализованная инфекция с преимущественным поражением околоушных и других слюнных желез, кроме того, могут поражаться мозг, поджелудочная железа, гонады. Путь передачи заболевания — воздушно- капельный: через капельки слюны. Вирус выделяется из слюны за 7 дней до начала паротита и в течение 9 дней после. Инкубационный период: 14-18 дней. Болеют в основном дети до 15 лет, после этого возраста регистрируются только 10% случаев заболевания. Треть взрослых имеют иммунитет к заболеванию, как следствие клинической или субклинической инфекции. Свинка менее заразна, чем ветрянка или корь, но среди беременных она встречается чаще: 0,8-10/10000. Продром проявляется в виде лихорадки, недомогания, миальгии, анорексии. Через 24 часа появляются явления паротита, чаще двустороннего. Подчелюстные железы поражаются реже, и всегда при явлениях паротита. Подъязычные железы поражаются редко. Обычно заболевание не дает осложнений и заканчивается самостоятельно. Но изредка осложнения все же возможны: оофорит, асептический менингит (всегда с благоприятными исходами), а также панкреатит, мастит, тиреоидит, миокардит, нефрит, артрит. У беременных инфекция протекает легко и не отличается от течения у небеременных . При заболевании паротитом в 1 триместре беременности отмечен рост числа самопроизвольных абортов в 2 раза. Уровень недонашивания, задержки роста плода, перинатальной смертности не меняются. Связь заболевания с эндокардиальным фиброэластозом новорожденных, с врожденными аномалиями развития считается не доказанной . Диагноз ставится на основании клинических проявлений, при неясной клинической картине требуется изоляция вируса или, чаще, серологические тесты: фиксация комплимента, торможение гемагглютинации, титр нейтрализующих антител в парных сыворотках (острая инфекция- выздоровление). Лечение- симптоматическое. Прерывание беременности не требуется . Возможна вакцинация живой вакциной (у 95% привитых появляются антитела к вирусу). Длительность последующей защиты от инфицирования- не установлена. Хотя риск для плода является лишь теоретическим, иммунизация живой вакциной при беременности не рекомендуется.
VI. Инфлюэнца (грипп).
Возбудитель относится к миксовирусам. По антигенному составу различают три типа вируса. Тип А является причиной большинства эпидемий и наиболее тяжелых случаев заболевания. Тип В реже является причиной эпидемий и характерен мягкими формами течения заболевания. Тип С наиболее редко встречающийся возбудитель заболевания.
Частота и тяжесть заболевания связаны с изменением в антигенной структуре вируса. Значительные изменения происходящие с интервалом в 10-30 лет приводят к тяжелому течению инфекции, ежегодные незначительные изменения в антигенной структуре вируса таких последствий не имеют. Инкубационный период продолжается 1-4 дня. Клинические проявления, начинаясь внезапно, продолжаются около 3 дней. Диагноз подтверждается выделением вируса из смывов глотки (острый период) или 4-х кратным подъемом титра антител в парных сыворотках: острый период — реконвалесценция. Возможно проведение тестов фиксации комплемента или торможения гемагглютинации.
Наиболее опасным осложнением у беременных является угрожающая жизни пневмония. По данным, полученным при эпидемиях 1918 и 1957 гг., беременные составляли наиболее обширную группу среди умерших от гриппа. Материнская смертность при заболевании гриппом в пандемию 1918 г. составила около 30%, а в случаях, осложненных пневмонией- до 50% . В пандемию 1957 г. до 50% всех случаев смерти при заболевании гриппом приходилось на беременных.
Влияние на плод незначительно . Сведения об уродствах плода противоречивы: там, где связь с уродствами плода найдена, они наиболее вероятны при заболевании в 1 триместре беременности (5,3%), и наиболее характерными являются пороки сердца. Но в ряде исследований связь заболевания гриппом с аномалиями плода отрицается. То же касается и других осложнений беременности. Большинство беременных, заболевших гриппом, имеют нормальный перинатальный исход .
Лечение инфлюэнцы- симптоматическое, при признаках пневмонии, которая у беременных течет тяжелее, необходима госпитализации и антибиотикотерапия. Применение при беременности амантадина не рекомендуется, т. к. у животных отмечено его тератогенное действие. Возможна вакцинация препаратами убитого вируса, которые безопасны для беременных, и одинаково эффективны, как и вне беременности .
VII. Энтеровирусы
Представлены тремя подгруппами РНК содержащих пикорновирусов:
1. Полиовирусы представлены вирусом полиомиелита. У беременных может вызывать аборты, мертворождение, задержку роста плода, у новорожденных- полиомиелит. Вирус может передаваться плоду через плаценту, но 2/3 беременных с клиническими проявлениями полиомиелита рождают здоровых новорожденных. Тератогенного эффекта у вируса полиомиелита не отмечено.
2. Эховирусы , насчитывают примерно 33 вида, могут вызывать респираторные заболевания, гастроэнтериты, конъюнктивиты, менингиты, перикардиты. Осложнений беременности: абортов, преждевременных родов, мертворождений, уродств — не отмечено. Может быть причиной инфекции у новорожденных (возможно врожденной): лихорадка, спленомегалия, ЛАП, сыпь, понос, рвота, отит, пневмония, менингит, желтуха. Специфического лечения или вакцины не существует.
3. Вирусы Коксаки представлены двумя группами: А (23 типа) и В (6 типов). Вирусы группы А за редкими исключениями не вызывают перинатальной заболеваемости. Вирусы группы В могут вызывать менингоэнцефалит, миокардит и, редко, гепатит, пневмонию, гемолитико-уремический синдром. Возможны уродства плода. Доказана передача вируса плоду через плаценту. Риск для плода не определен. Большинство случаев инфекции у матери не дает осложнений беременности и проходит без последствий для плода.
Диагноз возможен при изоляции вируса из глотки или прямой кишки, при регистрации подъема титра антител в период выздоровления, тестами торможения гемагглютинации, фиксации комплимента.
VIII. Вирус папилломы человека.
У лиц с нормальной цитологией шейки матки вирус выделен в 6% случаев, при дисплазии шейки- в 60% случаев. Остроконечные кондиломы, являющиеся следствием инфекции, могут вызывать крайний дискомфорт, трудности при дефекации и мочеиспускании, быть причинами кровотечения. Основной путь передачи- половой (контакт с кожей), но возможны и другие пути: через белье. Контагиозность относительно высокая. У новорожденных возможен респираторный папилломатоз. Кондиломы во время родов отмечены у 60% их матерей.
Наиболее часто инфицирование происходит в возрасте 16-25 лет. Инкубационный период составляет 3-8 месяцев. Диагноз основан на клинических проявлениях заболевания: кондиломы имеют вид мягких разрастаний несколько мм в диаметре, высота их чаще больше, чем ширина, могут быть одиночными или групповыми. Редко встречаются «гигантские» К. более 3 см в диаметре. Чаще находятся в увлажненных местах тела: преддверии влагалища, влагалище. Очень мелкие плоские разрастания, видимые только при кольпоскопии, часто располагаются на шейке матки. Необходимо различать широкие кондиломы, встречающиеся при сифилисе (провести серологические тесты). При атипичных формах может потребоваться биопсия для исключения злокачественности.
Респираторный папилломатоз у детей в 1/3-1/2 случаев проявляется к возрасту 5 лет.
Наиболее часто поражаются голосовые связки, характерный симптом- хрипота. Возможны симптомы обструкции дыхательных путей. В 90% случаев выделяется ВПЧ типов 6 и 11. У 60% женщин, чьи дети больны респираторным папилломатозом, выделена ДНК ВПЧ. Риск перинатального контакта с ВПЧ имеют 2-5% всех новорожденных. Но респираторная форма инфекции является редкостью : 0,04% от всех родов через влагалище, или 1:80-1:1500 при наличии у матери ВПЧ. Передача вируса происходит в родах, но возможно и внутриутробное заражение. Риск заражения ВПЧ в 10 раз меньше, чем вирусом простого герпеса. Учитывая редкость передачи заболевания, возможность внутриутробного заражения, кесарево сечение не рассматривается, как метод профилактики ВПЧ инфекции у новорожденных .
Лечение беременных. При беременности не следует использовать подофиллин (токсичен, возможен тератогенез), 0,5% подофилокс, 5-флуороурацил (интоксикация плода, возможны уродства при применении в 1 триместре), интерфероны (малоэффективны). Возможно местное применение три- и бихлоруксусной кислот. Одна аппликация приводит к излечению только в 20-30% случаев, поэтому требуются повторные процедуры через 7-10 дней. Возможна комбинация с лечением лазером. Криохирургия применяется при поражении вульвы, влагалища, шейки матки. При крупных кондиломах возможно хирургическое иссечение в сочетании с электрокоагуляцией, кюретажем.
IX. Парвовирус человека.
Относится к ДНК содержащим вирусам. Патогеном для человека является только тип В 19. Имеет склонность к гемопоэтической системе, токсичен для клеток эритроидного ряда. Вызывает транзиторную апластическую анемию, наиболее частым проявлением является заболевание характерное для детского возраста: инфекционная эритема (пятая болезнь). Доказана возможность внутриутробного инфицирования и неиммунной водянки плода.
Вирус широко распространен во всем мире у детей 5-14 лет. Наличие антител к вирусу (Ig G) зависит от возраста: в 1-5 лет-2-15%, в 5-19 лет-15-60%, у взрослых-30-60% . Примерно 50-75% женщин репродуктивного возраста имеют антитела к вирусу .
Клинические проявления заболевания характерны для детского возраста: отмечена сезонность подъема заболеваемости (зима-весна), клиника «мягкая», проявляется лихорадкой с последующей эритематозной сыпью на лице («след пощечины»), переходящей на конечности. У взрослых заболевание протекает чаще бессимптомно, но возможны артриты, аденопатия без сыпи. Контагиозность вируса высокая: инфицируются до 60-80% членов семьи, имевших контакт с больным, риск инфицирования у социальных служащих (учителя, воспитатели) составляет 20-30%.
Вне эпидемии ежегодный уровень сероконверсии составляет для медработников 0,42%, для работников школы-2,93%. В эпидемию уровень сероконверсии поднимается до 20-40%. Для отдельного человека риск инфицирования на рабочем месте в 2 раза превышает таковой при пребывании дома. Беременным, не имеющим антител к вирусу, следует избегать контакта с больными гемолитической анемией, сопровождающейся лихорадкой, или апластическим кризом.
Диагностика осуществляется на основании клинической картины, серологических тестов (Ig G и Ig M методом ELISA), культурального метода, ПЦР, а также при выявлении типичных изменений в клетках- предшественниках эритроцитов.
При передаче плоду возможно развитие апластической анемии (разрушение эритроцитов) и, как следствие, через 4-6 недель после инфицирования матери (через 1-12 недель)- неиммунная водянка плода. Частота водянки составляет около 26%, смертность плодов- 10-16% . Но в большинстве случаев инфекция матери не влияет на исходы беременности для плода . По данным последних иследований смертность плодов среди инфицированных беременных составила 5,9%. Инфицирование беременных не сопровождалось ростом числа преждевременных родов, уродств плода и снижением его массы. Поэтому, по современным представлениям, риск для плода при инфицировании матери парвовирусом низок .
Женщины, имевшие контакт с больными инфекционной эритемой при беременности, должны быть обследованы с применением серологических тестов на наличие антител (Ig G и Ig M) к парвовирусу. При наличии антител (иммунитет) проводится обычное наблюдение. При их отсутствии необходимо предостеречь беременную от возможного контакта, особенно во время эпидемии пятой болезни (учителя, социальные работники). При отсутствии Ig G, но при наличии Ig M (острая инфекция) необходимо оценить возможность развития водянки плода. Необходимо серийное измерение уровня альфа-фетопротеина у матери (подъём до развития водянки), а при его повышении- проведение УЗИ.
При развитии водянки плода возможны два варианта ведения беременной.
Первый — проведение внутриутробной гемотрансфузии посредством кордоцентеза;
второй — консервативное ведение, т.к. отмечено, что водянка плода исчезает самостоятельно через 4-6 недель. Гемотрансфузию целесообразно проводить у плодов с гестационным возрастом до 20-22 недель, когда существует риск внутриутробной гибели плода. Плоды более старшего возраста, с более функционально развитой иммунной системой, лучше переносят инфекцию парвовирусом, что допускает консервативное ведение беременности.
Методов лечения и вакцины против парвовирусной инфекции не существует . Единственным методом профилактики является исключения контактов с больным.
Риск смерти плода у беременных с неясным серологическим статусом составляет 1:500-1:4000. Вне эпидемии риск неблагоприятных последствий для плода столь низок, что серологический скрининг и изменение образа жизни беременной не требуются . Но во время эпидемии, когда уровень инфицированности возрастает в 5-20 раз эти меры оправданны, особенно для групп риска по заболеванию: сиделки, учителя начальной школы, работники больниц, где лечатся больные с апластической анемией, лица из домашнего окружения больного ребёнка. Для большинства женщин источником инфекции является больной ребенок школьного возраста, находящийся дома .
X. ВИЧ ИНФЕКЦИЯ ПРИ БЕРЕМЕННОСТИ
Остается неясным влияние беременности на течение ВИЧ инфекции. С одной стороны есть данные об ускорении прогрессирования заболевания при беременности: интервал от заражения до проявлений СПИД сокращается с 6 лет до 2-4 лет. С другой стороны не наблюдается существенных различий в смертности и частоте СПИД у женщин, имевших и не имевших беременность.
При изучении исходов беременности у ВИЧ инфицированных беременных без СПИД не найдено их существенного различия с исходами беременности у неинфицированных женщин. Отмечена более частая госпитализация по поводу бактериальной пневмонии. В то же время при наличии СПИД, когда количество СД 4 (+) клеток становится менее 30%, чаще регистрируются преждевременные роды, мертворождение, низкая масса плода, хориоамнионит, послеродовый эндометрит. В целом, чем тяжелее заболевание, чем выше его стадия, тем более вероятны осложнения беременности .
Вертикальная передача ВИЧ является установленным фактом. Но остаются неясными: время, частота передачи и определяющие её факторы. При абортах у ВИЧ инфицированных женщин инфицирование плодов отмечено в 17%. Передача ВИЧ от матери к новорожденному осуществляется : а) трансплацентарно, б) в родах, посредством инокуляции или заглатывания инфицированной крови или амниотической жидкости, в) после родов через материнское молоко. Если у новорожденного в первые дни и недели жизни имеются признаки ВИЧ-инфицирования (культура, ПЦР, серология), то, скорее всего, инфицирование произошло антенатально (около 50%). При выявлении ВИЧ на 7-90 день жизни и отсутствии грудного вскармливания следует предполагать, что передача вируса произошла во время родов. Уровень перинатальной передачи ВИЧ составляет по современным данным — 20-50%. Отмечалась более высокая вероятность инфицирования первого плода при двойнях (25% против 8%). Ведущим в вертикальной трансмиссии является путь передачи вируса в родах (50-60%). Кесарево сечение не является надежной защитой плода от инфицирования ВИЧ .
Третий путь передачи вируса новорожденному- грудное вскармливание, увеличивающее риск инфицирования ВИЧ вдвое. Матери, получившие вирус с трансфузией зараженной крови, имеют значительно большее число его частиц в крови и молоке и представляют большую опасность для новорожденного, чем матери с хронически и бессимптомно протекающей инфекцией. При наличии СПИД вероятность инфицирования через грудное молоко значительно повышается. Считается, что при возможности искусственного вскармливания ВИЧ инфицированная роженица не должна кормить ребенка грудным молоком . Следует отметить, что ВИЧ чувствителен к теплу, поэтому нагревание грудного молока уменьшает опасность инфицирования.
Выявление ВИЧ инфицированных новорожденных до 18 месяцев жизни возможно лишь путем определения антигена р24 посредством ПЦР или культуральным методом, т.к. IgG, полученный плодом от матери, может определяться в его крови до 15 месяцев после рождения . Использование определения IgA, не проникающего через плаценту, значительно менее точно, чем вышеуказанные методы.
Факторами передачи ВИЧ являются : стадия заболевания, виремия при острой инфекции, количество СД 4 (+) лимфоцитов (при количестве лимфоцитов менее 500 кл/мкл и антигенемии вероятность передачи вируса повышается в 10 раз), роды до 34 недель, способ родоразрешения (операция КС снижает вероятность передачи, но для предотвращения одного случая перинатального инфицирования необходимо оперировать 16 рожениц), повреждение кожи головки плода, гипертермия у роженицы. Противовирусное лечение снижает уровень перинатальной передачи. Но лучший способ снижения перинатальной передачи ВИЧ-предупреждение инфицирования женщин.
ВЕДЕНИЕ БЕРЕМЕННЫХ С ВИЧ. Все женщины, планирующие беременность, должны пройти скрининг на ВИЧ . Важно обращать внимание на факторы риска: партнеры-наркоманы, анамнез гемотрансфузий, ИППП с язвенными поражениями на половых органах. Но более 50% ВИЧ инфицированных женщин не имеют факторов риска . При выявлении ВИЧ инфекции необходима подробная консультация пациента, в ранних сроках беременности целесообразно обсудить возможность её прерывания.
Необходимые мероприятия:
— обратить внимание на возможные проявления ВИЧ инфекции в виде заболеваний различных органов: ЛАП, пневмония, саркома Капоши, увеличение печени и селезенки.
— выявить возможные ИППП: сифилис, хламидиоз, гепатит Б, герпес, антитела к ЦМВ и токсоплазме (исходный титр для последующей диагностики рецидива).
— выявление туберкулеза (папула равная или более 5 мм считается положительной пробой).
— цитологическое исследование шейки матки на наличие злокачественных изменений (мазок с окраской по Папаниколау).
— контроль за иммунологическим статусом: определение числа Т-лимфоцитов (СД 4 и СД 8).
— полезен подсчет клеток крови, тромбоцитов, СОЭ, функциональные тесты печени, контроль за ростом иммуноглобулинов в сыворотке крови.
Лечение. Первым средством, зарегистрированным для лечения ВИЧ инфекции был ЗИДОВУДИН (азидотимидин). У беременных З. быстро проникает через плаценту, а его фармакодинамика не отличается от таковой у небеременных. Это же относится и к дозам препарата. Зидовудин относительно безопасен для плода: уровень уродств (2%) не превышает таковой в общей популяции, признаков гематоинтоксикации не отмечено. Возможно небольшое повышение числа новорожденных с анемией и признаками ВЗРП. При ранних стадиях заболевания З. снижает вертикальную передачу ВИЧ в 3 раза (25,5% и 8,3%).
Лечение беременных зидовудином.
| КОЛИЧЕСТВО СД 4 (+) КЛ. | ТАКТИКА | ПОВТОРНЫЙ ТЕСТ |
| более 600 / мкл (мм 3) | лечение не показано | ч/з 6 мес. |
| 500 — 600 / мкл | лечение можно обсуждать, усилить наблюдение | ч/з 3 мес. |
| 300 — 500 / мкл | рассмотреть возможность лечения, его можно отложить до завершения беременности. Консультация инфекциониста. | ч/з 6 мес. |
| 200 — 300 / мкл | лечение показано, возможна профилактика пневмоцистной инфекции триметопримом. Усилить наблюдение. | ч/з 3 мес. |
| менее 200 / мкл | лечение З. и профилактика пневмоцистной инфекции | по ситуации |
Примерная схема лечения З. при беременности 14-34 нед. и СД 4 (+) более 200/мкл: 100 мг 5 р. в сутки per os, в родах-2 мг/кг в/в в течение 1 часа, далее — 1мг/ кг/час в/в до родоразрешения. Новорожденные: 2 мг/кг через 6 часов per os в течение 6 недель.
Ведение в родах . Родоразрешение консервативное. К.С. для снижения риска перинатальной передачи- не рекомендуется . Применение акушерских щипцов и вакуум-экстракции повышает риск перинатальной передачи вируса.
После родов .
Вышеизложенные меры предосторожности. Новорожденный остается с матерью . По последним данным уровень послеродовых инфекционных осложнений у ВИЧ инфицированных родильниц не превышает таковой у неинфицированных . При уходе за новорожденным использовать перчатки, часто мыть руки, избегать оперативных вмешательств, до уточнения факта инфицирования не проводить вакцинацию живой вакциной. Проводить контроль за наличием и уровнем ВИЧ антител: до их исчезновения или до 15 месяцев жизни. Выделение культуры вируса, положительные данные ПЦР или наличие антигена являются доказательством ВИЧ инфекции в любом возрасте .
БАКТЕРИИ
I. СИФИЛИС (перинатальные аспекты) .
Половина случаев врожденного сифилиса наблюдается у матерей не имевших пренатального врачебного наблюдения. Спирохеты проникают к плоду в любой срок беременности, а не после 16-18 недель, как считали ранее, но в ранних сроках беременности изменений у плода не наблюдается ввиду отсутствия иммунного ответа. Главные факторы, определяющие риск инфицирования плода- концентрация спирохет в крови матери и её стадия заболевания. При нелеченном сифилисе с длительностью заболевания менее 2 лет 50% новорожденных рождаются нормальными, 38% имеют врожденный сифилис, 8,7% — мертворожденные, 4,4%-умирают в течение 2 месяцев после рождения. При нелеченном сифилисе с длительностью заболевания 2-5 лет эти цифры составляют соответственно: 75%-14%-7%-4%. При нелеченном сифилисе с длительностью заболевания более 5 лет после 3 месяцев жизни, соответственно: 81%-6%-6%-7% (1937 г.).
По более современным данным (1952 г.) первичный и вторичный нелеченный сифилис в половине случаев приводит к мертворождению, недонашиванию или смерти новорожденного. Ещё в половине случаев имеется врожденный сифилис. При раннем латентном сифилисе недонашивание составило 20%, мертворождение -16%, смертность новорожденных-4%, врожденный сифилис-40%. Без отклонений от нормы родилось только 20% новорожденных. При позднем сифилисе у матери врожденный сифилис составил только 10%, роста недонашивания и перинатальной смертности не отмечалось.
Исследования 80-х годов подтвердили неблагоприятное влияние сифилиса на исходы беременности. При врожденном сифилисе мертворождаемость составила 35%, а перинатальная смертность-46,4% (1989 г.). При этом частым осложнением беременности остается недонашивание и внутриутробная задержка роста плода, достигающая 21%.
Клинические проявления сифилиса у беременных не отличаются от таковых у небеременных. Подавляющее большинство беременных, больных сифилисом, не имеют симптомов заболевания, которое находится в латентной фазе, а его длительность составляет более 1 года . Врожденный сифилис имеет две фазы. При раннем врожденном С. клинические проявления заболевания появляются в пределах первого года жизни. При позднем врожденном С. симптомы проявляются после 2 лет жизни.
При раннем врожденном сифилисе новорожденные обычно не имеют симптомов заболевания , единственны признаком которого являются положительные серологические тесты. Через 2-6 недель появляются поражения кожи, напоминающие таковые при вторичном С. : располагаются в аногенитальной зоне, на стопах и ладонях. Типична макулопапулезная сыпь, но возможны везикулезные и буллезные высыпания, что нехарактерно для взрослых. Чаще встречаются точечные кровоизлияния в слизистые, широкие кондиломы, которые дают положительный результат на трепонему при исследовании в темном поле. Наблюдается ринит с гнойно-слизистыми выделениями, заложенность носа. Весьма часты трещины на губах и аногенитальной зоне, которые заживая, образуют рубцы. В возрасте 4 месяцев возможны остеохондрит (псевдопаралич Парро), остеит, периостит длинных костей. Примерно у 2/3 новорожденных с ранним врожденным С. наблюдается гепатоспленомегалия, примерно у половины- симптомы менингита. Кроме того, при раннем врожденном сифилисе могут выявляться анемия, лихорадка, ЛАП, «белая» пневмония, ирит, седловидный нос.
Для позднего врожденного С. характерны две основные группы симптомов. К первой группе (сифилитические стигмы) относятся проявления С. явившиеся результатом рубцевания проявлений раннего С. или вызванных им нарушений развития: перфорация носовой перегородки, седловидный нос, утолщение лобных костей, зубы Гатчинсона (выемка на постоянных резцах), моляры в виде ягоды шелковицы, саблевидные голени, рубцы (губы, анус). Вторая группа симптомов является результатом продолжающегося активного воспаления: интерстициальный кератит, нейросифилис, невральная глухота, двусторонний гидрартроз, гуммы.
Диагностика С. осуществляется по общим принципам. Ранний врожденный С. следует подозревать у любого новорожденного с водянкой неизвестного происхождения, большой плацентой, затянувшимся ринитом (сопли), узорчатой непроходящей сыпью, необъяснимой желтухой с гепатоспленомегалией или анемией. Поражения кожи, слизистых и выделения из носа, содержащие спирохеты, необходимо проверить на их наличие при исследовании в темном поле. При позднем врожденном С. типичными проявлениями достаточными для его диагностики являются триада Гатчинсона (зубы, интерстициальный кератит, глухота вследствие поражения 8 пары черепно-мозговых нервов), особая форма моляров и гидрартроз. Окончательный диагноз ставится при обнаружении спирохет при исследовании в темном поле или при гистологическом исследовании.
Для предположительного диагноза необходимо: а) растущие или длительно сохраняющиеся положительные результаты серологических тестов, б) положительные серологические тесты при наличии выделений из носа, широких кондилом, поражений костей, в) положительные серологические тесты при наличии двух или более клинических проявлений С. : гепатоспленомегалия, ЛАП, анемия, неиммунная водянка плода, поражения кожи и слизистых, псевдопаралич Парро, гломерулонефрит, поражение ЦНС.
Вероятный диагноз (подозрение на С.) ставится при наличии положительных серологических тестов при отсутствии клинических проявлений С. Так как положительные серологические тесты могут отражать наличие материнских антител в крови новорожденного, необходимо проведение серийных исследований (рост титра или его персистенция подтверждают наличие врожденного С.) или определение специфичного Ig M.
Лечение . Препаратом выбора для лечения как беременных, так и небеременных является пенициллин. Каждому новорожденному с подозрением на врожденный С. необходимо провести спиномозговую пункцию до начала лечения . Если данные исследования спиномозговой жидкости в пределах нормы, производится одна внутримышечная инъекция бензатин пенициллина в дозе 50 тыс. ед/кг. При патологических результатах или отсутствии пункции новорожденному следует назначить водный раствор кристаллического пенициллина: 50 тыс. ед/кг/сут в течение 10 дней.
Лечение беременных
Ранний сифилис (первичный, вторичный и латентный с длительностью заболевания менее 1 года):
Бензатин пенициллин G 2,4 млн. ед. внутримышечно, одна инъекция
При длительности заболевания более 1 года :
Бензатин пенициллин G 2,4 млн. ед. внутримышечно еженедельно, три инъекции
Нейросифилис:
Водный раствор кристаллического пенициллина G 2-4 млн. ед. внутривенно через 4 часа 10-14 дней с последующей одной внутримышечной инъекцией бензатин пенициллина G в дозе 2,4 млн. ед. или
Водный раствор прокаин пенициллина G 2,4 млн. ед. внутримышечно ежедневно с пробеницидом 500 мг 4 раза/сутки per os в течение 10-14 дней с последующей одной внутримышечной инъекцией бензатин пенициллина G в дозе 2,4 млн. ед.
II. ЛИСТЕРИОЗ.
Инфекция вызывается бактерией Listeria monocytogenes: подвижная неспорообразующая грамположительная палочка. Выделено семь видов, является исключительно патогеном человека. Морфологически неотличима от дифтероидов, поэтому часто «просматривается» при лабораторном иследовании. Выделено 16 серотипов, но 90% всех случаев клинически явной инфекции связаны с тремя серотипами: 46, 1/2в, 1/2а. Микроорганизм легко выделить из стерильной в норме среды (плацента, амниотическая жидкость, кровь), но очень трудно из микробных ассоциаций.
Наиболее чувствительны к инфекции лица с нарушениями иммунитета, а также беременные и их новорожденные. Особые опасения вызывает влияние инфекции на частоту недонашивания и состояние плода. При заболевании беременных листериозом отмечена высокая перинатальная заболеваемость и смертность .
При возможности восходящей инфекции главным путем инфицирования плода является распространение инфекции от заболевшей матери на плаценту, откуда возбудитель попадает к плоду, вызывая у него септицемию с вовлечением множества органов . Амниотическая жидкость инфицируется через поступление бактерий с мочой плода. Аспирация инфицированной амниотической жидкости может приводить к поражению дыхательных путей плода.
Листериоз существует в двух формах: эпидемической и спорадической. Эпидемическая форма связана с употреблением загрязнённых пищевых продуктов.
Во время эпидемии смертность среди взрослых и новорожденных детей составляет примерно 27-33% . Заболевание Л. чаще возникает и наиболее опасно у лиц с нарушением иммунитета: беременных, новорожденных, при пересадке органов, злокачественных заболеваниях, почечной недостаточности, системной красной волчанке, стероидной терапии, ВИЧ инфекции. Чем раньше при беременности наступает инфицирование, тем выше риск гибели плода (незрелая иммунная система). Средний гестационный возраст, в котором произошло инфицирование, у погибших плодов составил 26 недель, а у выживших- 34 недели. Чаще имеют место спорадические (эндемические) формы заболевания. Лица, инфицированные Л. при употреблении заражённой пищи, не имеют симптомов заболевания, становятся хроническими носителями возбудителя в своем желудочно-кишечном тракте. В последующем у женщин наступает колонизация листерией влагалища и шейки матки . Многие инфицированные беременные симптомов заболевания не имеют. Чаще (2/3 случаев) заражение сопровождается клиническими проявлениями (продром): лихорадка, озноб, головная боль, миалгия, боль в спине, поражение верхних дыхательных путей, реже возможны диаррея и боль в животе . Продром представляет стадию бактериемии, когда, вероятно, происходит инфицирование плодного яйца. Через 3-7 дней после этого продрома возможно развитие амнионита с последующими преждевременными родами, септическим абортом, инфекцией плода, мертворождением. Материнская инфекция протекает нетяжело, редко возможен общий сепсис. Чаще Л. наблюдается в III триместре беременности. К сожалению, Л. не имеет специфических клинических проявлений отличающих его от других инфекций, поэтому беременные с подобными симптомами в конце II- начале III триместра должны быть обследованы на наличие Л . В отличии от матери, Л. у новорожденных протекает тяжелее и может закончиться летально (3-50%).
Листериоз у новорожденных представлен двумя серологически и клинически различными видами. Ранний Л. (серотипы Iа и IVв) протекает в форме общего сепсиса с мультиорганным поражением: легкиех, печени, ЦНС, приводит к высокой мертворождаемости и неонатальной смертности, чаще болеют маловесные дети. Инфицирование плода происходит перед родами (во время продрома у матери). Заболевание проявляется в первые часы- дни жизни. Характерны множественные гранулемы, которые чаще находят в плаценте и печени. Они могут быть ключом к диагнозу при неонатальном сепсисе первых дней жизни.
Поздний Л. встречается у доношенных новорожденных при неосложненном течении беременности. Частыми последствиями заболевания являютмя гидроцефалия, задержка умственного развития, а смертность приближается к 40%. Новорожденные при рождении выглядят здоровыми, а заболевание проявляется через несколько дней или недель после родов: явления менингита бывают чаще, чем сепсис. Считается, что заражение происходит в родах или после них: во время прохождения плода через родовой канал или в отделении новорожденных родильного дома.
Учитывая высокую смертность при заболевании новорожденного Л., все беременные с лихорадкой должны обследоваться на наличие инфекции : посев выделений из цервикального канала и крови (учесть сходство с дифтероидами при окраске по Граму: грам-положительные плейоморфные палочки с закругленными концами). Возможно проведение амниоцентеза и исследование на наличие возбудителя Л.
Лечение проводится пенициллином или ампициллином. На сегодняшний день оптимальным считается сочетание ампициллина и аминогликозидов. Лечение матери: ампициллин в/в 1-2,0 каждые 4-6 часов и гентамицин 2 мг/кг в/в через 8 часов в течение недели. Лечение для новорожденного: ампициллин 200-300 мг/кг/сут в 4-6 введениях в течение недели. Лечение, начатое при беременности, может быть успешным и беременность заканчивается рождением здорового новорожденного .
III. ТУБЕРКУЛЁЗ.
По данным США, в период 1985-1992 гг. у женщин детородного возраста отмечен подъем заболеваемости Т. на 41%, а у беременных- в 8 раз (95:100 000 родов). Диагноз основывается на наличии микобактерий в мокроте при микроскопии, но для окончательного диагноза необходимо выделение возбудителя в культуре. У более чем половины беременных наблюдается состояние анергии с отрицательными кожными тестами. Беременность не повышает частоту заражения, не вызывает обострения заболевания даже у ВИЧ- инфицированных, хотя у них Т. встречается чаще.
Врожденный Т. является большой редкостью : опубликовано менее 300 случаев. Более половины матерей не имеют симптомов заболевания. Средний возраст его проявления-24 день жизни (1-84), а наиболее частые признаки: гепатоспленомегалия (76%), респираторный дистресс (72%), лихорадка (48%), ЛАП (38%), увеличение живота (24%), угнетение или возбудимость (21%), выделения из ушей (17%), папулезные высыпания на коже (14%). Большинство новорожденных имеют патологические данные рентгенографии легких, кожные тесты, как правило, отрицательны . Смертность высокая: 38%, среди новорожденных, получавших лечение- 22% .
Лечение . Необходимо избегать назначения стрептомицина (повреждение 8 пары черепно-мозговых нервов до 15%) и этионамида (тератоген). Начинать лечение следует с назначения изониазида, рифампицина, этамбутола. Последний можно заменить на парааминосалициловую кислоту (ПАСК), которая лучше переносится. Кормление грудью разрешается .
Превентивному лечению подлежат:
— ВИЧ инфицированные с туберкулиновой пробой более 5 мм
— Лица, имеющие тесный контакт с вновь выявленным случаем Т. (папула более 5 мм)
— Лица с недавно выявленным инфицированием: туберкулиновая проба более 10 мм в пределах последних двух лет (для лиц старше 35 лет- более 15 мм)
— Лица с рентгенографическими данными, указывающими на фиброзный процесс в легких (папула более 5 мм)
— Лица, принимающие наркотики в/в, при кожном тесте более 10 мм
— Лица с заболеваниями, повышающими риск Т., при кожном тесте более 10 мм
Обычным режимом превентивной терапии является назначение изониазида в дозе 300 мг/сут (при необходимости- дважды в сутки в дозе 15 мг / кг, но не более 900 мг в сут) в течение 6-12 месяцев: лечение в течение года предусмотрено для ВИЧ инфицированных и при патологических данных рентгенологического исследования, в остальных случаях- лечение проводится в течение 6 месяцев. При беременности более 28 недель профилактическое лечение возможно отложить до родоразрешения, при беременности I триместра- до II триместра. Вне зависимости от того, проводится или нет профилактическое лечение, всем беременным с положительной туберкулиновой пробой (папула более 5 мм) проводится рентгенография легких для выявления возможного активного туберкулеза. Это необходимо для своевременного начала лечения заболевания и для профилактики заражения новорожденного матерью с активным Т. легких.
ПРОСТЕЙШИЕ.
I. ТОКСОПЛАЗМОЗ
Серологические признаки бывшей инфекции наблюдаются у 20-40% жителей США, у жителей Парижа- до 84% . Уровень сероконверсии при беременности составляет 1-2/1000 . Примерно в 1/3 случаев (до 60%) наступает инфицирование плода : треть новорожденных имеют клинические формы, 2/3- субклинические формы заболевания. Уровень инфицирования плода растет с ростом срока беременности , в котором произошло заражение, являясь минимальным в период вскоре после зачатия: для I триместра-14% (клинические формы около 11%), для II триместра- 29%, для III триместра- 59% (в литературе можно встретить и более низкие цифры). Однако тяжесть инфекции у плода и перинатальная смертность выше при заболевании беременной в I триместре . Риск врожденного Т. составляет при сроке беременности (после менструации): 0-2 недели- 0%, 3-10 недель- 2%, 27-30 недель- 22%, 31-34 недели- 67%. У каждой конкретной женщины только один ребенок может иметь Т . Несмотря на 20 лет иследований, роль Т. как возможной причины повторных абортов остается невыясненной.
Как правило, и у взрослых и у новорожденных наблюдается субклиническая форма заболевания. Явные клинические проявления включают: ЛАП (шея), лихорадку, боли в горле, макулопапулезную сыпь, гепатоспленомегалию (редко), лимфоцитоз. Клиника напоминает «грипп» или инфекционный мононуклеоз. В отдельных случаях у взрослых могут встречаться изменения зрения: «туман», боль, светобоязнь, на глазном дне- точечные желто-белые высыпания (местный некротизирующий ретинохориоидит).
Большинство новорожденных с врожденным токсоплазмозом (55%) имеют лишь серологические признаки заболевания . При клинических проявлениях Т. изредка встречается триада: кальцификаты ткани мозга (11%), хориоретинит (22%), гидроцефалия (проявляется позже, в 4% случаев). При остром Т. у беременных возможны выкидыши, преждевременные роды, задержка роста плода.
Диагностика:
1. Гистологическое исследование лимфоузлов с определением возбудителя: трудоемко и малочувствительно,
2. Выделение Т. в культуре: культура тканей (фибробласты мыши)- более быстрый, а интраперитонеальная инокуляция мышам (6 недель с последующим определением специфических антител)- более чувствительный метод,
3. Определение антигена Т. методом имунофлуоресценции (чувствительность ограничена),
4. Серологические тесты (8 методик). Ig G появляется через 1-2 месяца после инфицирования и в низких титрах определяется несколько лет, Ig M появляется в пределах 1 недели от инфицирования и определяется в течение нескольких недель. Отсутствие Ig M и присутствие Ig G в титрах выше 1:1000 указывает на наличие инфицирования в прошлом. Диагноз острого Т. у беременной основан на появлении в крови специфического Ig G (сероконверсия) или подъем его титра через 3 и более недель .
5. Определение ДНК возбудителя: ПЦР в амниотической жидкости — точный и быстрый метод диагностики инфицирования плода,
6. Неспецифические тесты (у новорожденного): лейкоцитоз, УЗИ, энзимы печени. УЗИ: расширение желудочков мозга, повышение эхогенности ткани мозга, печени, утолщение и повышение эхогенности плаценты, гепатомегалия, асцит, перикардиальный и плевральный выпот.
Профилактика
. Состоит в пропаганде мер личной гигиены, что, к сожалению, дает незначительный эффект. Для беременных:
— не есть сырое мясо
— мыть руки после контакта с кошкой
— не убирать фекалии кошки
— домашнее содержание кошек (инфицирование от мышей)
— не кормить кошку сырым мясом
— не трогать бродячих кошек и не пускать их в дом
Целесообразность рутинного скриннинга Т. сомнительна : при низком уровне заболеваемости он очень дорог.
Ведение и лечение . При заболевании матери Т. в I трместре необходимо диагностировать Т. у плода и при положительном результате предложить прерывание беременности. При заболевании Т. в более поздние сроки беременности возможно лечение: сульфадиазин с триметопримом (токсичен для костного мозга), фолиевая кислота. Назначение спирамицина не исключает инфицирование плода. При лечении острого Т. 77% детей рождаются без признаков заболевания, а клиника заболевания проявляется у 5% новорожденных. При отсутствии лечения эти цифры составляют соответственно 39% и 14%. И все же лечение матери остается дискуссионным: неполная эффективность, тератогенность некоторых медикаментов (пириметамин). Но лечение новорожденных с подтвержденным Т. обязательно: пириметамин, сульфадиазин, фолиевая кислота, возможно, спирамицин. Лечение и наблюдение продолжаются в течение года. Без лечения поражения глаз и ЦНС отмечены у 40% инфицированных новорожденных, при лечении- только у 2%.
| Токсоплазмоз | Краснуха | Цитомегаловирус | Вирус простого герпеса | |
| Способ передачи | Фекалии кошек, сырые козье молоко и мясо, | Воздушно- капельный | Секреты тела | |
| 10-40% | 85-90% | 50-80% | 50% | |
| Лечение беременных | Пириметамин, сульфадиазин | нет | Ганцикловир | Ацикловир |
| Необходимость скрининга | нет | да | нет | нет |
| Пожизненный иммунитет | Пожизненный иммунитет | Пожизненное носительство | Пожизненное носительство | |
| Да (при первичной инфекции) | Да (при первичной инфекции) | Да | Да (при первичной инфекции) | |
| Нет | Нет | Редко | Да | |
| Способ родораз- решения | Вагинальный | Вагинальный | Вагинальный | Кесарево сечение (высыпания на половых органах) |
| Нет | Да (активная) | Нет | Нет |
| Cифилис | Гепатит В | ВИЧ | Стрепто- кокки группы В | |
| Способ передачи | Контакт со слизистыми и кожей | Секреты тела | Секреты тела | Половой, орально- фекальный |
| Серопози- тивность в общей популяции | — | 1% хронических носителей | 0,1%(?) | 35% коло- низации половых путей |
| Лечение беременных | Бензатин пенициллин (ретарпен, экстенциллин) | Специфический иммуно- глобулин | Зидовудин (азидо- тимидин) | Пенициллин |
| Необходимость скрининга | да | да | да | нет |
| Состояние после перенесенного заболевания | Пожизненное носительство (нелеченный) | Пожизненный иммунитет (при носительстве) | Пожизненный инфек- ционный процесс | Пожизненная колонизация |
| Риск транс- плацентарной передачи (антенатально) | Да | Редко | Да | Редко |
| Риск инфицирования плода в родах | Нет | Да | Да | Да |
| Способ родораз- решения | Вагинальный | Вагинальный | Вагинальный | Вагинальный |
| Необходимость иммунизации матери и новорожденного | Нет | Да (активная и пассивная) | Нет | Нет |
Литература.
- Акушерство. Под ред. К. Нисвандера, А. Эванса (пер. англ.).-1999 г.
- Дэвис П. А., Готефорс Л. А. Бактериальные инфекции плода и новорожденного (пер. англ.).-М., 1987 г.
- Клиническая патология беременности и новорожденного. Под ред. М. Н. Кочи, Г. Л. Гилберта, Дж. Б. Брауна (пер. англ.).-М., 1986 г.
- Неизвестная эпидемия: герпес. Под ред. Л. Н. Хахалина.-Смоленск, 1997 г.
- Репродуктивное здоровье. Под ред. Л. Г. Клейна, Г. С. Бергера, Д. А. Эдельмана (пер. англ.).-1988 г.
- Complications of pregnancy: Medical, Surgical, Gynecologic, Psychosocial and Perinata l. -4th edition.-Ed. by Sh. H. Cherry, I. R. Merkatz.-1991.
- Sweet R. L., Gibbs R. S. Infectious deseases of the female genital tra ct .-3rd edition.-1995.
(Visited 116 times, 1 visits today)
Перинатальные инфекции (ПИ) - это инфекции, которые могут передаваться от матери к плоду с последующей возможной реализацией внутриутробной инфекции в неблагоприятное течение и окончания беременности, патологию плода и новорожденного. ПИ - это одна из ведущих причин перинатальной заболеваемости и детской смертности. Частота ранней неонатальной заболеваемости и смертности при внутриутробной инфекции варьирует от 5,3 до 27,4%, а мертворождаемость достигает 16,8%. Врожденная инфекционная патология в 36-39% случаев является непосредственной причиной перинатальной смертности.
Необходимо различать термины "внутриутробное инфицирование» и «внутриутробная инфекция".
Под термином "внутриутробное инфицирование" понимают факт внутриутробного заражения, и именно проникновения возбудителей инфекции к плоду, но отсутствие признаков инфекционного заболевания плода.
Внутриутробная инфекция - это процесс распространения инфекционных агентов в организме плода вызывает морфофункциональные нарушения в различных органах и системах, присущих этому инфекционном заболевания, возникающего анте-или интранатально и проявляется перинатальной или после рождения ребенка.
Инфицирование матери не значит инфицирования эмбриона, плода и заболевания новорожденного, поскольку частота внутриутробного инфицирования составляет около 10% всех беременностей, а частота клинически выраженных форм внутриутробных инфекций составляет 0,5-1% в своевременных родов и 3,5-16% по преждевременных.
Факторы риска внутриутробного инфицирования.
К группе высокого риска внутриутробного инфицирования следует относить женщин с такими факторами риска:
возраст беременной и ее мужа (партнера) 35 и более лет, наличие профессиональных вредных факторов и привычек;
генетическая предрасположенность к заболеваниям;
данные соматического анамнеза (наличие хронических воспалительных процессов органов мочевыделительной, дыхательной системы и других экстрагенитальных заболеваний);
раннее начало половой жизни, частая смена половых партнеров;
воспалительные заболевания матки, придатков матки, кольпитах в анамнезе;
длительная внутриматочная контрацепция;
неоднократное искусственное прерывание беременности;
искусственное прерывание беременности с осложненным послеабортные периодом;
самопроизвольное прерывание беременности в разные сроки, беременность без прогрессирования;
пороки развития и антенатальная гибель плода;
осложненное течение послеродового периода в прошлых родах;
плацентарная недостаточность, хронический дистресс и (или) синдром задержки развития плода (СЗРП)
несвоевременное излитие околоплодных вод, аномалии родовой деятельности и отделения последа, выраженный травматизм мягких тканей родовых путей;
кольпиты и бактериальный вагиноз, диагностированные во время беременности;
хирургическая коррекция истмико-цервикальной недостаточности при настоящей беременности;
многоводие, маловодие или плацентарная недостаточность (ПН).
Обращают внимание также на заболевания новорожденного (везикульоз, конъюнктивит, пневмония, синдром дыхательных расстройств, воспалительные заболевания головного мозга, гипотрофия, пустимо-и гепатоспленомегалия, сепсис и др.)., Наличие в семье детей-инвалидов с детства, с детским церебральным параличом (ДЦП) или другими заболеваниями центральной нервной системы различной степени тяжести, с задержкой развития.
Классификация
В зависимости от пути попадания возбудителя инфекции к материнскому организму, а дальше к эмбриона и / или плода различают следующие перинатальные инфекции:
восходящие;
гематогенные (трансплацентарный путь);
трансцидуальни (трансмуральный путь);
Нисходящая (через маточные трубы);
инфекции, передающиеся через молоко матери;
инфекции, передающиеся через кровь и ее компоненты;
госпитальные инфекции;
смешанные (два или более путей инфицирования);
ятрогенные инфекции.
В зависимости от возбудителя: бактериальные, вирусные, спирохетозни, протозойные, смешанные.
Патогенез
Патогенез ВУИ разнообразен и зависит от вида возбудителя, его взаимодействия с эмбрионом (плодом), а также от срока гестации. Возможны следующие последствия фетальной инфекции: врожденная патология, антенатальная гибель плода, преждевременные роды, заражение плода во время родов и др..
Клиника
Клинические проявления и тяжесть перинатальных инфекций зависят от:
вида возбудителя, его вирулентности, специфичности действия, массивности обсеменения, а также от того, является ли инфекция первичной или хронической;
иммунного гомеостаза организма женщины;
стадии инфекционного процесса у беременной;
срока беременности, в котором произошло инфицирование;
пути проникновения возбудителя в организм беременной.
Клиническими особенностями ПИ следует считать общие признаки их проявления у матери и плода.
Общие признаки ВУИ у матери
Наряду с острой форме, существуют стертые, латентные формы заболевания или бессимптомно заболевания.
Клинические проявления не всегда зависят от типа возбудителя, его вирулентности, уровня иммунологической реактивности организма.
Заражение плода и новорожденного может возникнуть вследствие острой инфекции матери или вследствие активации хронической, персистентной инфекции во время беременности.
Активация персистентной инфекции возможна в случае любого нарушения гомеостаза в организме беременной (переохлаждение, стресс, респираторные инфекции).
Перенесенные инфекции не оставляют стойкого иммунитета, поэтому наблюдаются реинфекции, рецидивы.
Заболевания, передающиеся половым путем, значительно увеличивают риск ВИЧ-инфекции, гепатитов В и С, рака шейки матки.
Общие признаки ВУИ у плода.
Сходство проявлений зависимости от срока инфицирования.
Алгоритм обследования беременных с высоким инфекционным риском
После оценки факторов риска внутриутробного инфицирования формируют группы беременных с высоким инфекционным риском, подлежащих обследованию.
Клинико-лабораторное обследование
Клинико-лабораторное обследование беременных с высоким инфекционным риском состоит из стандартных, специфических и дополнительных методов исследования.
Стандартные методы исследования
В случае неосложненного течения беременности до 28 недель осмотр проводят 1 раз в месяц, с 28-го по 36-ю неделю - 1 раз в 2 недели., А после 36-й недели - еженедельно (при наличии вирусной и / или бактериальной инфекции наблюдения за беременной проводят чаще, по показаниям). Регулярно определяют массу тела беременной, ее приложение, высоту дна матки, окружность живота, измеряют пульс, артериальное давление. После 18-20 недель гестации определяют подвижность плода.
Определение группы крови, резус-фактора и титра антител, серологические пробы на Р / Л /, НВ5 и НСЛ-антигены, анализы мочи и крови, биохимические, реологические исследования крови беременных, микроскопия влагалищных мазков, Кольпоцитограмма, посевы из носа, зева и цервикального канала на флору. Исследование крови беременной на титр антител к фосфолипидам, поскольку в этой группе пациенток антифосфолипидный синдром может быть непосредственной причиной самопроизвольных выкидышей и привычного невынашивания.
УЗИ с плацентометрии и биометрией эмбриона и плода необходимо проводить в конце первого триместра, во II триместре - в сроке гестации 16-22 недели, а также в III триместре - в 33 и 36-38 недель беременности.
Ультразвуковое допплерометрическое исследования системы мать-плацента-плод-с 19-20-й недели беременности (при нормальных показателей фето-и маточно-плацентарного кровообращения повторяют каждые 3-4 недели, за нарушение гемодинамики - в процессе и сразу после лечения).
С 32-33 недели беременности назначают КТГ плода, определяют его биофизический профиль. КТГ обязательно повторяют в динамике после курса лечения хронического дистресса плода и перед родами.
Специфические лабораторные методы обследования. Используют бактериоскопические, бактериологические, вирусологические, цитологические, серологические и молекулярно-биологические методы (лигазная цепная реакция, полимеразная цепная реакция).
Дополнительные методы исследования. Дополнительные методы исследования заключаются в биопсии трофобласта и хориона, кордоцентез, амниоцинтези, медико-генетическом консультировании и т.п..
Следует исследовать такие биологические материалы.
Исследование содержания цервикального канала, влагалища, уретры:
бактериоскопическое;
бактериологическое (качественное и количественное) при наличии бактериоурии;
вирусологическое.
Исследование мочи:
бактериоскопическое;
бактериологическое (качественное и количественное)
вирусологическое;
биохимическое (определение нитритов).
Исследование мочи имеет целью выявление бессимптомной бактериурии или подтверждения диагноза манифестных форм инфекции мочевых путей (уретрит, цистит, пиелонефрит).
Бессимптомная бактериурия - наличие в 1 мл средней порции мочи микробных возбудителей в количестве> 105 (100 000) колоний Образование единиц (КОЕ) при отсутствии каких-либо клинических проявлений. Возможна также лейкоцитурия (не обязательно).
Исследование крови на наличие специфических антител. Чаще всего для исследования крови используют серологические методы. Так, иммуноферментным анализом (ИФА) определяют наличие специфических антител IgM, IgG. Чувствительность - 99%, специфичность - 95%. Это необходимо для своевременного выявления IgM-антител или увеличение суммарной концентрации IgM и IgG.
Для повышения достоверности результатов реакция в одном образце материала обязательно следует проводить с двумя видами антисывороток (IgIg класс М и G).
Учитывая возможную гипердиагностику, инфекция должна быть верифицирована не менее чем двумя методами (ИФА и ПЦР). Самую точную информацию о наличии внутриутробного инфицирования и состояние внутриутробного "пациента" в сроке беременности с 16-18 до 32 недель можно получить в современных акушерских стационарах с помощью бактерио-и / или вирусологических исследований околоплодных вод (полученных путем трансабдоминального амниоцентеза) и фетальной крови (путем кордоцентеза). В околоплодных водах определяют также уровень а-ФП (отклонение от нормы, начиная с 17-18-й недели гестации, свидетельствуют о высоком риске перинатальной патологии).
Показания к обследованию на выявление ПИ.
Показаниями к обследованию на выявление возбудителей гонореи, хламидиоза, трихомоноз, кандидоза, бактериального вагиноза является наличие клинических признаков вагинита.
Показаниями к обследованию на выявление вируса герпеса является наличие характерных высыпаний.
Показаниями к обследованию на выявление краснухи:
контакт с больным краснухой при отсутствии иммунитета к краснухе у беременной;
подозрение или наличие симптомов заболевания (сыпь).
Показаниями к обследованию на выявление стрептококков В есть ситуации:
безводный период более 18 часов;
лихорадка в родах (более 38o);
инфицирования старших детей стрептококками группы В;
бактериурия стрептококком группы В.
Тактика врача при ведении беременности
Рекомендуемые следующие подходы к обследованию беременных, лечения и последствий отдельных перинатальных инфекций
Перинатальные инфекции – это инфекции, вызванные бактериями или вирусами, которые могут передаваться от матери к ребенку во время беременности или родов. Перинатальные инфекции включают бактериальные или вирусные заболевания и в некоторых случаях, могут вызвать осложнения при родах. Некоторые перинатальные инфекции передаются половым путем.
Передача многих перинатальных инфекций происходит во время родов, особенно в тех случаях, когда используются инвазивные методы, такие как эпизиотомия или искусственный разрыв мембраны. В других случаях передача может происходить во время беременности, если инфекционный агент пересекает плацентарный барьер, это может произойти также во время кормления грудью, если возбудитель при в грудном молоке.
Частота перинатальных инфекций зависит от типа возбудителя. Например, перинатальная передача ЦМВ происходит в 2-24 случаях на каждую 1000 родившихся живыми детей. Передача генитального герпеса во время беременности от одного до двух на каждую из 2000 беременностей; передача группы бета-стрептококков вызывает неонатальную инфекцию на одного-пять из каждой 1000 родившихся живыми младенцев, и краснухи – 0,02 на каждую 1000 дете. ВИЧ передается от матери к ребенку в 25-40 процентах случаев.
Разновидности перинатальных инфекций
Ниже приводятся некоторые из наиболее распространенных инфекций, которые могут передаваться перинатально.
Хламидиоз
Хламидиоз является наиболее распространенным бактериальным венерическим заболеванием. Большинство женщин с хламидийной инфекцией не имеют явных симптомов. Инфекция влияет на репродуктивный тракт и вызывает воспалительные заболевания тазовых органов, бесплодие и внематочную беременность . Эта инфекция может вызвать преждевременный разрыв мембраны и преждевременные роды. Хламидиоз может быть передан ребенку во время родов и может привести к бленнорее новорожденных (инфекция глаз) в течение первого месяца жизни, и пневмонии в течение одного-трех месяцев. Симптомы хламидийной пневмонии выражаются в кашле и учащенном дыхании. Одышка, как и лихорадка, бывают редко.
Цитомегалии
 Цитомегаловирус (ЦМВ) является распространенным вирусом семейства герпеса. Он содержится в слюне, моче и других жидкостях организма и может передаваться при половом контакте или других формах физического контакта. У взрослых, ЦМВ может вызвать легкие симптомы опухания лимфатических желез, лихорадки и усталости. Многие люди, которые являются носителями данного вируса, не испытывают никаких симптомов вообще. Ребенок может заразиться ЦМВ, если заболеет мать или развивается рецидив инфекции во время беременности. ЦМВ препятствует нормальному развитию плода и может привести к умственной отсталости, слепоте, глухоте или эпилепсии.
Цитомегаловирус (ЦМВ) является распространенным вирусом семейства герпеса. Он содержится в слюне, моче и других жидкостях организма и может передаваться при половом контакте или других формах физического контакта. У взрослых, ЦМВ может вызвать легкие симптомы опухания лимфатических желез, лихорадки и усталости. Многие люди, которые являются носителями данного вируса, не испытывают никаких симптомов вообще. Ребенок может заразиться ЦМВ, если заболеет мать или развивается рецидив инфекции во время беременности. ЦМВ препятствует нормальному развитию плода и может привести к умственной отсталости, слепоте, глухоте или эпилепсии.
Генитальный герпес
Генитальный герпес, который обычно вызывается вирусом простого герпеса второго типа (ВПГ-2), является заболеванием, передающимся половым путем, и вызывает болезненные язвы на половых органах. Женщины, которые имеют первые вспышки генитального герпеса во время беременности имеют высокий риск выкидыша или низкого веса при рождении ребенка. Инфекция может передаваться от матери ребенку во время родов, если мать имеет активную форму болезни. Самым серьезным риском для ребенка является возможность развития энцефалита, с воспалением головного мозга, симптомами раздражительности и плохого аппетита.
Гепатит Б
Гепатит Б является инфекционным вирусом, который вызывает повреждение печени и является ведущей причиной хронических заболеваний печени и цирроза. Ребенок подвергается высокому риску развития гепатита инфекции через контакт с кровью зараженной матери во время родов.
Вирус иммунодефицита человека (ВИЧ)
Подпишитесь на наш Ютуб-канал !
ВИЧ является серьезным, контагиозным вирусом, вызывающим синдром приобретенного иммунодефицита (СПИД). Около 25-40 процентов беременных женщин со ВИЧ передают инфекцию своим новорожденным детям. Симптомы ВИЧ-инфекции у детей раннего возраста выражается признаками задержки развития, хронической молочницы и диареи.
Вирус папилломы человека
 Вирус папилломы человека (ВПЧ), передаваемое половым путем заболевание, которое вызывает генитальные бородавки и может увеличить риск развития некоторых видов рака. ВПЧ может передаваться от матери к ребенку во время родов и привести к трахеальному сужению.
Вирус папилломы человека (ВПЧ), передаваемое половым путем заболевание, которое вызывает генитальные бородавки и может увеличить риск развития некоторых видов рака. ВПЧ может передаваться от матери к ребенку во время родов и привести к трахеальному сужению.
Краснуха (немецкая корь)
Краснуха является вирусом, который вызывает сыпь, лихорадку и симптомы инфекций верхних дыхательных путей. Большинство людей подвергаются краснухе в детстве и вырабатывают антитела к вирусу. Краснуха во время ранней беременности может проходить через плаценту и вызывать серьезные врожденные дефекты, в том числе сердечные аномалии, умственную отсталость, слепоту и глухоту.
Группа бета-стрептококк
Группа бета-стрептококк (СГБ) является наиболее распространенной бактериальной причиной смерти новорожденных в результате инфекций, хотя показатели несколько снизились с появлением антибиотиков . У женщин СГБ может вызвать вагинит и инфекции мочевых путей. Обе инфекции могут вызывать преждевременные роды, и бактерии могут быть переданы ребенку в матке или во время родов. СГБ вызывает пневмонию, менингит и другие серьезные инфекции у детей грудного возраста.
Сифилис
Сифилис – заболевание, которое передается половым путем, и может передаваться от матери к младенцу через плаценту до рождения. До 50 процентов детей, рожденных от матерей с сифилисом, являются преждевременными или мертворожденными, либо умирают вскоре после рождения. Инфицированные младенцы могут иметь серьезные врожденные дефекты. Те дети, которые выживают в младенчестве, могут иметь симптомы сифилиса до двух лет спустя.
Отказ от ответственности: Информация, представленная в этой статье про перинатальные инфекции, предназначена только для информирования читателя. Она не может быть заменой для консультации профессиональным медицинским работником.