Perinatální infekce u těhotných žen. Typy perinatálních infekcí. Klinický protokol z porodnické péče "Perinatální infekce"
– skupina onemocnění plodu a novorozence, která se vyvinou v důsledku infekce v prenatálním období nebo během porodu. Nitroděložní infekce může vést k úmrtí plodu, samovolnému potratu, retardaci intrauterinního růstu, předčasnému porodu, vzniku vrozených vad, poškození vnitřních orgánů a centrálního nervového systému. Metody diagnostiky intrauterinních infekcí zahrnují mikroskopické, kultivační, imunoenzymové a molekulárně biologické studie. Léčba intrauterinních infekcí se provádí pomocí imunoglobulinů, imunomodulátorů, antivirových a antibakteriálních léků.

Obecná informace
Intrauterinní infekce jsou patologické procesy a onemocnění způsobené prenatální a intrapartální infekcí plodu. Skutečná prevalence nitroděložních infekcí nebyla stanovena, nicméně podle zobecněných údajů se nejméně 10 % novorozenců rodí s vrozenou infekcí. Závažnost problému nitroděložních infekcí v pediatrii je dána vysokými reprodukčními ztrátami, časnou novorozeneckou morbiditou vedoucí k invaliditě a postnatální smrti dětí. Problematika prevence nitroděložních infekcí leží v oblasti zvažování porodnictví a gynekologie, neonatologie a pediatrie.

Příčiny intrauterinních infekcí
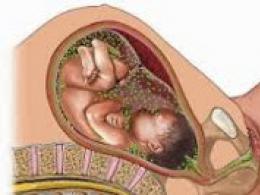
Intrauterinní infekce vznikají jako následek infekce plodu v prenatálním období nebo přímo během porodu. Zdrojem nitroděložní infekce pro dítě je typicky matka, tedy existuje vertikální přenosový mechanismus, který je v prenatálním období realizován transplacentárními nebo ascendentními (přes infikovanou plodovou vodu) cestami a v intranatálním období aspirací popř. kontaktní trasy.
Iatrogenní infekce plodu se v těhotenství vyskytuje méně často, když žena podstupuje invazivní prenatální diagnostiku (amniocentéza, kordocentéza, biopsie choriových klků), zavedení krevních produktů do plodu cévami pupeční šňůry (plazma, červené krvinky, imunoglobuliny ), atd.
V prenatálním období je infekce plodu obvykle spojena s virovými původci (zarděnky, herpes, cytomegalie, viry hepatitidy B a Coxsackie, HIV) a intracelulárními patogeny (toxoplazmóza, mykoplazmóza).
V intranatálním období častěji dochází k mikrobiální kontaminaci, jejíž povaha a rozsah závisí na mikrobiální krajině porodních cest matky. Z bakteriálních původců jsou to nejčastěji enterobakterie, streptokoky skupiny B, gonokoky, Pseudomonas aeruginosa, Proteus, Klebsiella aj. Placentární bariéra je pro většinu bakterií a prvoků neprostupná, pokud je však placenta poškozena a vzniká fetoplacentární insuficience, prenatální může dojít k mikrobiální infekci (například původcem syfilis). Navíc nelze vyloučit intrapartální virovou infekci.
Faktory vzniku nitroděložních infekcí jsou zatížená porodnická a gynekologická anamnéza matky (nespecifická kolpitida, endocervicitida, pohlavně přenosné choroby, salpingoforitida), nepříznivý průběh těhotenství (hrozba potratu, gestóza, předčasné abrupce placenty) a infekční morbidita těhotné . Riziko rozvoje manifestní formy nitroděložní infekce je výrazně vyšší u nedonošených dětí a v případech, kdy je žena primárně infikována během těhotenství.
Závažnost klinických projevů intrauterinní infekce je ovlivněna načasováním infekce a typem patogenu. Pokud tedy dojde k infekci v prvních 8-10 týdnech embryogeneze, těhotenství obvykle končí spontánním potratem. Intrauterinní infekce, které se vyskytují v časném fetálním období (před 12. týdnem těhotenství), mohou vést k narození mrtvého dítěte nebo ke vzniku hrubých malformací. Nitroděložní infekce plodu ve druhém a třetím trimestru těhotenství se projevuje poškozením jednotlivých orgánů (myokarditida, hepatitida, meningitida, meningoencefalitida) nebo generalizovanou infekcí.
Je známo, že závažnost projevů infekčního procesu u těhotné ženy a u plodu se nemusí shodovat. Asymptomatický nebo minimálně symptomatický průběh infekce u matky může způsobit těžké poškození plodu, včetně jeho smrti. To je způsobeno zvýšeným tropismem virových a mikrobiálních patogenů vůči embryonálním tkáním, zejména centrálnímu nervovému systému, srdci a orgánu zraku.
Klasifikace
Etiologická struktura intrauterinních infekcí naznačuje jejich rozdělení na:
Pro označení skupiny nejčastějších intrauterinních infekcí se používá zkratka TORCH syndrom, kombinující toxoplazmózu, zarděnky, cytomegalovirus a herpes simplex. Písmeno O (jiné) označuje další infekce, včetně virové hepatitidy, infekce HIV, planých neštovic, listeriózy, mykoplazmózy, syfilis, chlamydií atd.).
Příznaky intrauterinních infekcí
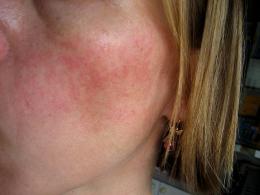
Na přítomnost nitroděložní infekce u novorozence lze mít podezření již během porodu. Intrauterinní infekci může naznačovat odtok zakalené plodové vody, kontaminované mekoniem a nepříjemně zapáchající, a stav placenty (pletora, mikrotrobóza, mikronekróza). Děti s intrauterinní infekcí se často rodí ve stavu asfyxie, s prenatální malnutricí, zvětšenými játry, malformacemi nebo stigmaty dysembryogeneze, mikrocefalie, hydrocefalu. Od prvních dnů života pociťují žloutenku, prvky pyodermie, roseolózní nebo vezikulární vyrážky na kůži, horečku, křeče, respirační a kardiovaskulární poruchy.
Časné novorozenecké období s nitroděložními infekcemi je často zhoršeno intersticiální pneumonií, omfalitidou, myokarditidou nebo karditidou, anémií, keratokonjunktivitidou, chorioretinitidou, hemoragickým syndromem atd. Při instrumentálním vyšetření může jít o vrozený šedý zákal, glaukom, vrozené srdeční vady, cysty a kalcifikace mozku zjištěno u novorozenců.
V perinatálním období dítě zažívá častou a hojnou regurgitaci, svalovou hypotenzi, syndrom deprese centrálního nervového systému a šedou barvu kůže. V pozdějších stádiích, s dlouhou inkubační dobou nitroděložní infekce, je možný rozvoj pozdní meningitidy, encefalitidy a osteomyelitidy.
Uvažujme o projevech hlavních intrauterinních infekcí, které tvoří TORCH syndrom.
Vrozená toxoplazmóza
Po porodu v akutním období se intrauterinní infekce projevuje horečkou, žloutenkou, edematózním syndromem, exantémem, krvácením, průjmem, křečemi, hepatosplenomegalií, myokarditidou, nefritidou, zápalem plic. V subakutním průběhu dominují známky meningitidy nebo encefalitidy. Při chronické perzistenci se rozvíjí hydrocefalus s mikrocefalií, iridocyklitida, strabismus a atrofie zrakového nervu. Někdy se vyskytují monosymptomatické a latentní formy intrauterinní infekce.
Mezi pozdní komplikace vrozené toxoplazmózy patří mentální retardace, epilepsie a slepota.
Vrozená zarděnka
Intrauterinní infekce se vyskytuje v důsledku zarděnek během těhotenství. Pravděpodobnost a následky infekce plodu závisí na gestačním věku: v prvních 8 týdnech riziko dosahuje 80 %; Následky intrauterinní infekce mohou zahrnovat spontánní potrat, embryo- a fetopatii. Ve druhém trimestru je riziko intrauterinní infekce 10-20%, ve třetím - 3-8%.
Děti s intrauterinní infekcí se obvykle rodí předčasně nebo s nízkou porodní hmotností. Novorozenecké období je charakterizováno hemoragickou vyrážkou a prodlouženou žloutenkou.
Vrozená herpetická infekce
Intrauterinní herpetická infekce se může vyskytovat v generalizované (50 %), neurologické (20 %), mukokutánní formě (20 %).
Generalizovaná intrauterinní kongenitální herpetická infekce se vyskytuje s těžkou toxikózou, syndromem respirační tísně, hepatomegalií, žloutenkou, pneumonií, trombocytopenií, hemoragickým syndromem. Neurologická forma vrozeného oparu se klinicky projevuje encefalitidou a meningoencefalitidou. Intrauterinní herpetická infekce s rozvojem kožního syndromu je doprovázena výskytem vezikulární vyrážky na kůži a sliznicích, včetně vnitřních orgánů. Když se rozvine bakteriální infekce, rozvine se novorozenecká sepse.
Intrauterinní herpetická infekce u dítěte může vést ke vzniku vývojových vad - mikrocefalie, retinopatie, hypoplazie končetin (kortikální nanismus). Mezi pozdní komplikace vrozeného herpesu patří encefalopatie, hluchota, slepota a opožděný psychomotorický vývoj.
Diagnostika
V současné době je prenatální diagnostika nitroděložních infekcí naléhavým úkolem. Za tímto účelem se v časných stádiích těhotenství provádí mikroskopie stěru, bakteriologická kultivace pochvy na flóru, PCR vyšetření seškrabů a vyšetření na komplex TORCH. Invazivní prenatální diagnostika (aspirace choriových klků, amniocentéza s vyšetřením plodové vody, kordocentéza s vyšetřením pupečníkové krve) je indikována u těhotných žen s vysokým rizikem rozvoje intrauterinní infekce. detekuje známky.
Léčba nitroděložních infekcí
Obecné zásady pro léčbu nitroděložních infekcí zahrnují imunoterapii, antivirovou, antibakteriální a syndromickou terapii.
Imunoterapie zahrnuje použití polyvalentních a specifických imunoglobulinů, imunomodulátorů (interferonů). Cílená antivirová terapie se provádí především acyklovirem. Pro antimikrobiální terapii bakteriálních intrauterinních infekcí se používají širokospektrá antibiotika (cefalosporiny, aminoglykosidy, karbapenemy) u mykoplazmových a chlamydiových infekcí, makrolidy;
Syndromová terapie nitroděložních infekcí je zaměřena na zmírnění jednotlivých projevů perinatálního poškození centrálního nervového systému, hemoragického syndromu, hepatitidy, myokarditidy, zápalu plic atd.
očkování proti zarděnkám, musí být očkována nejpozději 3 měsíce před očekávaným těhotenstvím. V některých případech mohou být základem pro umělé nitroděložní infekceInfekce plodu během vývoje v těle těhotné ženy může vést k různým infekčním onemocněním spojeným společným názvem - intrauterinní infekce Dítě se může nakazit jednou
osobní patogeny infekčních onemocnění při porodu (při průchodu infikovanými porodními cestami) nebo po porodu (mateřským mlékem a jinými biologickými tekutinami). Infekční onemocnění, která se vyvinula v důsledku těchto důvodů, se nazývají neonatální infekce (intra- a postnatální). Mnoho novorozenců, kteří se nakazí během porodu nebo po něm, může být asymptomatických. U některých z nich, zejména u nedonošených dětí, se však rozvinou závažné klinické projevy onemocnění. Perinatální infekce jsou infekční onemocnění, která vznikají v důsledku infekce plodu během nitroděložního vývoje, během porodu nebo po porodu.
V posledních letech došlo k výraznému nárůstu četnosti vrozených infekcí, převážně virové etiologie. Virové infekce způsobují až 80 % vrozených vývojových vad u dětí, mezi nimi přední místo zaujímají léze centrálního nervového systému a také vrozené vady srdce a ledvin. Četné vědecké údaje naznačují etiologickou souvislost vrozených vývojových vad u dětí s virovými infekcemi prodělanými během těhotenství nebo s transplacentárním přenosem virů z těhotné ženy s přetrvávající formou infekce.
Mezi nejčastější perinatální infekce patří herpes, CMV, parvovirové a toxoplazmové infekce, zarděnky a chlamydie. Včasná diagnostika a léčba těchto infekcí u žen je naléhavým problémem moderní klinické praxe.
Virologické vyšetření novorozenců a těhotných žen umožňuje diagnostikovat virovou infekci u naprosté většiny vyšetřených (až 98 %).
Včasná a včasná diagnostika virové infekce u těhotných žen a vrozené infekce u dětí nám umožňuje vyvinout optimální taktiku terapeutického managementu a racionálně používat antivirotika s cílem snížit pravděpodobnost vývojových vad u dětí.
Při podezření na nitroděložní infekci se těhotné nejčastěji vyšetřují na přítomnost markerů herpetické, CMV, parvovirové, chlamydiové a toxoplazmové infekce a také zarděnek. Negativní výsledky testů ve většině případů vylučují možnost infekce plodu. Pokud existuje podezření na intra- a postnatální infekci, je nutné provést paralelní krevní test matky a dítěte. V tomto případě jsou možné různé situace, které způsobují lékařům potíže při interpretaci výsledků. Nejběžnější z nich jsou uvedeny v tabulce.
Při použití údajů uvedených v tabulce v posudku je nutné vzít v úvahu, že průkaz pouze IgG protilátek u novorozence není příliš vypovídající vzhledem k transplantačnímu průniku mateřských protilátek do jeho těla během nitroděložního vývoje. K vyloučení infekce je proto nutné stanovit dynamiku IgG protilátek u dítěte v 1., 3., 6. a 11.–12. měsíci, a když se objeví klinické příznaky onemocnění, použít metody přímého průkazu patogenu (PCR detekce Ag pomocí RIF nebo ELISA).
V některých případech je při vyšetřování novorozenců na přítomnost intrauterinních infekcí možný falešně negativní sérologický výsledek.
studie vlivem vysoké koncentrace mateřských protilátek třídy IgG, „maskování“ přítomnosti IgM protilátek u dítěte nebo imunologické tolerance (neschopnost organismu reagovat a syntetizovat protilátky). V tomto ohledu je za přítomnosti klinických projevů onemocnění nutné použít metody přímé detekce patogenu.
Tabulka Interpretace výsledků laboratorních vyšetření matky a dítěte
Přítomnost protilátek u matky a dítěte na stejný patogen(y)
Detekce protilátek u matky a jejich absence u novorozence, pokud má klinický obraz onemocnění, a také při vyšetření dítěte narozeného infikované matce
Detekce vysokých titrů IgG protilátek u dítěte brzy po narození
Detekce AT a/nebo patogenů (Ag) u dítěte v nepřítomnosti AT u matky
Titr specifických IgG protilátek v krevním séru dítěte převyšuje titr podobných protilátek u matky (při absenci IgM a IgA protilátek) Přítomnost IgM a/nebo IgA protilátek (pro chlamydie) u dítěte Vzhled IgM a/ nebo IgA protilátky (pro chlamydie) spolu s IgG protilátkami nebo IgG pouze u dříve séronegativního dítěte (sérokonverze)
Přítomnost IgM protilátek ukazuje na vrozenou infekci. Pokud je titr AT IgG zvýšený, je nutné provést dynamickou AT studii po 1-2 měsících. V případě potřeby by měly být použity metody pro přímou detekci patogenu (PCR, detekce Ag pomocí RIF nebo ELISA)
Použijte metody pro přímou detekci patogenu (PCR, detekce Ag pomocí RIF nebo ELISA) u dítěte nebo sledujte titr protilátek v průběhu prvního roku života, protože infekci nelze vyloučit (při syntéze protilátek může dojít k imunologické toleranci nevyskytuje se)
Zvýšený obsah protilátek IgG svědčí spíše o pasivní imunitě přijaté od matky než o vrozené infekci. Pro objasnění situace je nutné studovat titr IgM AT nebo sledovat dynamiku IgG AT (pokud dítě není infikováno, jejich titr prudce klesá do věku 4-6 měsíců) Nitroděložní infekce nebo infekce během porodu; je možné, že se dítě nakazí mateřským mlékem nebo transfuzí krve a jejích složek; V některých případech nelze vyloučit infekci zdravotnickým personálem. Situace je možná u žen, které byly léčeny na infekci, pokud během léčby nebo v prvních měsících po léčbě dojde k těhotenství. Výsledky studie nemohou naznačovat, že je dítě infikováno. Je nutné studovat titr protilátek v čase a používat metody přímého průkazu patogenu (PCR, průkaz Ag pomocí RIF nebo ELISA) Označuje, že dítě je infikováno (protilátky IgM nepronikají do placenty) Označuje primární infekci
Manuál pro lékaře a stážisty
Jaroslavská státní lékařská akademie
Gynekologicko-porodnická klinika
Fakulta dalšího vzdělávání a odborné přípravy zdravotnických specialistů
autoři:
Doktor lékařských věd M.B.Okhapkin, Ph.D. M.V. Khitrov, I.N
(Porodnická a gynekologická klinika Jaroslavské státní lékařské akademie - vedoucí katedry prof. M. B. Okhapkin.)
RECENZENT:
Docent V.P Kiselev, přednosta Kliniky dětských infekčních nemocí Pediatrické fakulty YSMA.
Metodická příručka byla schválena Metodickou komisí pro postgraduální vzdělávání Jaroslavské státní lékařské akademie.
VIRY.
I. Rubella
Rubeola (zarděnka, německy spalničky) je vzdušná infekce a přenáší se nosohltanovým sekretem. Přestože je toto onemocnění typické pro dětský věk, více než polovina všech případů je v posledních letech starších 9 let a ve věku 20-29 let onemocní 19-31 % pacientů ve věku 30 let; nebo starší, 9-31 %. V reprodukčním věku již 75-85 % žen (polovina v subklinické formě) prodělalo zarděnky a má celoživotní imunitu vůči tomuto onemocnění.
Očkování proti zarděnkám je zavedeno od roku 1969 a jeho četnost výrazně klesla: na 1:100 000 populace (podle USA). Problémem je výskyt K. u těhotných žen v časných stadiích. Riziko deformací plodu, pokud je matka nemocná v prvním trimestru těhotenství, je asi 20%(až 50 % v 1. měsíci a 10 % ve 3. měsíci těhotenství). Možné deformity jsou: šedý zákal, otevřený ductus arteriosus, hluchota a za několik let se může vyvinout diabetes.
Virus se uvolňuje z krve a hltanu 7-10 dní po infekci a jeho uvolňování pokračuje asi 1 týden. Onemocnění je doprovázeno vyrážkou, která začíná na obličeji 16-18 dní po infekci, artralgií, lymfadenopatií a horečkou. Ale přítomnost klinického obrazu k diagnostice onemocnění nestačí. K potvrzení infekce se používají různé sérologické testy.
Hemaglutinační inhibiční reakce(Ig G protilátky). Od 5 do 15 % těch, kteří se uzdravili z K., mají protilátky vysoké titry: 1:256. Současně je důkazem imunity vůči K titr 1:8-1:16. Zvýšení titru protilátek proti K při opakovaném testu 4krát a více ukazuje na akutní infekci. V posledních letech byla inhibice hemaglutinace pro jejich větší přesnost a nízkou cenu nahrazena řadou jiných testů: latexová aglutinace, fluorescenční protilátky, pasivní hemaglutinace, hemolýza v gelu, enzymové imunitní testy.
Studie K-specifických Ig M potvrzuje „čerstvou“ infekci (může zmizet z krve za méně než 4-5 týdnů).
Podávání imunoglobulinu G nezabrání ani virémii, ani následnému onemocnění, ale pouze zmírní její příznaky, a proto se nedoporučuje po kontaktu s nemocným K. jako rutinní zákrok. Pouze u žen, které odmítají ukončit těhotenství, může být podání Ig G opatřením k prevenci infekce plodu.
Tabulka 1. Riziko infekce plodu.
| DÉLKA TĚHOTENSTVÍ (TÝDNY) | FETÁLNÍ INFEKCE (%) |
| <11 | 90 |
| 11-12 | 30 |
| 13-14 | 20 |
| 15-16 | 10 |
| > 16 | 5 |
Rezervoárem infekce jsou děti předškolního a základního školního věku. Očkování živou vakcínou má za následek imunitní ochranu v 95 % případů. Nedávno očkovaní jedinci mohou vylučovat virus K, ale jejich kontakt s těhotnými ženami „citlivými“ na virus pro ně nepředstavuje nebezpečí. Ženám citlivým na virus (bez protilátek) se doporučuje očkování, ale je vhodné odložit těhotenství o 90 dní. Pokud je však vakcína aplikována během těhotenství, v prvních 3 měsících je virus detekován v tkáních plodu pouze ve 3 % případů a nezpůsobuje deformace (1,7 %). Očkování je možné v časném poporodním období a není překážkou kojení. Očkování se nedoporučuje při horečce a imunosupresi.
II. Cytomegalie.
Původcem je virus obsahující DNA, který patří do skupiny herpetických virů. V současnosti je považována za nejčastější příčinu nitroděložní infekce. Podle moderních údajů má 0,5–2,5 % všech novorozenců virus při narození a dalších 3–5 % všech novorozenců jej dostane v perinatálním období. Teratogenní potenciál nebyl stanoven. Deformace jako je šedý zákal nebo srdeční vady, jsou vzácné. Velké buňky s jádry obsahujícími inkluze, tzv., charakteristické pro onemocnění. příznak „sovích očí“ (patognomický, ale zřídka se vyskytuje u infikovaných jedinců) je znám od počátku 20. století, ale samotný virus byl izolován až v roce 1956. Po izolaci kultury viru bylo zjištěno, že většina případy infekce probíhají bez klinických projevů.
Epidemiologie. Asi 40 % žen zůstává citlivých na CMV infekci ve svém reprodukčním věku: 45 % žen s vysokým socioekonomickým statusem a 15 % s nízkým. Největší sérokonverze je pozorována ve věku 15-35 let. Každý rok se CMV nakazí 2 % žen s vysokým SES a 6 % s nízkým SES.
Rizikové faktory pro CMV infekci jsou: nízký SES, opakovaná těhotenství, vyšší věk, první těhotenství před 15. rokem věku a počet sexuálních partnerů. Absence rizikových faktorů zvyšuje pravděpodobnost infekce CMV během těhotenství: 1,6–2,2 % těhotných žen „citlivých“ na CMV je infikováno během těhotenství. Nakažlivost CMV je nízká, takže infekce vyžaduje úzký kontakt s nosičem viru: sexuální kontakt, kontakt v domácnosti (děti). Děti navštěvující předškolní zařízení jsou infikovány ve 25–80 % a virus vylučují přibližně 2 roky po infekci. Pokud se jeden člen rodiny nakazí CMV, infikuje polovinu členů rodiny.
V 90 % případů je infekce u dospělých subklinická, ale v 10 % se objevují příznaky podobné mononukleóze: leuko-, lymfocytóza, jaterní dysfunkce, hektická horečka, malátnost, hepatosplenomegalie a žloutenka nejsou nalezeny. Závažné komplikace infekce u dospělých jsou vzácné a jsou pozorovány pouze ve stavu imunodeficience nebo při lékové imunosupresi; jejich výskyt je pravděpodobnější u plodu, zejména s nízkou porodní hmotností (méně než 1200,0). U nemocných se virus neustále uvolňuje do vnějšího prostředí a může představovat nebezpečí infekce po dlouhou dobu: při intrauterinní infekci - 4 roky, při infekci během porodu - 2 roky, u dospělých se uvolňuje periodicky (reinfekce, reaktivace stavy imunosuprese). Těhotné ženy s asymptomatickou infekcí vylučují virus: děložní čípek - 3-18%, močové cesty - 3-9%, mateřské mléko - až 27%, hltan - 1-2%, celkově - 2-28%. Frekvence izolace viru se zvyšuje s průběhem těhotenství: v 1. trimestru - 2,6%, ve 3. trimestru - 7,6%. Hladina protilátek proti CMV v krvi přitom zůstává konstantní.
Intrauterinní CMV infekce se obvykle vyskytuje transplacentárně i když je možná i vzestupná infekce z děložního čípku. Asi 1 % (0,5-2,5) všech novorozenců izoluje CMV při narození (obvykle z moči). Dalších 3-5 % všech novorozenců dostane CMV během porodu a později (cervikální sekrece, transplacentární transfuze, mateřské mléko). Pokud má matka v době porodu CMV infekci v genitálním traktu, bude infikováno 30–50 % novorozenců. Pokud je CMV přítomna v mateřském mléce, 2/3 novorozenců se nakazí do 3 měsíců.
Pokud má matka protilátky proti CMV, vrozená infekce je pozorována u 1,4–1,9 % novorozenců. Když je matka infikována CMV poprvé během těhotenství, až 46–50 % plodů je infikováno in utero, komplikace pro novorozence jsou častější (7–8 % oproti 25–35 %): neurosenzorické poruchy - 5-13%, klinické příznaky infekce - 0- 11-18%, mentální retardace - 0-13%, oboustranná ztráta sluchu - 0-8%.
I přes vysokou frekvenci CMV u matky je hladina infekce u plodu a novorozence 3-4krát nižší. Nejzávažnější následky vrozené CMV infekce jsou pozorovány při infekci plodu v 1. a 2. trimestru těhotenství. Při infekci ve 3. trimestru novorozenec nemá žádné příznaky infekce, ale v krevním séru je zjištěno Ig M Nepřítomnost příznaků infekce při porodu neznamená další pohodu může vést k patologii centrálního nervového systému a neurologickým komplikacím, což jsou hlavní důsledky infekcí.
Při výskytu příznaků CMV (přibližně 10 % infikovaných) u novorozence dosahuje mortalita 20–30 % a 90 % přeživších novorozenců má pozdní komplikace onemocnění: křeče, spastická diplegie, atrofie zrakového nervu, slepota, hluchota, mentální retardace. Ale u infikovaných novorozenců bez příznaků onemocnění (90%) jsou možné i pozdní komplikace: mentální retardace (mikrocefalie nebo hydrocefalus) - 2%, hluchota - 7%, choreoretinitida - 1%, ale mnohem méně často - 10%. U poloviny novorozenců s příznaky onemocnění je typická, i když se podobá projevům jiných známých infekcí: hepatosplenomegalie, žloutenka, trombocytopenická purpura, mikrocefalie, hluchota, choreoretinitida, atrofie zrakového nervu, kalcifikace mozkové tkáně (periventrikulární nebo v subependymální zóna), zpomalení růstu.
Diagnostika těhotných žen infikovaných CMV, zpravidla není diagnostikována kvůli absenci klinického obrazu onemocnění. K potvrzení diagnózy se používají sérologické metody: nepřímá hemaglutinace, nepřímá imunofluorescence, imunosorpce (ELISA), prokazující přítomnost sérokonverze. Protože nejméně asi 40 % dospělých má protilátky proti CMV, jediný výsledek nenaznačuje závažnost infekce: stará nebo „čerstvá“, akutní. Přítomnost specifického Ig M indikuje infekci v následujících 4-8 měsících. Izolace viru v kultuře (může vyžadovat 2 až 6 týdnů) nerozlišuje mezi primární a recidivující infekcí, ale izolace viru z moči nebo děložního čípku potvrzuje asymptomatické přenášení viru, protože během rekurentní infekce se hladina protilátek v těle pacienta mění beze změny. U novorozenci Klinické projevy CMV infekce pro svou nespecifitu nestačí k diagnostice onemocnění, jehož diagnostika vyžaduje laboratorní vyšetření. Sérologické testy jsou považovány za pomocné testy a izolace viru v buněčné kultuře je považována za nejpřesnější. Materiál pro výzkum lze získat z moči, nosohltanu, spojivek a mozkomíšního moku.
Prenatální diagnostika možné pomocí ultrazvuku, amniocentézy, kordocentézy. Ultrazvuk nejčastěji odhalí mikro- a hydrocefalus, cystické změny nebo ložiska kalcifikace (nekrózy) v periventrikulární zóně mozku, jaterní tkáni, placentě, omezení růstu plodu, oligohydramnion, fetální ascites, perikardiální nebo pleurální výpotek, hypoechogenní střevo, hydrops plodu . Ve fetální krvi získané kordocentézou je možné detekovat zvýšenou hladinu specifického Ig M (senzitivita 69 %), detekovat anémii, trombocytopenii, hyperbilirubinémii a zvýšené jaterní transaminázy. Je možné kultivovat AF, kde je virus vylučován ledvinami plodu, a provést PCR. Pokud je výsledek testu negativní, ale existuje vysoké riziko infekce matky, opakuje se po 4-8 týdnech.
Léčba. Neexistuje žádná specifická léčba. Je možné použít ganciklovir a foscarnet pro CMV retinitidu u lidí infikovaných HIV (AIDS). Na vakcíně se pracuje, protože... protilátky proti CMV, ačkoli neničí virus a nevylučují intrauterinní infekci ( Většina novorozenců infikovaných in utero měla matky s protilátkami proti CMV), přesto významně snižují riziko infekce a jejích závažných následků pro plod a novorozence.
Promítání pro CMV infekci Nedoporučeno:
a) drahé, b) většina případů vrozené CMV infekce je registrována u žen s protilátkami proti viru, c) nejpravděpodobnějším výsledkem těhotenství komplikovaného CMV infekcí je narození normálního dítěte.
Izolace pacientů infikovaných CMV, včetně novorozenců není požadováno. Je nutné omezit se na standardní opatření ke kontrole šíření infekčních nemocí.
III. Varicella zoster (plané neštovice).
Původcem je virus herpes skupiny obsahující DNA. Týká se „dětských“ infekcí. Je vysoce nakažlivá, ale vyskytuje se u většiny populace (více než 90 %) před reprodukčním věkem. Charakteristické jsou typické kožní léze: makulopapulózní vyrážka přecházející ve vezikulární vyrážku, poté v pustulární vyrážku s tvorbou krust a škrábanců. Proces je sebeomezující. Onemocněním u dospělých je reaktivace latentní virové infekce, projevující se bolestivou vezikulární vyrážkou podél nervů, charakteristickou pro starší osoby a stavy imunosuprese.
Cesta šíření je vzduchem; pro infekci je nutný úzký kontakt. Inkubační doba je 10-20 dní (13-17). U dětí se hypertermie a vyrážka objevují současně. U dospělých se několik dní před vyrážkou objevuje malátnost a hypertermie. Vyrážka začíná na obličeji a hlavě, rozšiřuje se na trup a zřídka postihuje končetiny. Jeho vývoj je doprovázen svěděním. Nové vyrážky se objevují po 2-5 dnech, všechny prvky vyrážky existují současně.
Nakažlivost: 1-2 dny před vyrážkou a do opadnutí krust. Komplikace zahrnují sekundární bakteriální kožní infekci, stejně jako encefalitidu, meningitidu, myokarditidu, glomerulonefritidu a artritidu (vzácné). Velmi závažnou komplikací je pneumonie, která zvyšuje riziko úmrtnosti: u dospělých až o 5-10%, u dětí - méně často. Rentgen hrudníku ukazuje rozšířené nodulární peribronchiální infiltráty a možné známky respirační tísně.
Incidence mezi těhotnými ženami je nízká: 0,5-0,7 případů na 1000. Těhotné ženy neonemocní častěji nebo vážněji než netěhotné ženy, ale u pneumonie (9-22 %) může úmrtnost dosáhnout 14-30- 42 %. Léčba je s acyklovirem 10-15 mg/kg IV * 3krát denně po dobu 7 dnů nebo 800 mg * 5krát per os.
U 2/3 těhotných žen, které popírají, že v minulosti měly plané neštovice, jsou detekovány protilátky proti viru. V případech, kdy je anamnéza nejasná, jsou protilátky detekovány v 90 %. Pokud je znám kontakt mezi těhotnou a pacientkou s V., je nutné stanovit přítomnost protilátek proti viru (ELISA, ELISA). Při jejich nepřítomnosti je nutné do 96 hodin od stávajícího kontaktu podat specifický imunoglobulin: 125 IU / 10 kg tělesné hmotnosti (až 625 IU) im.
Poprvé poškození plodu při onemocnění těhotné ženy popsali LaForet a Lynch v roce 1947. Při onemocnění v časném těhotenství jsou popsány potraty, mrtvé porody a deformity: kožní jizvy, hypoplazie končetin, atrofie mozková kůra, mentální retardace, retardace růstu, mikroftalmie, šedý zákal. Deformace jsou velmi vzácné: asi 1 %, ale novorozenecká úmrtnost v těchto případech dosahuje 25 %. Vyšetřením různých částí vajíčka je možné identifikovat virus V. v plodu, ale nelze přesně určit rozsah jeho poškození. Optimální metodou pro posouzení možných následků infekce je ultrazvuk před 20. týdnem těhotenství, kde je možné identifikovat přítomnost polyhydramnia, hydropsu plodu, hypoechogenních ložisek v játrech, deformit končetin, často doprovázejících poškození centrálního nervového systému plodu.
Mateřské protilátky (Ig G), i když došlo během těhotenství k sérokonverzi, chrání plod. Největší riziko onemocnění u novorozence existuje, když je matka infikována 2 dny před porodem a do 5 dnů po porodu. Když je matka infikována 4-5 dní před porodem, úroveň vrozené infekce u novorozenců je 10-20% a mortalita je 20-30%. Při infekci matky více než 5 dní před porodem se novorozenci narodili s mírnými formami infekce nebo bez jejích projevů. Pokud porod infikované těhotné ženy nelze oddálit o 5-7 dní, je nutná pasivní imunizace novorozence ihned po porodu: 125 IU IM. Imunizace nechrání novorozence před infekcí (až 60 % se nakazí), ale zabrání smrti na nemoc. Existuje názor na nutnost imunizace novorozence, pokud je matka infikována během týdne před a po porodu.
Vyvíjí se vakcína pro malé děti. Jeho použití umožní skoncovat s virem V. jako zdrojem nemocnosti těhotných žen. Pásový opar, což je reaktivace latentní infekce v přítomnosti protilátek proti viru B, neohrožuje zdraví plodu a novorozence.
IV. Spalničky (rubeola).
Původcem je virus obsahující RNA patřící mezi paramyxoviry. Onemocnění je charakteristické pro dětství a je nejnakažlivější ze všech dětských infekcí doprovázených vyrážkou. Klinické projevy: hypertermie, konjunktivitida, kašel, makulopapulózní vyrážka, objevující se obvykle 1-2 dny po objevení se patognomických Koplikových-Filatovových skvrn v dutině ústní. Přenáší se vzdušnými kapkami. Inkubační doba: 10-14 dní, největší nakažlivost je v prodromu a ve fázi katarálních jevů (onemocní 3/4 kontaktovaných s pacientem). Vzestup výskytu K. má frekvenci 2-3 roky (před zahájením očkování). Živá vakcína proti spalničkám se používá od roku 1963. Možné komplikace jsou zánět středního ucha, krupice, encefalitida (1:1000), myokarditida. Výskyt K. mezi těhotnými ženami je nízký. Před očkováním to bylo 0,4-0,6/10 000. Komplikace jsou u těhotných žen vzácné, nejnebezpečnější z hlediska úmrtnosti je bakteriální zápal plic.
Pro plod není riziko komplikací (potrat, deformity) prokázáno nebo je velmi malé. Pokud se u novorozence objeví klinické projevy spalniček v prvních 10 dnech života, je třeba infekci považovat za vrozenou, pokud se klinické projevy onemocnění objeví 14. den nebo později, je třeba ji považovat za postnatálně získanou. U vrozených spalniček byla úmrtnost donošených novorozenců před nasazením antibiotik 20–30 % (nenarozených – 56 %). Při antibiotické terapii a moderních resuscitačních metodách je mortalita výrazně nižší.
Léčba u nekomplikované K. je symptomatická, u zánětu středního ucha, zápalu plic je třeba předepisovat antibiotika s přihlédnutím k citlivé flóře. K prevenci onemocnění u neonemocněných těhotných žen a novorozenců se používá pasivní imunizace: imunitní sérový globulin (spalničky) v dávce 0,25 ml/kg tělesné hmotnosti do 6 dnů od kontaktu. U novorozenců narozených matkám, které onemocněly spalničkami 1 týden před nebo po porodu, se doporučuje imunizace stejnou dávkou. Přestože existuje pouze teoretické riziko pro plod, nedoporučuje se používat živou vakcínu během těhotenství nebo do 3 měsíců před početím (minimální doba od očkování do otěhotnění je 1 měsíc).
V. Prase.
Původcem je virus ze stejné skupiny jako původce spalniček. Akutní generalizovaná infekce s převažujícím poškozením příušních a jiných slinných žláz, navíc může být postižen mozek, slinivka břišní a pohlavní žlázy. Cesta přenosu onemocnění je vzduchem: prostřednictvím kapiček slin. Virus se izoluje ze slin 7 dní před propuknutím příušnic a 9 dní poté. Inkubační doba: 14-18 dní. Postiženy jsou většinou děti do 15 let, po tomto věku je zaznamenáno pouze 10 % případů onemocnění. Třetina dospělých je vůči této nemoci imunní v důsledku klinické nebo subklinické infekce. Příušnice jsou méně nakažlivé než plané neštovice nebo spalničky, ale jsou častější u těhotných žen: 0,8-10/10 000. Prodrom se projevuje ve formě horečky, malátnosti, myalgie, anorexie. Po 24 hodinách se objevují příznaky příušnic, často oboustranné. Submandibulární žlázy jsou postiženy méně často a vždy s příušnicemi. Sublingvální žlázy jsou postiženy zřídka. Obvykle onemocnění nezpůsobuje komplikace a končí samo. Občas jsou však stále možné komplikace: ooforitida, aseptická meningitida (vždy s příznivými výsledky), stejně jako pankreatitida, mastitida, tyreoiditida, myokarditida, nefritida, artritida. U těhotných žen je infekce mírná a neliší se od průběhu u netěhotných žen.. Při onemocnění příušnicemi v 1. trimestru těhotenství byl pozorován 2násobný nárůst počtu spontánních potratů. Úroveň nedonošenosti, omezení růstu plodu a perinatální mortalita se nemění. Spojení onemocnění s endokardiální fibroelastózou novorozenců, s vrozenými vývojovými anomáliemi je považován za neprokázaný. Diagnóza je stanovena na základě klinických projevů při nejasném klinickém obrazu je nutná izolace viru nebo častěji sérologické testy: fixace komplimentu, inhibice hemaglutinace, titr neutralizačních protilátek v párových sérech (akutní infekce - zotavení) . Léčba je symptomatická. Ukončení těhotenství není nutné. Očkování živou vakcínou je možné (95 % očkovaných si vytvoří protilátky proti viru). Doba trvání následné ochrany před infekcí nebyla stanovena. I když je riziko pro plod pouze teoretické, imunizace živou vakcínou se v těhotenství nedoporučuje.
VI. Chřipka (chřipka).
Původcem je myxovirus. Na základě jejich antigenního složení se rozlišují tři typy virů. Typ A je příčinou většiny epidemií a nejzávažnějších případů onemocnění. Typ B méně pravděpodobně způsobí epidemie a je charakterizován mírnými formami onemocnění. Typ C je nejvzácnější patogen.
Frekvence a závažnost onemocnění jsou spojeny se změnami v antigenní struktuře viru. Významné změny vyskytující se v intervalu 10-30 let vedou k těžkému průběhu infekce každoroční drobné změny v antigenní struktuře viru takové následky nemají. Inkubační doba trvá 1-4 dny. Klinické projevy začínají náhle a trvají asi 3 dny. Diagnóza je potvrzena izolací viru z výtěrů z hltanu (akutní období) nebo 4násobným zvýšením titru protilátek v párových sérech: akutní období - rekonvalescence. Mohou být provedeny testy fixace komplementu nebo inhibice hemaglutinace.
Nejnebezpečnější komplikací u těhotných žen je život ohrožující zápal plic. Podle údajů získaných během epidemií v letech 1918 a 1957 tvořily těhotné ženy největší skupinu mezi zemřelými na chřipku. Mateřská úmrtnost na chřipku během pandemie v roce 1918 byla asi 30 % a v případech komplikovaných zápalem plic až 50 %. Během pandemie v roce 1957 se až 50 % všech úmrtí na chřipku vyskytlo u těhotných žen.
Vliv na plod je zanedbatelný. Informace o fetálních deformitách jsou rozporuplné: tam, kde je nalezena souvislost s fetálními deformitami, se nejčastěji vyskytují v 1. trimestru těhotenství (5,3 %) a nejčastější jsou srdeční vady. Řada studií však souvislost mezi chřipkou a abnormalitami plodu popírá. Totéž platí pro další těhotenské komplikace. Většina těhotných žen, které onemocní chřipkou, má normální perinatální výsledek.
Léčba chřipky je symptomatická, se známkami zápalu plic, který je u těhotných žen závažnější, vyžaduje hospitalizaci a antibiotickou terapii. Užívání amantadinu během březosti se nedoporučuje, protože u zvířat byl zaznamenán jeho teratogenní účinek. Je možné očkovat přípravky s usmrceným virem, které jsou pro těhotné ženy bezpečné a stejně účinné jako mimo těhotenství.
VII. Enteroviry
Jsou reprezentovány třemi podskupinami pikornovirů obsahujících RNA:
1. Polioviry jsou reprezentovány virem dětské obrny. U těhotných žen může způsobit potrat, mrtvé narození, zpomalení růstu plodu a u novorozenců - poliomyelitidu. Virus se může přenést na plod přes placentu, ale 2/3 těhotných žen s klinickými projevy dětské obrny porodí zdravé novorozence. U viru dětské obrny nebyl pozorován žádný teratogenní účinek.
2. Echoviry, existuje přibližně 33 druhů, mohou způsobit onemocnění dýchacích cest, gastroenteritidu, konjunktivitidu, meningitidu a perikarditidu. Nebyly žádné komplikace těhotenství: potraty, předčasné porody, mrtvé porody, deformace. Může vyvolat infekci u novorozenců (pravděpodobně vrozenou): horečku, splenomegalii, tlapku, vyrážku, průjem, zvracení, zánět středního ucha, zápal plic, meningitidu, žloutenku. Neexistuje žádná specifická léčba ani vakcína.
3. Coxsackie viry jsou reprezentovány dvěma skupinami: A (23 typů) a B (6 typů). Viry skupiny A, až na vzácné výjimky, nezpůsobují perinatální morbiditu. Viry skupiny B mohou způsobit meningoencefalitidu, myokarditidu a vzácně hepatitidu, zápal plic a hemolyticko-uremický syndrom. Deformace plodu jsou možné. Byl prokázán přenos viru na plod placentou. Riziko pro plod nebylo stanoveno. Většina případů infekce u matky nezpůsobuje těhotenské komplikace a projde bez následků pro plod.
Diagnóza je možná izolací viru z hltanu nebo rekta, zaznamenáním vzestupu titru protilátek během období zotavení, testy inhibice hemaglutinace a fixací komplimentu.
VIII. Lidsky papillomavirus.
U osob s normální cervikální cytologií byl virus izolován v 6 % případů, v případech cervikální dysplazie - v 60 % případů. Genitální bradavice, které jsou důsledkem infekce, mohou způsobit extrémní nepohodlí, potíže s defekací a močením a způsobit krvácení. Hlavní cesta přenosu je sexuální (kontakt s pokožkou), ale jsou možné i jiné cesty: spodní prádlo. Nakažlivost je poměrně vysoká. U novorozenců je možná respirační papilomatóza. Kondylomy během porodu byly zaznamenány u 60 % jejich matek.
Nejčastěji se infekce vyskytuje ve věku 16-25 let. Inkubační doba je 3-8 měsíců. Diagnóza je založena na klinických projevech onemocnění: kondylomy mají vzhled měkkých výrůstků v průměru několika mm, jejich výška je často větší než šířka, mohou být jednotlivé nebo skupinové. „Obří“ K. o průměru větším než 3 cm se vyskytují zřídka. Nejčastěji se nacházejí na vlhkých místech těla: vestibul pochvy, pochva. Na děložním čípku se často nacházejí velmi malé ploché výrůstky, viditelné pouze při kolposkopii. Je nutné rozlišovat kondylomy lata, které se vyskytují u syfilis (provést sérologické testy). Atypické formy mohou vyžadovat biopsii k vyloučení malignity.
Respirační papilomatóza u dětí v 1/3-1/2 případů se projevuje do věku 5 let.
Nejčastěji jsou postiženy hlasivky, charakteristickým příznakem je chrapot. Mohou se objevit příznaky obstrukce dýchacích cest. V 90 % případů jsou izolovány HPV typu 6 a 11 U 60 % žen, jejichž děti mají respirační papilomatózu, je izolována HPV DNA. 2–5 % všech novorozenců je ohroženo perinatálním kontaktem s HPV. Ale infekce dýchacích cest je vzácná: 0,04 % všech vaginálních porodů nebo 1:80-1:1500, pokud má matka HPV. K přenosu viru dochází během porodu, ale možná je i intrauterinní infekce. Riziko nákazy HPV je 10x menší než u viru herpes simplex. Vzhledem k vzácnosti přenosu onemocnění, možnosti intrauterinní infekce, Císařský řez není považován za metodu prevence infekce HPV u novorozenců.
Léčba těhotných žen. Nesmí se používat během těhotenství podofylin (toxický, možná teratogeneze), 0,5 % podofilox, 5-fluorouracil (intoxikace plodu, možné deformity při použití v 1. trimestru), interferony (neúčinné). Lokální použití tri- a bichloroctových kyselin je možné. Jedna aplikace vede k vyléčení pouze ve 20-30% případů, proto jsou nutné opakované procedury po 7-10 dnech. Je možná kombinace s laserovým ošetřením. Kryochirurgie se používá pro léze vulvy, vagíny a děložního čípku. U velkých kondylomů je možná chirurgická excize v kombinaci s elektrokoagulací a kyretáží.
IX. Lidský parvovirus.
Odkazuje na DNA obsahující viry. Patogenem pro člověka je pouze typ B 19. Má sklon k krvetvornému systému a je toxický pro erytroidní buňky. Způsobuje přechodnou aplastickou anémii, nejčastějším projevem je onemocnění charakteristické pro dětský věk: erythema infectiosum (pátá nemoc). Byla prokázána možnost intrauterinní infekce a neimunitního hydropsu plodu.
Virus je rozšířen po celém světě u dětí ve věku 5-14 let. Přítomnost protilátek proti viru (Ig G) závisí na věku: v 1-5 letech - 2-15%, v 5-19 letech - 15-60%, u dospělých - 30-60%. Přibližně 50–75 % žen v reprodukčním věku má protilátky proti viru.
Klinické projevy onemocnění jsou typické pro dětský věk: je zaznamenán sezónní nárůst incidence (zima-jaro), klinika je „mírná“, projevuje se horečkou následovanou erytematózní vyrážkou na obličeji („fack mark“), šířící se do končetiny. U dospělých je nemoc často asymptomatická, ale je možná artritida a adenopatie bez vyrážky. Nakažlivost viru je vysoká: nakaženo je až 60–80 % rodinných příslušníků, kteří měli kontakt s pacientem, riziko nákazy u sociálních pracovníků (učitelů, vychovatelů) je 20–30 %.
Mimo epidemii je roční míra sérokonverze 0,42 % u zdravotníků a 2,93 % u školních pracovníků. Během epidemie se míra sérokonverze zvyšuje na 20–40 %. Pro jednotlivce je riziko nákazy v práci 2x vyšší než při pobytu doma. Těhotné ženy, které nemají protilátky proti viru, by se měly vyhýbat kontaktu s pacienty s hemolytickou anémií doprovázenou horečkou nebo aplastickou krizí.
Diagnostika provádí se na základě klinického obrazu, sérologických testů (Ig G a Ig M metodou ELISA), kultivační metody, PCR a také identifikací typických změn v prekurzorových buňkách erytrocytů.
Při přenosu na plod se může vyvinout aplastická anémie (destrukce červených krvinek) a v důsledku toho 4-6 týdnů po infekci matky (1-12 týdnů) - neimunitní hydrops fetalis. Incidence hydropsu je asi 26 %, fetální mortalita 10–16 %. Ale ve většině případů infekce matky neovlivňuje výsledky těhotenství pro plod. Podle nedávných studií byla úmrtnost plodu mezi infikovanými těhotnými ženami 5,9 %. Infekce těhotných žen nebyla doprovázena nárůstem počtu předčasných porodů, deformací plodu a snížením jeho hmotnosti. Proto, Podle moderních koncepcí je riziko pro plod, když je matka infikována parvovirem, nízké.
Ženy, které byly během těhotenství v kontaktu s pacientkami s erythema infectiosum, by měly být vyšetřeny pomocí sérologických testů na přítomnost protilátek (Ig G a Ig M) proti parvoviru. Pokud jsou přítomny protilátky (imunita), provádí se rutinní monitorování. Při jejich nepřítomnosti je nutné těhotnou varovat před možným kontaktem, zejména v době epidemie páté nemoci (učitelé, sociální pracovníci). Při absenci Ig G, ale při přítomnosti Ig M (akutní infekce) je nutné zhodnotit možnost rozvoje hydropsu fetalis. Je nutné sériově měřit hladinu alfa-fetoproteinu u matky (vzestup před rozvojem hydropsu), pokud se zvýší, provede se ultrazvuk.
S rozvojem hydropsu fetalis existují dvě možnosti, jak zvládnout těhotnou ženu.
První— provádění intrauterinní krevní transfuze kordocentézou;
druhý— konzervativní řízení, protože Bylo zjištěno, že hydrops plodu zmizí sám o sobě po 4-6 týdnech. Krevní transfuzi je vhodné provádět u plodů s gestačním stářím do 20-22 týdnů, kdy hrozí intrauterinní odumření plodu. Starší plody s funkčně vyvinutějším imunitním systémem lépe snášejí parvovirovou infekci, což umožňuje konzervativní vedení těhotenství.
Proti parvovirové infekci neexistuje žádná léčba ani vakcína. Jedinou metodou prevence je vyhnout se kontaktu s pacientem.
Riziko úmrtí plodu u těhotných žen s nejasným sérologickým stavem je 1:500-1:4000. Mimo epidemii riziko nepříznivých účinků na plod je tak nízké, že sérologický screening a změny životního stylu těhotné ženy nejsou nutné. Ale během epidemie, kdy se úroveň infekce zvýší 5-20krát, jsou tato opatření opodstatněná, zejména u skupin ohrožených onemocněním: zdravotní sestry, učitelé základních škol, pracovníci nemocnic, kde se léčí pacienti s aplastickou anémií, lidé z domova prostředí nemocného dítěte. Pro většinu žen je zdrojem nákazy nemocné dítě školního věku doma.
X. HIV INFEKCE BĚHEM TĚHOTENSTVÍ
Vliv těhotenství na průběh infekce HIV zůstává nejasný. Na jedné straně existují důkazy o zrychlení progrese onemocnění během těhotenství: interval od infekce k projevům AIDS se zkracuje ze 6 let na 2–4 roky. Na druhou stranu nejsou výrazné rozdíly v úmrtnosti a výskytu AIDS u žen, které mají a neměly těhotenství.
Při studiu výsledků těhotenství u těhotných žen infikovaných HIV bez AIDS nebylo zjištěno, že by se významně lišily od výsledků těhotenství u neinfikovaných žen. Byly zaznamenány častější hospitalizace pro bakteriální pneumonii. Současně v přítomnosti AIDS, kdy počet buněk DM 4 (+) klesne pod 30 %, je častěji zaznamenáván předčasný porod, mrtvé narození, nízká hmotnost plodu, chorioamnionitida a poporodní endometritida. Obvykle, čím závažnější je onemocnění, čím vyšší je jeho stadium, tím pravděpodobnější jsou těhotenské komplikace.
Vertikální přenos HIV je prokázanou skutečností. Co však zůstává nejasné, je čas, frekvence přenosu a jeho určující faktory. Při potratech u žen infikovaných HIV byla infekce plodu pozorována v 17 %. Dochází k přenosu HIV z matky na novorozence: a) transplacentárně, b) během porodu, naočkováním nebo požitím infikované krve nebo plodové vody, c) po porodu mateřským mlékem. Pokud má novorozenec známky infekce HIV v prvních dnech a týdnech života (kultivace, PCR, sérologie), pak s největší pravděpodobností k infekci došlo předporodně (asi 50 %). Pokud je HIV detekován v 7. až 90. dni života a nedochází k kojení, mělo by se předpokládat, že k přenosu viru došlo během porodu. Podle aktuálních údajů je úroveň perinatálního přenosu HIV 20–50 %. U dvojčat byla vyšší pravděpodobnost infekce u prvního plodu (25 % vs. 8 %). Vedoucí cestou vertikálního přenosu je cesta přenosu viru během porodu (50-60 %). Císařský řez není spolehlivou ochranou plodu před infekcí HIV.
Třetím způsobem přenosu viru na novorozence je kojení, které zdvojnásobuje riziko infekce HIV. Matky, které dostaly virus transfuzí infikované krve, mají v krvi a mléce výrazně vyšší počet jeho částic a představují pro novorozence větší nebezpečí než matky s chronickou a asymptomatickou infekcí. Pokud máte AIDS, výrazně se zvyšuje pravděpodobnost infekce mateřským mlékem. Předpokládá se, že pokud je možné umělé krmení, neměla by rodící žena infikovaná HIV své dítě kojit. Je třeba poznamenat, že HIV je citlivý na teplo, takže ohřívání mateřského mléka snižuje riziko infekce.
Detekce novorozenců infikovaných HIV do 18 měsíců života je možná pouze stanovením antigenu p24 pomocí PCR nebo kultivace, protože IgG přijaté plodem od matky lze zjistit v jeho krvi až 15 měsíců po narození. Použití placenta-neutrálního IgA je výrazně méně přesné než výše uvedené metody.
Faktory přenosu HIV jsou: stadium onemocnění, virémie při akutní infekci, počet DM 4 (+) lymfocytů (při počtu lymfocytů pod 500 buněk/μl a antigenémii se pravděpodobnost přenosu viru zvyšuje 10x), porod před 34. týdnem, způsob porodu (operace CS snižuje pravděpodobnost přenosu, ale pro zamezení jednoho případu perinatální infekce je nutné operovat 16 rodících žen), poškození kůže hlavičky plodu, hypertermie u rodící ženy. Antivirová léčba snižuje rychlost perinatálního přenosu. Ale nejlepším způsobem, jak snížit perinatální přenos HIV, je zabránit tomu, aby se ženy nakazily.
MANAGEMENT TĚHOTNÝCH ŽEN S HIV. Všechny ženy plánující těhotenství by měly podstoupit screening na HIV. Je důležité věnovat pozornost rizikovým faktorům: drogově závislí partneři, krevní transfuze v anamnéze, STI s ulcerózními lézemi na genitáliích. Ale více než 50 % žen infikovaných HIV nemá rizikové faktory. Při zjištění infekce HIV je nutná podrobná konzultace s pacientkou v raných fázích těhotenství, je vhodné probrat možnost jejího ukončení.
Potřebné činnosti:
— věnujte pozornost možným projevům infekce HIV ve formě onemocnění různých orgánů: PAW, zápal plic, Kaposiho sarkom, zvětšená játra a slezina.
— identifikovat možné STI: syfilis, chlamydie, hepatitidu B, herpes, protilátky proti CMV a toxoplazma (počáteční titr pro následnou diagnózu relapsu).
— zjištění tuberkulózy (papula 5 mm nebo větší se považuje za pozitivní test).
- cytologické vyšetření děložního čípku na přítomnost maligních změn (stěr s barvením Papanicolaou).
— kontrola imunologického stavu: stanovení počtu T-lymfocytů (DM 4 a DM 8).
— užitečné je počítání krvinek, krevních destiček, ESR, jaterní testy, sledování růstu imunoglobulinů v krevním séru.
Léčba. Prvním registrovaným lékem pro léčbu infekce HIV byl ZIDOVUDIN (azidothymidin). U těhotných žen Z. rychle proniká placentou a její farmakodynamika se neliší od farmakodynamiky u netěhotných žen. Totéž platí pro dávky léků. Zidovudin je pro plod relativně bezpečný: míra deformací (2 %) nepřekračuje úroveň v běžné populaci, nebyly zaznamenány žádné známky hematointoxikace. Může dojít k mírnému zvýšení počtu novorozenců s anémií a známkami IUGR. V časných stádiích onemocnění Z. snižuje vertikální přenos HIV 3x (25,5 % a 8,3 %).
Léčba těhotných žen zidovudinem.
| POČET SD 4 (+) CL. | TAKTIKA | ZNOVU TEST |
| více než 600 / µl (mm 3) | léčba není indikována | h/w 6 měsíců |
| 500 – 600 / µl | o léčbě lze diskutovat, pozorování posíleno | h/w 3 měsíce |
| 300 – 500 / µl | Zvažte léčbu; může být odložena až po těhotenství. Konzultace s infekčním specialistou. | h/w 6 měsíců |
| 200 – 300 / µl | je indikována prevence infekce Pneumocystis trimethoprimem. Zvýšit dohled. | h/w 3 měsíce |
| méně než 200/ul | léčba Z. a prevence infekce pneumocystou | záleží na situaci |
Přibližný léčebný režim pro Z. během těhotenství 14-34 týdnů a DM 4 (+) více než 200/μl: 100 mg 5 r. za den per os, během porodu - 2 mg/kg IV po dobu 1 hodiny, poté - 1 mg/kg/h IV až do porodu. Novorozenci: 2 mg/kg každých 6 hodin perorálně po dobu 6 týdnů.
Vedení během porodu. Dodávka je konzervativní. K.S. ke snížení rizika perinatálního přenosu – nedoporučuje se. Použití porodnických kleští a vakuové extrakce zvyšuje riziko perinatálního přenosu viru.
Po porodu .
Výše uvedená opatření. Novorozenec zůstává s matkou. Podle posledních údajů úroveň poporodních infekčních komplikací u HIV infikovaných žen po porodu nepřevyšuje úroveň neinfikovaných žen. Při péči o novorozence používejte rukavice, často si myjte ruce, vyhýbejte se chirurgickým zákrokům a neočkujte živou vakcínou, dokud nebude zjištěna skutečnost, že jde o infekci. Sledujte přítomnost a hladinu protilátek proti HIV: do vymizení nebo do 15 měsíců života. Izolace virové kultury, pozitivní data PCR nebo přítomnost antigenu jsou důkazem infekce HIV v jakémkoli věku.
BAKTERIE
I. SYFILIS (perinatální aspekty).
Polovina případů vrozené syfilis je pozorována u matek, které neměly prenatální lékařský dohled. Spirochety pronikají do plodu v jakékoli fázi těhotenství, a ne po 16-18 týdnech, jak se dříve myslelo, ale v raných stádiích těhotenství nejsou u plodu pozorovány žádné změny kvůli chybějící imunitní odpovědi. Hlavními faktory určujícími riziko infekce plodu jsou koncentrace spirochet v krvi matky a její stadium onemocnění. Při neléčené syfilis s délkou onemocnění do 2 let se 50 % novorozenců rodí normálně, 38 % má vrozenou syfilis, 8,7 % se narodí mrtvě, 4,4 % zemře do 2 měsíců po narození. Pro neléčenou syfilis s trváním onemocnění 2–5 let jsou tato čísla: 75 % -14 % -7 % -4 %. Pro neléčenou syfilis s trváním onemocnění delším než 5 let po 3 měsících života: 81 % -6 % -6 % -7 % (1937).
Podle modernějších údajů (1952) primární a sekundární neléčená syfilis v polovině případů vede k narození mrtvého dítěte, předčasnému porodu nebo smrti novorozence. Další polovina případů má vrozenou syfilis. Na raně latentní syfilis, nedonošenost byla 20 %, mrtvorozenost -16 %, novorozenecká úmrtnost -4 %, vrozená syfilis -40 %. Pouze 20 % novorozenců se narodilo bez odchylek od normy. Na pozdní syfilis U matky byla vrozená syfilis pouze 10%, nedošlo k žádnému zvýšení prematurity a perinatální mortality.
Výzkum v 80. letech 20. století potvrdil nepříznivé účinky syfilis na výsledky těhotenství. U vrozené syfilis byla míra mrtvorozenosti 35 % a perinatální úmrtnost 46,4 % (1989). Častou komplikací těhotenství přitom zůstává nedonošenost a intrauterinní růstová retardace dosahující 21 %.
Klinické projevy syfilis u těhotných žen se neliší od syfilis u netěhotných žen. Naprostá většina těhotných žen se syfilisem nemá příznaky onemocnění, které je v latentní fázi a jeho trvání je více než 1 rok. Vrozená syfilis má dvě fáze. Při časné kongenitální S. se klinické projevy onemocnění objevují během prvního roku života. Při pozdním vrozeném S. se příznaky objevují po 2 letech života.
Při časné vrozené syfilis nemají novorozenci obvykle žádné příznaky onemocnění, jehož jedinými známkami jsou pozitivní sérologické testy. Po 2-6 týdnech se objevují kožní léze, které se podobají lézím sekundárního S.: nacházejí se v anogenitální zóně, na chodidlech a dlaních. Typická je makulopapulózní vyrážka, ale jsou možné vezikulární a bulózní vyrážky, což u dospělých není typické. Častější jsou bodová krvácení do sliznic a condylomas lata, které při vyšetření v tmavém poli dávají pozitivní výsledek na treponém. Je pozorována rýma s purulentním slizničním výtokem a nazální kongescí. Velmi časté jsou praskliny na rtech a anogenitální oblasti, které při hojení tvoří jizvy. Ve věku 4 měsíců je možná osteochondritida (Parroova pseudoparalýza), osteitida a periostitis dlouhých kostí. Asi 2/3 novorozenců s časným vrozeným S. mají hepatosplenomegalii a asi polovina má příznaky meningitidy. Navíc u časné vrozené syfilis lze detekovat anémii, horečku, PAP, „bílou“ pneumonii, iritidu a sedlový nos.
Pro pozdní vrozená S. se vyznačuje dvěma hlavními skupinami příznaků. Do první skupiny (syfilitická stigmata) patří projevy S., které jsou důsledkem zjizvení projevů raného S. nebo jím způsobených vývojových poruch: perforace nosní přepážky, sedlový nos, ztluštění čelních kostí, Hutchinsonovy zuby (zářez na stálých řezácích), stoličky v podobě moruší, šavle holeně, jizvy (rty, řitní otvor). Druhá skupina příznaků je důsledkem probíhajícího aktivního zánětu: intersticiální keratitida, neurosyfilis, nervová hluchota, bilaterální hydrartróza, dásně.
Diagnostika S. se provádí podle obecných zásad. Časně vrozené S. by měl být podezřelý u každého novorozence s hydropsem neznámého původu, velkou placentou, perzistující rýmou (sople), vzorovanou přetrvávající vyrážkou, nevysvětlitelnou žloutenkou s hepatosplenomegalií nebo anémií. Kožní léze, sliznice a výtok z nosu obsahující spirochéty musí být zkontrolovány na jejich přítomnost během vyšetření v tmavém poli. S pozdním vrozeným S. Typickými projevy postačujícími pro její diagnostiku jsou Hutchinsonova triáda (zuby, intersticiální keratitida, hluchota v důsledku poškození 8. páru hlavových nervů), speciální forma molárů a hydrartróza. Konečná diagnóza je stanovena, když jsou spirochety detekovány během vyšetření v tmavém poli nebo histologického vyšetření.
Pro předpokládanou diagnózu je nutné: a) zvyšující se nebo dlouhotrvající pozitivní výsledky sérologických testů, b) pozitivní sérologické testy při přítomnosti výtoku z nosu, condylomas lata, kostních lézí, c) pozitivní sérologické testy při přítomnosti dvou nebo více klinických projevů S.: hepatosplenomegalie , PAP, anémie, neimunitní hydrops fetalis, léze kůže a sliznic, Papouškova pseudoparalýza, glomerulonefritida, poškození centrálního nervového systému.
Pravděpodobná diagnóza (podezření na S.) je umístěn v přítomnosti pozitivních sérologických testů při absenci klinických projevů S. Protože pozitivní sérologické testy mohou odrážet přítomnost mateřských protilátek v krvi novorozence, je nutné provést sériové studie (zvýšení titru popř. jeho perzistence potvrzuje přítomnost vrozeného S.) nebo stanovení specifického Ig M.
Léčba. Penicilin je lékem volby pro léčbu těhotných i netěhotných žen. Každý novorozenec s podezřením na vrozený S. musí před léčbou podstoupit spinální punkci. Pokud jsou údaje o vyšetření mozkomíšního moku v normálních mezích, podává se jedna intramuskulární injekce benzathinpenicilinu v dávce 50 tisíc jednotek/kg. Pokud jsou výsledky patologické nebo nedojde k punkci, je třeba novorozenci předepsat vodný roztok krystalického penicilinu: 50 tisíc jednotek/kg/den po dobu 10 dnů.
Léčba těhotných žen
Časná syfilis(primární, sekundární a latentní s trváním onemocnění kratším než 1 rok):
Benzathine penicilin G 2,4 milionu jednotek. intramuskulárně, jedna injekce
Během trvání onemocnění více než 1 rok:
Benzathine penicilin G 2,4 milionu jednotek. intramuskulárně týdně, tři injekce
Neurosyfilis:
Vodný roztok krystalického penicilinu G 2-4 miliony jednotek. intravenózně po 4 hodinách po dobu 10-14 dnů, poté jednou intramuskulární injekcí benzathinpenicilinu G v dávce 2,4 milionu jednotek. nebo
Vodný roztok prokain penicilinu G 2,4 milionů jednotek. intramuskulárně denně s probenecidem 500 mg 4krát denně per os po dobu 10-14 dnů, poté jednou intramuskulární injekcí benzathinpenicilinu G v dávce 2,4 milionu jednotek.
II. LISTERIÓZA.
Infekce je způsobena bakterií Listeria monocytogenes: pohyblivá grampozitivní tyčinka, která nevytváří spory. Bylo identifikováno sedm druhů, jedná se výhradně o lidský patogen. Morfologicky nerozeznatelný od difteroidů, proto je často „viditelný“ při laboratorním výzkumu. Bylo identifikováno 16 sérotypů, ale 90 % všech případů klinicky zjevné infekce je spojeno se třemi sérotypy: 46, 1/2b, 1/2a. Mikroorganismus se snadno izoluje z normálně sterilního prostředí (placenta, plodová voda, krev), ale velmi obtížně se izoluje od mikrobiálních asociací.
K infekci jsou nejvíce náchylné osoby s narušenou imunitou, stejně jako těhotné ženy a jejich novorozenci. Zvláště znepokojivý je dopad infekce na výskyt nedonošených dětí a stav plodu. V případech listeriózy u těhotných žen je pozorována vysoká perinatální morbidita a mortalita..
Pokud je možná ascendentní infekce, je hlavní cestou infekce plodu šíření infekce z nemocné matky do placenty, odkud se patogen dostane k plodu a způsobí septikémii postihující více orgánů. Plodová voda se infikuje průchodem bakterií močí plodu. Aspirace infikované plodové vody může vést k poškození dýchacích cest plodu.
Listerióza existuje ve dvou formách: epidemická a sporadická. Epidemická forma je spojena s konzumací kontaminovaných potravin.
Během epidemie je úmrtnost mezi dospělými a novorozenci přibližně 27-33%. L. nemoc se vyskytuje častěji a je nejnebezpečnější u osob s narušenou imunitou: těhotné ženy, novorozenci, transplantace orgánů, maligní onemocnění, selhání ledvin, systémový lupus erythematodes, terapie steroidy, infekce HIV. Čím dříve dojde k infekci během těhotenství, tím vyšší je riziko úmrtí plodu (nevyzrálý imunitní systém). Průměrný gestační věk, kdy došlo k infekci, byl 26 týdnů u mrtvých plodů a 34 týdnů u přeživších plodů. Častěji se vyskytují sporadické (endemické) formy onemocnění. Osoby infikované L. požitím kontaminované potravy nemají příznaky onemocnění a stávají se chronickými přenašeči patogenu ve svém trávicím traktu. Následně jsou ženy kolonizovány Listerií v pochvě a děložním čípku. Mnoho infikovaných těhotných žen nemá žádné příznaky onemocnění. Častěji (2/3 případů) je infekce provázena klinickými projevy (prodrom): horečka, zimnice, bolest hlavy, myalgie, bolesti zad, poškození horních cest dýchacích, méně často je možný průjem a bolesti břicha. Prodrom představuje stadium bakteriémie, kdy je pravděpodobný výskyt infekce gestačního vaku. 3-7 dní po tomto prodromu se může rozvinout amnionitida, následovaná předčasným porodem, septickým potratem, infekcí plodu a narozením mrtvého plodu. Infekce matky není závažná; celková sepse je zřídka možná. Častěji je L. pozorován ve třetím trimestru těhotenství. Bohužel L. nemá specifické klinické projevy, které by ji odlišovaly od jiných infekcí, proto Těhotné ženy s podobnými příznaky na konci 2. - začátku 3. trimestru by měly být vyšetřeny na přítomnost L. Na rozdíl od matky je L. u novorozenců závažnější a může být fatální (3-50 %).
Listeriózu u novorozenců představují dva sérologicky a klinicky odlišné typy. Časná L. (sérotypy Ia a IVb) se vyskytuje ve formě celkové sepse s multiorgánovým poškozením: plíce, játra, centrální nervový systém, vede k vysoké mrtvě narozené a novorozenecké úmrtnosti, častěji jsou postiženy děti s nízkou porodní hmotností. K infekci plodu dochází před porodem (během matčina prodromu). Onemocnění se projevuje v prvních hodinách a dnech života. Charakterizováno mnohočetnými granulomy, které se často nacházejí v placentě a játrech. Mohou být klíčem k diagnostice novorozenecké sepse v prvních dnech života.
Pozdní L. se vyskytuje u donošených novorozenců během nekomplikovaného těhotenství. Častými následky onemocnění je hydrocefalus, mentální retardace a mortalita se blíží 40 %. Novorozenci se po narození zdají být zdraví, ale onemocnění se projeví několik dní nebo týdnů po narození: meningitida je častější než sepse. Předpokládá se, že k infekci dochází během porodu nebo po něm: při průchodu plodu porodními cestami nebo na novorozeneckém oddělení porodnice.
Vzhledem k vysoké úmrtnosti u novorozenecké L. nemoci, všechny těhotné ženy s horečkou by měly být vyšetřeny na infekci: kultivace sekretu z cervikálního kanálu a krve (vzhledem k podobnosti s difteroidy při barvení Gramem: grampozitivní pleiomorfní tyčinky se zaoblenými konci). Je možné provést amniocentézu a test na přítomnost patogenu L.
Léčba provádí se penicilinem nebo ampicilinem. Dnes se za optimální považuje kombinace ampicilinu a aminoglykosidů. Léčba matky: ampicilin IV 1-2,0 každých 4-6 hodin a gentamicin 2 mg/kg IV každých 8 hodin po dobu jednoho týdne. Léčba pro novorozence: ampicilin 200-300 mg/kg/den ve 4-6 injekcích během týdne. Léčba zahájená v těhotenství může být úspěšná a těhotenství končí narozením zdravého novorozence.
III. TUBERKULÓZA.
Podle údajů USA v období 1985-1992. U žen ve fertilním věku došlo ke zvýšení výskytu T. o 41 %, u těhotných o 8krát (95:100 000 porodů). Diagnóza je založena na přítomnosti mykobakterií ve sputu pod mikroskopem, ale definitivní diagnóza vyžaduje izolaci patogenu v kultuře. Více než polovina těhotných žen zažívá stav anergie s negativními kožními testy. Těhotenství nezvyšuje četnost infekce a nezpůsobuje exacerbaci onemocnění ani u HIV infikovaných, i když je u nich T. častější.
Vrozená T. je velmi vzácná: Uveřejněno méně než 300 případů. Více než polovina matek nemá žádné příznaky onemocnění. Průměrný věk jeho začátku je 24 dní života (1-84) a nejčastějšími příznaky jsou: hepatosplenomegalie (76 %), respirační tíseň (72 %), horečka (48 %), PAW (38 %), břišní zvětšení (24 %), deprese nebo excitabilita (21 %), výtok z uší (17 %), papulární vyrážky na kůži (14 %). Většina novorozenců má abnormální nálezy na rentgenu hrudníku a kožní testy jsou většinou negativní. Úmrtnost je vysoká: 38 %, mezi léčenými novorozenci - 22 %.
Léčba. Je nutné se vyvarovat užívání streptomycinu (poškození 8. páru hlavových nervů do 15 %) a ethionamidu (teratogen). Léčba by měla začít isoniazidem, rifampicinem, ethambutolem. Ta může být nahrazena kyselinou para-aminosalicylovou (PAS), která je lépe tolerována. Kojení je povoleno.
Preventivnímu ošetření podléhají:
— infikované HIV s tuberkulinovým testem větším než 5 mm
— Osoby, které jsou v těsném kontaktu s nově identifikovaným případem T. (papula větší než 5 mm)
— Osoby s nově diagnostikovanou infekcí: tuberkulinový test více než 10 mm za poslední dva roky (pro osoby starší 35 let - více než 15 mm)
— Osoby s rentgenovými údaji naznačujícími fibrotický proces v plicích (papula větší než 5 mm)
— Osoby užívající nitrožilně léky s kožním testem větším než 10 mm
— Osoby s nemocemi, které zvyšují riziko T., s kožním testem větším než 10 mm
Obvyklý režim preventivní léčby je isoniazid v dávce 300 mg/den (v případě potřeby dvakrát denně v dávce 15 mg/kg, ale ne více než 900 mg denně) po dobu 6–12 měsíců: léčba po dobu jednoho roku je poskytována pro HIV infikované osoby a v případě patologických RTG údajů se v ostatních případech léčba provádí po dobu 6 měsíců. Při těhotenství delším než 28 týdnů lze preventivní léčbu odložit až do porodu během těhotenství v prvním trimestru, až do druhého trimestru; Bez ohledu na to, zda je preventivní léčba prováděna nebo ne, všechny těhotné ženy s pozitivním tuberkulinovým testem (papula větší než 5 mm) podstoupí rentgen hrudníku k identifikaci možné aktivní tuberkulózy. To je nezbytné pro včasné zahájení léčby onemocnění a pro prevenci infekce novorozence matkou s aktivní T. plic.
PROTOZOY.
I. TOXOPLASMÓZA
Sérologické známky dřívější infekce jsou pozorovány u 20–40 % obyvatel USA a až 84 % u obyvatel Paříže. Míra sérokonverze během těhotenství je 1-2/1000. Přibližně v 1/3 případů (až 60 %) dochází k infekci plodu: třetina novorozenců má klinické formy, 2/3 subklinické formy onemocnění. Míra infekce plodu se zvyšuje s gestačním věkem, ve kterém došlo k infekci, minimální v období krátce po početí: za první trimestr - 14 % (klinické formy asi 11 %), za druhý trimestr - 29 %, za třetí trimestr - 59 % (nižší čísla mohou najdete v literatuře). nicméně závažnost infekce u plodu a perinatální úmrtnost jsou vyšší, když těhotná žena onemocní v prvním trimestru. Riziko vrozené T. je v těhotenství (po menstruaci): 0-2 týdny - 0%, 3-10 týdnů - 2%, 27-30 týdnů - 22%, 31-34 týdnů - 67%. U každé ženy může mít T pouze jedno dítě. Přes 20 let výzkumu zůstává úloha T. jako možné příčiny opakovaných potratů nejasná.
Subklinická forma onemocnění je zpravidla pozorována jak u dospělých, tak u novorozenců. Mezi zjevné klinické projevy patří: PAW (krk), horečka, bolest v krku, makulopapulózní vyrážka, hepatosplenomegalie (vzácné), lymfocytóza. Klinika připomíná „chřipku“ nebo infekční mononukleózu. V některých případech mohou dospělí zaznamenat změny vidění: „mlhu“, bolest, fotofobii a přesné žlutobílé vyrážky na fundu (lokální nekrotizující retinochoroiditida).
Většina novorozenců s vrozenou toxoplazmózou (55 %) má pouze sérologické známky onemocnění. V klinických projevech T. se občas setkáváme s triádou: kalcifikace mozkové tkáně (11 %), chorioretinitida (22 %), hydrocefalus (objevuje se později, ve 4 % případů). Pro akutní T. u těhotných žen jsou možné potraty, předčasný porod a retardace růstu plodu.
Diagnostika:
1. Histologické vyšetření lymfatických uzlin s identifikací patogenu: pracné a necitlivé,
2. Izolace T. v kultuře: tkáňová kultivace (myší fibroblasty) je rychlejší metodou a intraperitoneální inokulace u myší (6 týdnů s následným stanovením specifických protilátek) je citlivější metodou,
3. Stanovení T. antigenu imunofluorescencí (citlivost je omezena),
4. Sérologické testy (8 metod). Ig G se objeví 1-2 měsíce po infekci a je detekován v nízkých titrech po několik let; Absence Ig M a přítomnost Ig G v titrech nad 1:1000 svědčí o přítomnosti infekce v minulosti. Diagnóza akutní T. u těhotné ženy je založena na výskytu specifického Ig G v krvi (sérokonverze) nebo zvýšení jeho titru po 3 a více týdnech.
5. Stanovení DNA patogenu: PCR v plodové vodě je přesná a rychlá metoda pro diagnostiku infekce plodu,
6. Nespecifické testy (u novorozence): leukocytóza, ultrazvuk, jaterní enzymy. Ultrazvuk: expanze mozkových komor, zvýšená echogenita mozkové tkáně, jater, ztluštění a zvýšená echogenita placenty, hepatomegalie, ascites, perikardiální a pleurální výpotek.
Prevence. Spočívá v podpoře opatření osobní hygieny, která má bohužel malý účinek. Pro těhotné:
- nejezte syrové maso
- po dotyku s kočkou si umyjte ruce
- nesbírat kočičí výkaly
- chov koček doma (infekce od myší)
- nekrmte svou kočku syrovým masem
- nedotýkejte se toulavých koček a nepouštějte je do domu
Proveditelnost rutinního screeningu T. je sporná: S nízkým výskytem je to velmi drahé.
Management a léčba. Pokud je matka nemocná T. v prvním trimestru, je nutné diagnostikovat T. u plodu a v případě pozitivního výsledku nabídnout ukončení těhotenství. U T. nemoci v pozdějších fázích těhotenství je možná léčba: sulfadiazin s trimethoprimem (toxický pro kostní dřeň), kyselina listová. Předepsání spiramycinu nevylučuje infekci plodu. Při léčbě akutní T. se 77 % dětí rodí bez známek onemocnění a klinický obraz onemocnění se projevuje u 5 % novorozenců. Při absenci léčby jsou tato čísla 39 % a 14 %. A přesto zůstává léčba matky kontroverzní: neúplná účinnost, teratogenita některých léků (pyrimethamin). Ale léčba novorozenců s potvrzenou T. je povinná: pyrimethamin, sulfadiazin, kyselina listová, případně spiramycin. Léčba a pozorování pokračují po dobu jednoho roku. Bez léčby byly léze oka a centrálního nervového systému pozorovány u 40 % infikovaných novorozenců s léčbou, pouze u 2 %.
| Toxoplazmóza | Zarděnky | Cytomegalovirus | Herpes simplex virus | |
| Způsob přenosu | Kočičí výkaly, syrové kozí mléko a maso, | Kapka ve vzduchu | Tělesná tajemství | |
| 10-40% | 85-90% | 50-80% | 50% | |
| Léčba těhotných žen | Pyrimethamin, sulfadiazin | Ne | ganciklovir | Acyclovir |
| Potřeba screeningu | Ne | Ano | Ne | Ne |
| Doživotní imunita | Doživotní imunita | Celoživotní nosič | Celoživotní nosič | |
| Ano (pro primární infekci) | Ano (pro primární infekci) | Ano | Ano (pro primární infekci) | |
| Ne | Ne | Zřídka | Ano | |
| Způsob doručení | Vaginální | Vaginální | Vaginální | císařský řez (vyrážka na genitáliích) |
| Ne | Ano (aktivní) | Ne | Ne |
| Syfilis | Žloutenka typu B | HIV | Streptokoky skupiny B | |
| Způsob přenosu | Kontakt se sliznicemi a kůží | Tělesná tajemství | Tělesná tajemství | Sexuálně, orálně-fekálně |
| Séropozitivita v běžné populaci | — | 1 % chronických nosičů | 0,1%(?) | 35% kolonizace genitálního traktu |
| Léčba těhotných žen | Benzathin penicilin (retarpen, extensilin) | Specifický imunoglobulin | Zidovudin (azido-thymidin) | penicilin |
| Potřeba screeningu | Ano | Ano | Ano | Ne |
| Stav po nemoci | Celoživotní nosič (neléčený) | Celoživotní imunita (pokud je nositelem) | Celoživotní infekční proces | Celoživotní kolonizace |
| Riziko transplacentárního přenosu (předporodní) | Ano | Zřídka | Ano | Zřídka |
| Riziko infekce plodu během porodu | Ne | Ano | Ano | Ano |
| Způsob doručení | Vaginální | Vaginální | Vaginální | Vaginální |
| Potřeba imunizace matky a novorozence | Ne | Ano (aktivní a pasivní) | Ne | Ne |
Literatura.
- Porodnictví. Ed. K. Niswander, A. Evans (přeloženo do angličtiny - 1999).
- Davis P.A., Gotefors L.A. Bakteriální infekce plodu a novorozence (překlad anglicky).-M., 1987.
- Klinická patologie těhotenství a novorozence. Ed. M. N. Kochi, G. L. Gilbert, J. B. Brown (přeloženo do angličtiny - M., 1986).
- Neznámá epidemie: herpes. Ed. L. N. Chachalina.-Smolensk, 1997
- Reprodukční zdraví. Ed. L. G. Klein, G. S. Berger, D. A. Edelman (přel. angličtina - 1988).
- Komplikace těhotenství: lékařské, chirurgické, gynekologické, psychosociální a perinatální l. -4. vydání.-Vyd. od Sh. H. Cherry, I. R. Merkatz.-1991.
- Sweet R. L., Gibbs R. S. Infekční onemocnění ženského genitálního traktu .-3. vydání.-1995.
(Návštíveno 116krát, dnes 1 návštěv)
Perinatální infekce (PI) jsou infekce přenosné z matky na plod s následným možným provedením nitroděložní infekce při nepříznivém průběhu a konci těhotenství, patologii plodu a novorozence. PI je jednou z hlavních příčin perinatální morbidity a dětské úmrtnosti. Incidence časné novorozenecké morbidity a mortality v důsledku intrauterinní infekce kolísá od 5,3 do 27,4 % a míra mrtvorozenosti dosahuje 16,8 %. Vrozená infekční patologie je přímou příčinou perinatální mortality v 36-39 % případů.
Je nutné rozlišovat mezi pojmy „nitroděložní infekce“ a „nitroděložní infekce“.
Termínem „nitroděložní infekce“ se rozumí nitroděložní infekce, konkrétně pronikání infekčních agens do plodu, ale absence známek infekčního onemocnění plodu. Intrauterinní infekce je proces šíření infekčních agens v těle plodu způsobující morfofunkční poruchy v různých orgánech a systémech, které jsou tomuto infekčnímu onemocnění vlastní, vyskytující se ante- nebo intranatálně a projevující se perinatálně nebo po narození dítěte.
Infekce matky neznamená infekci embrya, plodu a onemocnění novorozence, protože frekvence intrauterinní infekce je asi 10% všech těhotenství a frekvence klinicky výrazných forem intrauterinních infekcí je 0,5-1% včas porodů a 3,5-16 % u předčasných porodů.
Rizikové faktory pro intrauterinní infekci.
Ženy s následujícími rizikovými faktory by měly být považovány za vysoké riziko intrauterinní infekce: věk těhotné ženy a jejího manžela (partnera) je 35 let nebo více, přítomnost škodlivých faktorů a návyků z povolání;
genetická predispozice k nemocem;
údaje o somatické anamnéze (přítomnost chronických zánětlivých procesů močového, dýchacího systému a dalších extragenitálních onemocnění);
časný nástup sexuální aktivity, častá změna sexuálních partnerů;
anamnéza zánětlivých onemocnění dělohy, děložních přívěsků, kolpitidy;
dlouhodobá nitroděložní antikoncepce;
opakované umělé ukončení těhotenství;
umělé ukončení těhotenství s komplikovaným obdobím po potratu;
spontánní ukončení těhotenství v různých časech, těhotenství bez progrese;
malformace a prenatální smrt plodu;
komplikovaný průběh poporodního období u předchozích porodů;
placentární insuficience, chronický distres a/nebo syndrom omezení růstu plodu (FGR)
předčasné prasknutí plodové vody, anomálie porodu a odloučení placenty, těžká traumata měkkých tkání porodních cest;
kolpitida a bakteriální vaginóza diagnostikovaná během těhotenství;
chirurgická korekce isthmicko-cervikální insuficience během skutečného těhotenství;
polyhydramnion, oligohydramnion nebo placentární insuficience (PI).
Všímají si také onemocnění novorozence (vezikulóza, zánět spojivek, zápal plic, syndrom respirační tísně, zánětlivá onemocnění mozku, malnutrice, pustomegalie a hepatosplenomegalie, sepse aj.), přítomnost v rodině dětí se zdravotním postižením od r. dětství, s dětskou mozkovou obrnou (dětská mozková obrna) nebo jinými onemocněními centrálního nervového systému různé závažnosti, s vývojovým opožděním.
Klasifikace
V závislosti na cestě vstupu infekčního agens do těla matky a poté do embrya a/nebo plodu se rozlišují následující perinatální infekce: vzestupně;
hematogenní (transplacentární cesta);
transcidální (transmurální dráha);
Sestupně (přes vejcovody);
infekce přenášené mateřským mlékem;
infekce přenášené krví a jejími složkami;
nemocniční infekce;
smíšené (dvě nebo více cest infekce);
Iatrogenní infekce.
V závislosti na patogenu: bakteriální, virové, spirochetální, protozoální, smíšené.
Patogeneze
Patogeneze IUI je různorodá a závisí na typu patogenu, jeho interakci s embryem (plodem) a také na gestačním věku. Jsou možné následující následky infekce plodu: vrozená patologie, prenatální úmrtí plodu, předčasný porod, infekce plodu během porodu atd. Klinika
Klinické projevy a závažnost perinatálních infekcí závisí na: typ patogenu, jeho virulenci, specifičnost účinku, masivnost kontaminace a také to, zda je infekce primární nebo chronická;
imunitní homeostáza ženského těla;
stadia infekčního procesu u těhotné ženy;
období těhotenství, ve kterém došlo k infekci;
cesty vstupu patogenu do těla těhotné ženy.
Klinické příznaky PI by měly být považovány za obecné známky jejich manifestace u matky a plodu.
Obecné známky IUI u matky Spolu s akutní formou existují vymazané, latentní formy onemocnění nebo asymptomatická onemocnění.
Klinické projevy nemusí vždy záviset na typu patogenu, jeho virulenci nebo úrovni imunologické reaktivity organismu.
K infekci plodu a novorozence může dojít v důsledku akutní infekce matky nebo v důsledku aktivace chronické, přetrvávající infekce během těhotenství.
Aktivace perzistující infekce je možná při jakémkoliv narušení homeostázy v těle těhotné ženy (hypotermie, stres, respirační infekce).
Předchozí infekce nezanechávají trvalou imunitu, takže jsou pozorovány reinfekce a relapsy.
Pohlavně přenosné choroby výrazně zvyšují riziko infekce HIV, hepatitidy B a C a rakoviny děložního čípku.
Obecné známky IUI u plodu.
Podobnost projevů závisí na délce trvání infekce.
Algoritmus pro vyšetřování těhotných žen s vysokým rizikem infekce
Po posouzení rizikových faktorů nitroděložní infekce se tvoří skupiny těhotných s vysokým infekčním rizikem, které jsou podrobeny vyšetření. Klinické a laboratorní vyšetření
Klinické a laboratorní vyšetření těhotných žen s vysokým infekčním rizikem se skládá ze standardních, specifických a doplňkových výzkumných metod.
Standardní výzkumné metody
V případě nekomplikovaného těhotenství do 28 týdnů se vyšetření provádí jednou měsíčně, od 28. do 36. týdne - jednou za 2 týdny a po 36. týdnu - týdně (v přítomnosti viru a / nebo bakteriální infekce, pozorování Těhotné ženy jsou sledovány častěji, dle indikací). Pravidelně se zjišťuje tělesná hmotnost těhotné ženy, její poloha, výška děložního fundu, obvod břicha, měří se puls a krevní tlak. Po 18-20 týdnech těhotenství je stanovena pohyblivost plodu.
Stanovení krevní skupiny, Rh faktoru a titru protilátek, sérologické testy na R/L/, HB5 a NSL antigeny, moč a krevní testy, biochemické, reologické krevní testy těhotných žen, mikroskopie vaginálních stěrů, kolpocytogram, kultivace z nosu, hltanu a cervikálního kanálu do flóry. Testování krve těhotné ženy na titr protilátek proti fosfolipidům, protože u této skupiny pacientů může být antifosfolipidový syndrom přímou příčinou spontánních potratů a opakovaných potratů.
Ultrazvuk s placentometrií a biometrií embrya a plodu musí být proveden na konci prvního trimestru, ve druhém trimestru - v 16-22 týdnech těhotenství a ve třetím trimestru - ve 33 a 36-38 týdnech těhotenství.
Dopplerovské ultrazvukové vyšetření systému matka-placenta-plod od 19.-20. týdne těhotenství (pokud je feto- a uteroplacentární oběh normální, opakujte každé 3-4 týdny, u hemodynamických poruch - během léčby a bezprostředně po ní).
Od 32-33 týdne těhotenství je předepsáno CTG plodu a stanoven jeho biofyzikální profil. CTG se musí opakovat v průběhu času po léčbě chronického fetálního postižení a před porodem.
Specifické laboratorní vyšetřovací metody. Používají bakterioskopické, bakteriologické, virologické, cytologické, sérologické a molekulárně biologické metody (ligázová řetězová reakce, polymerázová řetězová reakce).
Další výzkumné metody. Mezi další výzkumné metody patří biopsie trofoblastu a choria, kordocentéza, amniocyntéza, lékařské genetické poradenství atd.
Takové biologické materiály by měly být zkoumány.
Vyšetření obsahu cervikálního kanálu, pochvy, močové trubice:
bakterioskopické;
bakteriologické (kvalitativní a kvantitativní) v přítomnosti bakteriourie;
virologické.
Vyšetření moči:
bakterioskopické;
bakteriologické (kvalitativní a kvantitativní)
virologické;
biochemické (stanovení dusitanů).
Vyšetření moči je zaměřeno na identifikaci asymptomatické bakteriurie nebo potvrzení diagnózy manifestních forem infekce močových cest (uretritida, cystitida, pyelonefritida).
Asymptomatická bakteriurie - přítomnost mikrobiálních patogenů v 1 ml průměrné moči v množství > 105 (100 000) kolonií Formační jednotky (CFU) při absenci jakýchkoli klinických projevů. Leukocyturie je také možná (není nutná).
Krevní test na přítomnost specifických protilátek. Nejčastěji se k vyšetření krve používají sérologické metody. Enzymově vázaný imunosorbentní test (ELISA) tedy určuje přítomnost specifických IgM a IgG protilátek. Senzitivita - 99 %, specificita - 95 %. To je nezbytné pro včasnou detekci protilátek IgM nebo zvýšení celkové koncentrace IgM a IgG.
Pro zvýšení spolehlivosti výsledků musí být reakce v jednom vzorku materiálu provedena se dvěma typy antisér (IgIg třída M a G).
S přihlédnutím k možné nadměrné diagnóze je nutné infekci ověřit minimálně dvěma metodami (ELISA a PCR). Nejpřesnější informace o přítomnosti intrauterinní infekce a stavu intrauterinní „pacientky“ během těhotenství od 16-18 do 32 týdnů lze získat v moderních porodnických nemocnicích pomocí bakteriálních a/nebo virologických studií plodové vody (získané transabdominální amniocentézou ) a fetální krev (kordocentézou). Hladina a-FP se zjišťuje i v plodové vodě (odchylky od normy počínaje 17.-18. týdnem gestace svědčí o vysokém riziku perinatální patologie).
Indikace k vyšetření k identifikaci PI.
Indikace k vyšetření k identifikaci patogenů kapavky, chlamydií, trichomoniázy, kandidózy, bakteriální vaginózy je přítomnost klinických příznaků vaginitidy.
Indikace pro vyšetření k detekci herpes viru jsou přítomnost charakteristických vyrážek.
Indikace pro screening zarděnek: kontakt s pacientem se zarděnkami při absenci imunity vůči zarděnkám u těhotné ženy;
podezření nebo přítomnost příznaků onemocnění (vyrážka).
Indikace pro vyšetření k detekci streptokoka B zahrnují následující situace:
bezvodá doba delší než 18 hodin;
horečka během porodu (více než 38o);
infekce starších dětí streptokoky skupiny B;
bakteriurie se streptokokem skupiny B.
Taktika lékaře během těhotenství
Následující doporučené přístupy k vyšetření těhotných žen, léčbě a následkům některých perinatálních infekcí Perinatální infekce jsou infekce způsobené bakteriemi nebo viry, které se mohou přenášet z matky na dítě během těhotenství nebo porodu. Mezi perinatální infekce patří bakteriální nebo virová onemocnění a v některých případech mohou způsobit komplikace během porodu. Některé perinatální infekce se přenášejí sexuálně.
K přenosu mnoha perinatálních infekcí dochází během porodu, zejména při použití invazivních technik, jako je epiziotomie nebo umělé protržení membrány. V jiných případech může k přenosu dojít během těhotenství, pokud infekční agens překročí placentární bariéru, může k němu dojít také během kojení, pokud je patogen v mateřském mléce.
Četnost perinatálních infekcí závisí na typu patogenu. Například perinatální přenos CMV se vyskytuje ve 2-24 případech z každých 1000 živě narozených dětí. Přenos genitálního herpesu během těhotenství se odhaduje na jedno až dvě z každých 2 000 těhotenství; přenos skupiny beta-streptococcus způsobuje neonatální infekci u jednoho až pěti z každých 1000 živě narozených dětí a zarděnky - 0,02 na každých 1000 dětí. HIV se přenáší z matky na dítě ve 25–40 procentech případů.
Typy perinatálních infekcí
Níže jsou uvedeny některé z nejčastějších infekcí, které mohou být přenášeny perinatálně.
Chlamydie
Chlamydie jsou nejčastější bakteriální pohlavně přenosné onemocnění. Většina žen s chlamydiovou infekcí nemá žádné zjevné příznaky. Infekce postihuje reprodukční trakt a způsobuje zánětlivé onemocnění pánve, neplodnost a mimoděložní těhotenství. Tato infekce může způsobit předčasné protržení membrány a předčasný porod. Chlamydie se mohou přenést na dítě během porodu a mohou vést k novorozenecké blenorrhee (oční infekci) během prvního měsíce života a zápalu plic během jednoho až tří měsíců. Mezi příznaky chlamydiové pneumonie patří kašel a zrychlené dýchání. Dušnost a horečka jsou vzácné.
Cytomegalie
 Cytomegalovirus (CMV) je běžný virus z rodiny herpes. Nachází se ve slinách, moči a dalších tělesných tekutinách a může se přenášet pohlavním stykem nebo jinými formami fyzického kontaktu. U dospělých může CMV způsobit mírné příznaky zduření lymfatických uzlin, horečku a únavu. Mnoho lidí, kteří jsou nositeli tohoto viru, nepociťuje vůbec žádné příznaky. Dítě se může nakazit CMV, pokud matka onemocní nebo se u něj během těhotenství znovu objeví. CMV narušuje normální vývoj plodu a může vést k mentální retardaci, slepotě, hluchotě nebo epilepsii.
Cytomegalovirus (CMV) je běžný virus z rodiny herpes. Nachází se ve slinách, moči a dalších tělesných tekutinách a může se přenášet pohlavním stykem nebo jinými formami fyzického kontaktu. U dospělých může CMV způsobit mírné příznaky zduření lymfatických uzlin, horečku a únavu. Mnoho lidí, kteří jsou nositeli tohoto viru, nepociťuje vůbec žádné příznaky. Dítě se může nakazit CMV, pokud matka onemocní nebo se u něj během těhotenství znovu objeví. CMV narušuje normální vývoj plodu a může vést k mentální retardaci, slepotě, hluchotě nebo epilepsii.
Genitální opar
Genitální herpes, obvykle způsobený virem herpes simplex typu 2 (HSV-2), je pohlavně přenosné onemocnění, které způsobuje bolestivé vředy na genitáliích. Ženy, u kterých se genitální herpes poprvé objeví během těhotenství, mají vysoké riziko potratu nebo nízké porodní hmotnosti dítěte. Infekce se může přenést z matky na dítě během porodu, pokud má matka aktivní onemocnění. Nejzávažnějším rizikem pro dítě je možnost vzniku encefalitidy se zánětem mozku, příznaky podrážděnosti a špatné chuti k jídlu.
Žloutenka typu B
Hepatitida B je infekční virus, který způsobuje poškození jater a je hlavní příčinou chronického onemocnění jater a cirhózy. Dítě je vystaveno vysokému riziku rozvoje infekce hepatitidou při kontaktu s krví infikované matky během porodu.
Virus lidské imunodeficience (HIV)
Přihlaste se k odběru našeho kanál YouTube !
HIV je závažný, nakažlivý virus, který způsobuje syndrom získané imunodeficience (AIDS). Asi 25-40 procent těhotných žen s HIV přenáší infekci na své novorozence. Příznaky infekce HIV u malých dětí zahrnují známky opožděného vývoje, chronickou drozd a průjem.
Lidsky papillomavirus
 Lidský papilomavirus (HPV), pohlavně přenosné onemocnění, které způsobuje genitální bradavice a může zvýšit riziko vzniku určitých typů rakoviny. HPV se může přenášet z matky na dítě během porodu a může způsobit zúžení průdušnice.
Lidský papilomavirus (HPV), pohlavně přenosné onemocnění, které způsobuje genitální bradavice a může zvýšit riziko vzniku určitých typů rakoviny. HPV se může přenášet z matky na dítě během porodu a může způsobit zúžení průdušnice.
Rubella (německé spalničky)
Rubella je virus, který způsobuje vyrážku, horečku a příznaky infekce horních cest dýchacích. Většina lidí je vystavena zarděnkám jako děti a vytvoří si protilátky proti viru. Rubeola během raného těhotenství může procházet placentou a způsobit vážné vrozené vady, včetně srdečních abnormalit, mentální retardace, slepoty a hluchoty.
Skupina beta streptokoků
Skupinový beta streptokok (GBS) je nejčastější bakteriální příčinou úmrtí novorozenců v důsledku infekcí, ačkoli výskyt se s příchodem antibiotik poněkud snížil. U žen může GBS způsobit vaginitidu a infekce močových cest. Obě infekce mohou způsobit předčasný porod a bakterie se mohou přenést na dítě v děloze nebo během porodu. GBS způsobuje u kojenců zápal plic, meningitidu a další závažné infekce.
Syfilis
Syfilis je pohlavně přenosné onemocnění, které se před narozením může přenášet z matky na dítě placentou. Až 50 procent dětí narozených matkám se syfilidou se narodí předčasně nebo mrtvě nebo zemře brzy po narození. Infikované děti mohou mít vážné vrozené vady. Děti, které přežijí dětství, mohou mít příznaky syfilis až o dva roky později.
Odmítnutí odpovědnosti: Informace uvedené v tomto článku o perinatálních infekcích jsou určeny pouze pro informování čtenáře. Není zamýšlen jako náhrada za radu od zdravotnického pracovníka.