Phasendiagramm des Al-Mg-Systems. Begründung der Materialwahl, seine wesentlichen Eigenschaften Zustandsdiagramm al mg
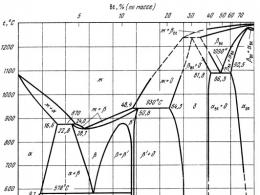
Das Phasendiagramm von Kupfer-Aluminium wurde über den gesamten Konzentrationsbereich mithilfe thermischer, metallographischer und röntgenographischer Analysemethoden erstellt und ist ein komplexes Diagramm mit Zwischenphasen. Das Zustandsdiagramm von Kupfer - Aluminium (Abb. 1) basiert auf Arbeiten verschiedener Autoren über einen längeren Zeitraum. Der Bereich kupferbasierter fester Lösungen (α-Phase) reicht bis zu 9 Masse-% Al. Mit sinkender Temperatur nimmt die Löslichkeit von Aluminium in Kupfer bei Temperaturen von 1037 zu; 900; 800; 700; 500 °C ist 7,4; 7,8; 8,2; 8,8; 9,4 Masse-% Al. Phase a weist ein fcc-Gitter auf, ähnlich dem Gitter von reinem Kupfer, dessen Periode mit zunehmendem Aluminiumgehalt zunimmt und in der Legierung mit 10,5 Masse-% Al 0,3657 nm beträgt.
Phase β ist eine feste Lösung auf Basis der Cu 3 Al-Verbindung. In Legierungen im β-Bereich können je nach Wärmebehandlung und Abkühlungsbedingungen zwei metastabile Zwischenphasen beobachtet werden: β" und β.
Phase γ 1 – eine feste Lösung auf Basis der Verbindung Cu 3 Al 4 liegt im Konzentrationsbereich von 16,0...18,8 % (Masse) Al vor und weist ein monoklines Gitter mit 102 Atomen in der Elementarzelle auf. Die α 2 -Phase hat ein ähnliches Gitter wie die α-Phase.
Im Bereich von bis zu 20 Masse-% Al besteht der Liquidus von Legierungen aus vier Zweigen der Primärkristallisation der Phasen α, β, χ und χ 1. Bei 1037 °C kristallisiert das Eutektikum α + β mit einem Eutektikumspunkt bei 8,5 Masse-% Al. Bei Temperaturen von 1036 und 1022 °C kommt es zu peritektischen Reaktionen Zh + β ↔χ und Zh + χ↔γ 1. jeweils. Die χ-Phase existiert im Temperaturbereich 1036...936 °C. Phase β kristallisiert aus der Schmelze entlang einer Kurve mit einem Maximum bei einer Temperatur von 1048 °C und entspricht einer Konzentration von 12,4 Masse-% Al. Im festen Zustand weist dieser Bereich eine Reihe eutektoider und peritektoider Transformationen auf. Bei 963 °C zerfällt die χ-Phase in die β- und γ 1 -Phase. Der eutektoide Punkt entspricht 15,4 Masse-% Al. Bei 780 °C zerfällt die γ 1 -Phase gemäß einer eutektoiden Reaktion in β- und γ 2-Phasen. Bei 873 °C entsteht durch eine peritektonische Reaktion die γ-Phase. Es wird davon ausgegangen, dass in der γ 2 -Phase eine Phasenumwandlung im Temperaturbereich 400...700 °C mit einem Aluminiumgehalt am Eutektoidpunkt von 11,8...11,9 % (Massenprozent) stattfindet. Im Konzentrationsbereich von 9...16 % (bezogen auf die Masse) Al wird die Existenz einer weiteren stabilen Phase angenommen – χ oder α 2, die durch die eutektoide Reaktion bei 363 °C gebildet wird und deren Aluminiumgehalt am eutektoiden Punkt ∼ beträgt 11,2 % (bezogen auf die Masse). Die Konzentrationsgrenzen des Homogenitätsbereichs dieser Phase wurden nicht ermittelt.
Die Autoren berechneten auf der Grundlage von Literaturdaten zu den thermodynamischen Eigenschaften von Komponenten und Zwischenphasen sowie auf der Grundlage experimenteller Daten zu Phasengleichgewichten das Phasendiagramm des Cu-Al-Systems. Die Werte der berechneten Temperaturen der Phasenumwandlungen stimmen praktisch mit den Daten der Arbeit überein.
Kupfer - Beryllium
Das Phasendiagramm von Kupfer-Beryllium wurde von vielen Forschern untersucht. Es ist über den gesamten Konzentrationsbereich aufgebaut (Abb. 2). Die Kristallisationskurven der Legierungen bestehen aus vier Zweigen, die der Kristallisation der Phasen α, β, δ und β-Be entsprechen. Die β-Phase kristallisiert entlang einer Kurve mit einem Minimum bei einer Temperatur von 860 °C und 5,3 Gew.-% Be. Bei 870 °C entsteht die β-Phase durch eine peritektische Reaktion und bei 578 °C zerfällt die β-Phase durch eine eutektische Reaktion. Es gibt Hinweise auf eine höhere eutektoide Umwandlungstemperatur – 605 °C.

Die Löslichkeit von Beryllium in Kupfer bei der Eutektoid-Umwandlungstemperatur beträgt 1,4 % (nach Gewicht). Mit sinkender Temperatur nimmt die Löslichkeit von Beryllium ab und beträgt: bei 500 °C – 1,0 % (Gewicht), bei 400 °C – 0,4 % (Gewicht), bei 300 °C – 0,2 % (Gewicht). Im Konzentrationsbereich von 50,8...64,3 % (at.) Be findet bei 930 °C eine peritektische Reaktion der Bildung der β"-Phase und bei 1090 °C die eutektische Umwandlung β ↔α-Be +δ statt findet statt. Phasengrenzbereiche δ/δ + α-Be und δ + α-Be/α-Be durchlaufen 81,5 und 92,5 % (at.) Be bei 1000 °C, bei 900 °C - 81,0 und 93,0 % (at.) .) Be, bei 700 °C - 80,8 bzw. 95,5 % (at.) Be.
Phase δ entsteht durch eine peritektische Reaktion bei einer Temperatur von 1239 °C. Die kupferbasierte feste Lösung (α-Phase) hat ein fcc-Gitter mit einer Periode α = 0,3638 nm bei 2,1 % (bezogen auf die Masse) Be, die δ-Phase hat ein ungeordnetes bcc-Gitter mit einer Periode α = 0,279 nm bei 7,2 % (nach Masse) Be, die β′-Phase hat ein geordnetes kubisch raumzentriertes Gitter vom Typ CsCl mit einer Periode α = 0,269...0,270 nm, die δ-Phase hat ein kubisches Gitter vom Typ MgCu 2 mit a Periode α = 0,5952 nm. Die β-Be-Phase ist eine Hochtemperaturphase und die α-Be-Phase ist eine Niedertemperaturmodifikation einer festen Lösung auf Berylliumbasis.
Den Daten zufolge, die einen Teil des Diagramms bis zu 50 % (at.) Cu zeigen, schmilzt die δ-Phase (Be 4 Cu-Be 2 Cu) kongruent bei 1219 °C und 22 % (at.) Cu. Die β-Phase weist eine Struktur vom Typ MgCu 2 auf und ändert den Gitterparameter im Homogenitätsbereich von α = 5957 nm auf α = 0,5977 nm bei 25 Atom-% Cu.
Kupfer - Eisen
Das Kupfer-Eisen-Phasendiagramm wurde von vielen Forschern untersucht. Die Ergebnisse dieser Studien werden in den Arbeiten ausführlich analysiert. Die wesentlichen Widersprüche betreffen die Frage der vollständigen oder teilweisen Mischbarkeit von Kupfer und Eisen im flüssigen Zustand. Als Ergebnis von Experimenten wurde festgestellt, dass im Kupfer-Eisen-System keine Schichtung vorliegt, im unterkühlten Zustand (100 °C) jedoch eine Schichtung auftritt. Der Trennbereich ist nahezu symmetrisch zur Achse, die der äquiatomaren Zusammensetzung entspricht, und die kritische Mischtemperatur liegt 20 °C unter der Liquidustemperatur bei äquiatomarer Zusammensetzung.
In Abb. Abbildung 3 zeigt ein Diagramm des Kupfer-Eisen-Zustands gemäß den Daten. Bei Temperaturen von 1480 wurden zwei peritektische und eine eutektoide Umwandlung festgestellt; 1094 und 850 °C. Löslichkeit von Eisen in Kupfer bei 1025; 900; 800 und 700 °C beträgt 2,5; 1,5; 0,9; jeweils 0,5 Masse-% Fe. Der Gitterparameter der kupferbasierten Mischkristalllegierung für die Legierung mit 2,39 Atom-% Fe beträgt 0,3609 nm. Der Gitterparameter von α-Fe (bcc) erhöht sich durch Zugabe von 0,38 Atom-% Cu von 0,28662 ± 0,00002 auf 0,28682 nm.

Kupfer - Kobalt
Das Zustandsdiagramm des Kupfer-Kobalt-Systems ist in Abb. dargestellt. 4 . Es stimmt gut mit den Ergebnissen früherer Studien zu diesem Diagramm überein. In diesem System entsteht infolge einer Unterkühlung um 100 °C oder mehr ein Bereich der Unmischbarkeit im flüssigen Zustand, der nahezu symmetrisch um die Achse ist, die der äquiatomaren Zusammensetzung entspricht. Bei dieser Zusammensetzung liegt die kritische Mischtemperatur 90 °C unterhalb der Liquiduskurve.

Das Cu-Co-System ist vom peritektischen Typ. Die Temperatur der peritektischen Reaktion beträgt 1112 °C. Daten zur Löslichkeit von Kobalt in einer festen Lösung auf Basis von Kupfer (β) und Kupfer in einer festen Lösung auf Basis von Kobalt (a) im Temperaturbereich 900...1100 °C sind in der Tabelle aufgeführt. 1.

Kupfer - Silizium
Das Zustandsdiagramm von Kupfer-Silizium ist in Abb. dargestellt. 5 (basierend auf der Gesamtheit der Werke). Das System enthält eine α-Mischkristalllösung auf Basis von Kupfer, β-, δ-, η-Phasen sowie K-, γ- und ε-Phasen, die durch peritektoide Reaktionen gebildet werden.

Der Existenzbereich der β-Phase [bcc-Gitter mit α = 0,2854 nm bei 14,9 Atom-% Si] liegt im Temperaturbereich 852...785 °C; Es entsteht durch eine peritektische Reaktion mit einem peritektischen Umwandlungspunkt von 6,8 Masse-% Si. Der Existenzbereich der β-Phase umfasst den Temperaturbereich 824...710 °C und entsteht durch eine peritektische Reaktion; peritektischer Transformationspunkt 8,65 % (Masse) Si. Phase η hat zwei Modifikationen: η′ und η″. Im Temperaturbereich 620...558 °C findet die Umwandlung η↔η′ statt, im Bereich 570...467 °C findet die Umwandlung η′↔η″ statt. Das η-Phasengitter ähnelt dem γ-Messinggitter.
Phase K entsteht durch eine peritektoide Reaktion bei +842 °C und existiert bis zu 552 °C, der peritektoide Punkt entspricht 5,9 Masse-% Si. Die K-Phase hat ein dicht gepacktes hexagonales Gitter mit α = 0,25543 nm und c = 0,41762 nm bei 11,8 Atom-% Si und α = 0,25563 nm und c = 0,41741 nm bei 14,6 Atom-% Si. Phase γ entsteht durch eine peritektoide Reaktion bei 729 °C und ist bis Raumtemperatur stabil; der peritektoide Punkt entspricht 8,35 Masse-% Si.
Die γ-Phase weist ein kubisches Gitter vom β-Mn-Gittertyp mit einer Periode α = 0,621 nm auf.
Die ε-Phase wird ebenfalls durch eine peritektoide Reaktion bei 800 °C gebildet und liegt in einem engen Konzentrationsbereich von 10,6...10,7 % (Masse) Si vor, stabil bis Raumtemperatur. Es hat ein bcc-Gitter mit α = 0,9694 nm. Die Löslichkeit von Kupfer in Silizium ist vernachlässigbar und beträgt 2,810 -3; 2·10 -3; 5,5·10 -4; 8,5·10 -5; 5,3·10 -6 % (at.) bei Temperaturen 1300; 1200; 1000; 800 bzw. 500 °C. Die Löslichkeit von Silizium in Kupfer ist signifikant und beträgt ∼5,3 Gew.-% bei 842 °C.
Kupfer - Mangan
Das Zustandsdiagramm des Kupfer-Mangan-Systems wird über den gesamten Konzentrationsbereich erstellt. Hier ist es entsprechend den Daten angegeben (Abb. 6). Kupfer und Mangan bilden ein Minimum auf der Liquiduskurve bei einem Gehalt von ∼37 % (at.) Mn und einer Temperatur von 870 ± 5 °C. Umwandlungen im Festkörper sind mit Ordnungsprozessen in Legierungen seitens des Kupfers und allotropen Modifikationen des Mangans verbunden. Die feste Lösung (α-Cu, γ-Mn) liegt bei ∼16 Atom-% Mn (MnCu 5) und 400 °C und bei ∼25 Atom-% Mn (MnCu 3) und 450 °C.

Die Löslichkeit von Kupfer in den Phasen α-Mn und β-Mn ist unbedeutend. Das System durchläuft einen kontinuierlichen Übergang von einem flächenzentrierten kubischen Gitter einer kupferbasierten festen Lösung (α-Cu) zu einem flächenzentrierten tetragonalen Gitter von γ-Mn.
Kupfer - Nickel
Das Zustandsdiagramm des Kupfer-Nickel-Systems ist ein System mit einer kontinuierlichen Reihe fester Lösungen. Abbildung 7 zeigt die Ergebnisse experimenteller Studien, die gut miteinander übereinstimmen. Im festen Zustand finden Umwandlungen statt, die mit magnetischen Umwandlungen in Nickel verbunden sind. Alle Legierungen des Cu-Ni-Systems haben ein fcc-Gitter. Annahmen über die Existenz von CuNi- und CuNi 3 -Verbindungen im System wurden in späteren Arbeiten nicht bestätigt. Legierungen dieses Systems bilden die Grundlage für Industrielegierungen vom Typ Kupfernickel.

Kupfer - Zinn
In Abb. Abbildung 8 zeigt ein Zustandsdiagramm basierend auf einer Vielzahl von Arbeiten. Das System hat die Existenz einer Reihe von Phasen nachgewiesen, die sowohl während der Primärkristallisation als auch während der Umwandlung in den festen Zustand gebildet werden. Die Phasen α, β, γ, ε, η entstehen bei der Primärkristallisation, die Phasen ζ und δ – im festen Zustand. Die Phasen β, γ und η entstehen durch peritektische Reaktionen bei Temperaturen von 798, 755 und 415 °C. Die Gitterperiode der α-Phase erhöht sich von 0,3672 auf 0,3707 nm. Die Phasen β und γ sind kristallographisch ähnlich und haben ein bcc-Gitter.

Die ε-Phase basiert auf der Cu 3 Sn-Verbindung und weist ein orthorhombisches Gitter auf. Die η-Phase entspricht der Cu 6 Sn 5-Verbindung. Die Temperatur liegt bei 189...186 °C. Phase ζ hat ein hexagonales Gitter mit der erwarteten Zusammensetzung Cu 20 Sn 6 . Die δ-Phase hat die Struktur von γ-Messing, ist eine elektronische Verbindung und entspricht der Formel Cu 31 Sn 8 bei 20,6 Atom-% Sn.
Die Löslichkeit von Zinn in Kupfer beträgt laut Röntgenspektralanalyse % (At.) Sn [% (Masse) – in Klammern]: 6,7 (11,9); 6,5 (11,4); 5,7 (10,10) bei Temperaturen 350; 250; 150 °C bzw. Die Löslichkeit von Kupfer in Zinn im festen Zustand bei der eutektischen Temperatur beträgt 0,01 % (at.) (nach Tokseitov et al.).
Kupfer - Blei
Das über den gesamten Konzentrationsbereich aufgebaute Zustandsdiagramm von Kupfer - Blei ist in Abb. dargestellt. 9 entsprechend der Arbeit. Das Zustandsdiagramm des Kupfer-Blei-Systems ist durch das Vorhandensein monotektischer und eutektischer Umwandlungen gekennzeichnet. Die Temperatur der monotektischen Umwandlung beträgt (955 ± 0,5) C und die Ausdehnung des Nichtmischbarkeitsbereichs bei dieser Temperatur beträgt 15,7–63,8 % (at.) Pb. Der eutektische Punkt entspricht 0,18 % (at.) Pb und den Daten zufolge einer Temperatur von 326 °C und 0,2 % (at.) Pb. Die Löslichkeitskurve zwischen der monotektischen Temperatur und dem Schmelzpunkt von Blei wurde sehr sorgfältig bestimmt. Es wurde festgestellt, dass diese Kurve die monotektische Horizontale bei einem Bleigehalt von 67 % (at.) schneidet. Die Löslichkeit von Blei in Kupfer im festen Zustand beträgt bei Temperaturen über 600 °C nicht mehr als 0,09 % (At.). Die Löslichkeit von Kupfer in Blei im festen Zustand beträgt weniger als 0,007 % (Gewichtsprozent).

Kupfer - Antimon
Das Zustandsdiagramm von Kupfer - Antimon wird gemäß den Daten in Abb. dargestellt. 10.

In den Legierungen dieses Systems wurde eine Hochtemperatur-β-Phase mit einem fcc-Gitter vom Typ BiF 3 entdeckt, die bei 684 °C kongruent schmilzt und die Legierung 28,6 Atom-% Sb enthält. Bei 435 °C zerfällt die β-Phase eutektoid in Phase k und Cu 2 Sb. Der eutektoide Punkt entspricht 24 % (at.) Sb. Maximale Löslichkeit der β-Phase 20...32%) (at.) Sb. Andere Zwischenphasen – η, ε, ε′ und k – werden durch peritektoide Reaktionen bei Temperaturen von 488 °C (η), 462 °C (e) gebildet. Die ε′-Phase hat ein hexagonales Gitter mit Perioden α = 0,992 nm, c = 0,432 nm und existiert im Temperaturbereich ∼375...260 °C. Die k-Phase hat eine orthorhombische Struktur vom Typ Cu 3 Ti, existiert im Bereich von 450 bis 375 °C und zerfällt bei einer Temperatur von 375 °C in die ε-Phase und Cu 2 Sb oder in die ε′-Phase und Cu 2 Sb (nach anderen Autoren). Phase η hat einen Homogenitätsbereich von 15,4 bis 15,8 % (at.) Sb bei 426 °C. Die Zwischenphase Cu 2 Sb entsteht durch eine peritektische Reaktion bei 586 °C und weist einen engen Homogenitätsbereich von 32,5...33,4 % (at.) Sb auf. Es hat ein tetragonales Gitter. Die maximale Löslichkeit von Antimon in Kupfer im festen Zustand bei Temperaturen von 600; 550:500; 450; 400; 360; 340 und 250 °C beträgt 5,79; 5,74; 5,69; 5,44; 4,61; 3,43; 3,02; 1,35 % (at.) oder 10,53; 10,44; 10,37; 9,92; 8,48; 6,38; 5,64; 2,56 % (bezogen auf die Masse).
Kupfer - Phosphor
Das Zustandsdiagramm des Kupfer-Phosphor-Systems ist gemäß den Daten in Abb. dargestellt. 11. Basierend auf den Ergebnissen späterer Arbeiten wurden zwei Verbindungen im System entdeckt: Cu 3 P und Cu P 2. Die Bildungstemperatur der Cu 3 P-Verbindung direkt aus der Schmelze wird von verschiedenen Autoren unterschiedlich angegeben: 1005; 1018 oder 1023; 1022 °C. Der Homogenitätsbereich der Cu 3 P-Verbindung beträgt 31 % (at.) P bei eutektischer Temperatur und 27,5 % (at.) P bei 700 °C. Die Cu 3 P-Verbindung hat ein hexagonales Gitter mit den Parametern α = 0,695 nm, c = 0,712 ± 0,02 nm, c/α = 1,02.

Die CuP 2 -Verbindung kristallisiert direkt aus der Schmelze bei 891 °C. Bei 714 °C findet eine eutektische Reaktion zwischen der Cu 3 P-Verbindung und Kupfer statt, der eutektische Punkt entspricht 15,72 % (at.) P.
Bei 833 °C herrscht ein eutektisches Gleichgewicht zwischen den Verbindungen Cu 3 P und Cu P 2 . Die Zusammensetzung des eutektischen Punktes beträgt 49 % (at.) R.
Im Bereich des Diagramms zwischen Phosphor und der CuP 2 -Verbindung wird die Existenz eines entarteten Eutektikums bei 590 °C angenommen.
Die Löslichkeit von Phosphor in Kupfer ist in der Tabelle angegeben. 2.

(Notiz. Der Phosphorgehalt ist in Klammern in Gewichtsprozent angegeben.)
Kupfer - Chrom
Das Kupfer-Chrom-Phasendiagramm wurde in der kupferreichen Region am gründlichsten untersucht. Es ist vollständig im Werk von G.M. wiedergegeben. Kuznetsova et al. basierend auf thermodynamischen Berechnungsdaten und Daten zu den Parametern der Wechselwirkung von Komponenten (Abb. 12). Die Struktur der Legierungen enthält zwei Phasen: feste Lösungen auf Basis von Kupfer (α) und Chrom (β). Bei 1074,8 °C findet eine eutektische Umwandlung bei einem Chromgehalt von 1,56 % (at.) statt. Die Löslichkeit von Chrom in Kupfer nach Angaben verschiedener Autoren ist in der Tabelle angegeben. 3.


Die Löslichkeit von Kupfer in Chrom im festen Zustand variiert zwischen 0,16 % (at.) bei 1300 °C und 0,085 % (at.) bei 1150 °C.
Kupfer - Zink
In Kupferlegierungen sind die Elemente der Gruppe II des Periodensystems von D.I. von größtem praktischem Interesse. Mendelejew steht für Zink. Das Kupfer-Zink-Phasendiagramm wurde von vielen Forschern über den gesamten Konzentrationsbereich untersucht. In Abb. Abbildung 13 zeigt ein Zustandsdiagramm, das aus einer Reihe von Arbeiten erstellt wurde, in denen Methoden der thermischen, röntgenologischen, metallographischen, elektronenmikroskopischen Analyse und Bestimmung der Liquidustemperatur verwendet wurden.
Die Liquiduslinie des Kupfer-Zink-Systems besteht aus sechs Primärkristallisationszweigen der Phasen α, β, γ, δ, ε und η. Es gibt fünf peritektische Transformationen im System, % (at.):
1) F (36,8 Zn) + α (31,9 Zn) ↔ β (36,1 Zn) bei 902 °C;
2) F (59,1 Zn) + β (56,5 Zn) ↔ γ (59,1 Zn) bei 834 °C;
3) F (79,55 Zn) + γ (69,2 Zn) ↔ δ (72,4 Zn) bei 700 °C;
4) F (88 Zn) + δ (76 Zn) ↔ ε (78 Zn) bei 597 °C;
5) F (98,37 Zn) + ε (87,5 Zn) ↔ η (97,3 Zn) bei 423 °C.
Die Löslichkeit von Zink in einer festen Lösung auf Kupferbasis steigt zunächst von 31,9 % (at.) bei 902 °C auf 38,3 % (at.) bei 454 °C, nimmt dann ab und beträgt 34,5 % (at.) bei 150 °C C und 29 % (at.) bei 0 °C.

Im Existenzbereich der α-Phase sind zwei Modifikationen α 1 und α 2 definiert. Der Existenzbereich der Phase β reicht von 36,1 % (at.) Zn bei 902 °C bis 56,5 % (at.) Zn bei 834 °C und von 44,8 % (at.) Zn bei 454 °C bis zu 48,2 % ( at.) Zn bei 468 °C. Im Temperaturbereich 454...468 °C kommt es zur Umwandlung bzw. Ordnung.
Die β′-Phase zersetzt sich gemäß der eutektoiden Reaktion β′↔α + γ bei einer Temperatur von ~255 °C. Die β-Phase existiert in vier Modifikationen: die γ''-Phase bis zu Temperaturen von 250...280 °C, oberhalb 280 °C ist die γ''-Phase stabil, die sich bei 550...650 °C in umwandelt die γ′-Phase; oberhalb von 700°C liegt eine γ-Phase vor. Die δ-Phase existiert im Bereich von 700 bis 558 °C und zersetzt sich eutektoid gemäß der Reaktion δ↔γ + ε bei 558 °C.
Die Löslichkeit von Kupfer in einer zinkbasierten η-Mischkristalllösung sinkt von 2,8 % (at.) bei 424 °C auf 0,31 % (at.) bei 100 °C. Die Gitterparameter der kupferbasierten α-Mischkristalllösung nehmen mit zunehmender Zinkkonzentration zu.
Die β-Phase hat ein raumzentriertes kubisches Gitter vom W-Typ, die β′-Phase hat ein geordnetes raumzentriertes Gitter vom CsCl-Typ. Die Gitterperiode der β′-Phase erhöht sich von O 2956 auf 0,2958 nm im Konzentrationsbereich von 48,23...49,3 % (at.) Zn.
Die γ-Phase hat eine Struktur vom γ-Messing-Typ. Seine Zusammensetzung entspricht der stöchiometrischen Zusammensetzung von Cu 5 Zn 8 . Die γ''′-Phase hat ein orthorhombisches Gitter mit Perioden α = 0,512 nm, b = 0,3658 nm und c = 0,529 nm.
Die γ''-Phase hat ein kubisches Gitter mit einer Periode α = 0,889 nm. Die Struktur und Gitterparameter der γ′- und γ-Phasen wurden nicht bestimmt. Phase 3 hat ein bcc-Gitter mit einer Periode α = 0,300 nm bei 600 °C für eine Legierung mit 74,5 Atom-% Zn. Die ε-Phase weist ein hexagonales Mg-Gitter auf.
Legierungen auf Basis des Kupfer-Zink-Systems (Messing) werden in verschiedenen Branchen häufig eingesetzt: Sie zeichnen sich durch hohe Herstellbarkeit und Korrosionsbeständigkeit aus. Die Herstellung verschiedener Teile und Gussteile aus Legierungen dieses Systems ist nicht besonders schwierig. Legierungen der Sorten L96, L90, L85, L80, L75, L70, L68, L66, L63, L59 – einfaches Messing – werden durch Druck im kalten und heißen Zustand verarbeitet und haben eine einphasige Struktur, die auf einer festen Lösung basiert Kupfer (a) für Legierungen mit einem Kupfergehalt von mindestens 61 Masse-% und zweiphasig (α + β) für Legierung L59. Ein- und zweiphasige Legierungen (α, α + β, β), legiert mit Aluminium, Eisen, Mangan, Silizium, Zinn, Blei, werden zur Herstellung von Gussteilen in verschiedenen Verfahren verwendet.
Derzeit werden neue Materialien auf Basis von Aluminium entwickelt, um den Anwendungsbereich dieser Materialien weiter zu erweitern. Für das Projekt eines umweltfreundlichen Flugzeugs, das mit flüssigem Wasserstoff (Temperatur: -253 °C) betrieben wird, war daher ein Material erforderlich, das bei solch niedrigen Temperaturen nicht versprödet. Die in Russland entwickelte O1420-Legierung auf Basis von mit Lithium und Magnesium legiertem Aluminium erfüllt diese Anforderungen. Aufgrund der Tatsache, dass beide Legierungselemente in dieser Legierung leichter als Aluminium sind, ist es außerdem möglich, das spezifische Gewicht des Materials und damit das Fluggewicht der Maschinen zu reduzieren. Durch die Kombination der guten Festigkeit von Duraluminium und der geringen Dichte weist die Legierung auch eine hohe Korrosionsbeständigkeit auf. Daher bewegen sich moderne Wissenschaft und Technologie auf dem Weg, Materialien zu schaffen, die ein Höchstmaß an nützlichen Eigenschaften vereinen.
Es ist auch zu beachten, dass es derzeit gleichzeitig mit der traditionellen alphanumerischen Kennzeichnung eine neue digitale Kennzeichnung von Aluminiumlegierungen gibt – siehe Abb. 3 und Tisch. 10.
Abbildung 3 – Prinzip der digitalen Markierung von Aluminiumlegierungen
Tabelle 10
Beispiele für Bezeichnungen mit den neuen Markierungen
|
Legierungselemente |
Markierung |
|
|
Traditionell | ||
|
Al (rein) | ||
Referenzliste
1. Kolachev B.A., Livanov V.A., Blagin V.I. Metallurgie und Wärmebehandlung von Nichteisenmetallen und -legierungen. M.: Metallurgie, 1972.-480 S.
2. Lakhtin Yu.M., Leontyeva V.P. Materialwissenschaften. M.: Maschinenbau, 1990.-528 S.
3. Gulyaev A.P. Metallurgie. M.: Metallurgie, 1986.-544 S.
4. Enzyklopädie anorganischer Materialien. Band 1.: Kiew: Chefredakteur der Ukrainischen Sowjetunion, 1977.-840 S.
5. Enzyklopädie anorganischer Materialien. Band 2.: Kiew: Chefredakteur der Ukrainischen Sowjetunion, 1977.-814 S.
6. Materialwissenschaft und Materialtechnologie. Fetisov G.P., Karpman M.G., Matyunin V.M. und andere. M.-V.Sh., 2000.- S.182
Anhang 1
Al-Mg-Phasendiagramm (a) und Abhängigkeit der mechanischen Eigenschaften
Legierungen je nach Magnesiumgehalt (b)
Anlage 2
ZustandsdiagrammAl - Cu:
gestrichelte Linie – Aushärtetemperatur von Legierungen

Anhang 3
ZustandsdiagrammAl – Si(a) und der Einfluss von Silizium
über die mechanischen Eigenschaften von Legierungen

Einführung. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . ………4
1 Aluminium. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . …...4
2 Legierungen auf Aluminiumbasis. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . …...5
2.1 Aluminium-Knetlegierungen,
nicht durch Wärmebehandlung gehärtet. . . . . . . . . . . . . . . . . . . . . . . . ........6
2.2 Aluminium-Knetlegierungen,
durch Wärmebehandlung verstärkt. . . . . . . . . . . . . . . . . . . . . . . . . . . ........7
2.3 Aluminiumgusslegierungen. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . ......elf
2.4 Pulvermetallurgisch hergestellte Legierungen………...……..…..14
Fazit…………………………………………………………….………………..……..16
Referenzen……………………….……………………………………...17
Anhang 1 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . …. . . . . . . . . . . . . . . . . . . ….19
Anlage 2. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . ... . . . . . . . . . . . . . . . . ….. 20
Anhang 3. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . ... . . . . . . . . . . . . . . . . ….21
Abteilung für theoretische Grundlagen der Materialwissenschaft
Aluminium ist einer der wichtigsten Werkstoffe in der Elektronikindustrie, sowohl in reiner Form als auch in zahlreichen darauf basierenden Legierungen. Reines Aluminium weist keine allotropen Modifikationen auf und weist eine hohe thermische und elektrische Leitfähigkeit auf, die 62–65 % der ähnlichen Parameter von Kupfer beträgt. Der Schmelzpunkt von Aluminium liegt bei 660 °C, der Siedepunkt bei 2500 °C. Die Härte von reinem Aluminium beträgt nach Brinell 25 HB. Aluminium lässt sich leicht durch Schneiden, Ziehen und Pressen bearbeiten.
Bei Kontakt mit Luft bildet sich auf der Aluminiumoberfläche ein porenfreier, etwa 2 nm dicker Oxidschutzfilm (20 Å), der das Aluminium vor weiterer Oxidation schützt. Aluminium weist in Alkalilösungen, Salz- und Schwefelsäuren eine geringe Korrosionsbeständigkeit auf. Organische Säuren und Salpetersäure haben darauf keinen Einfluss.
Die Industrie produziert Aluminium in verschiedenen Qualitäten: besondere Reinheit, hohe Reinheit und technische Reinheit. Hochreines Aluminium A999 enthält nicht mehr als 0,001 % Verunreinigungen; hochreine Qualitäten A995, A99, A97 bzw. A95 – nicht mehr als 0,005; 0,01; 0,03 und 0,05 % Verunreinigungen; technischer Reinheitsgrad A85 – nicht mehr als 0,15 % Verunreinigungen.
In der Elektronik wird reines Aluminium bei der Herstellung von Elektrolytkondensatoren und Folien sowie als Targets bei der Bildung von Aluminiumleiterbahnen mikroelektronischer Geräte mithilfe von thermischen, Ionenplasma- und Magnetron-Sputterverfahren verwendet.
Von größtem Interesse für die Elektrotechnik sind Legierungen auf Basis der Systeme Aluminium-Kupfer und Aluminium-Silizium, die zwei große Gruppen von Knet- und Gusslegierungen darstellen, die als Strukturmaterialien verwendet werden.
In Abb. Abbildung 2.7 zeigt das Gleichgewichtsdiagramm des Zustands des Systems „Aluminium – Kupfer“ von der Aluminiumseite. Die eutektische Legierung in diesem System enthält 33 % Kupfer und hat einen Schmelzpunkt von 548 °C. Mit zunehmendem intermetallischen Gehalt in der Legierung nimmt die Festigkeit der Legierung zu, ihre Bearbeitbarkeit verschlechtert sich jedoch. Die Löslichkeit von Kupfer in Aluminium beträgt bei Raumtemperatur 0,5 % und erreicht 5,7 % bei eutektischer Temperatur.
Legierungen mit einem Kupfergehalt von bis zu 5,7 % können durch Abschrecken bei einer Temperatur oberhalb der Linie in einen einphasigen Zustand überführt werden B.D. Gleichzeitig weist die gehärtete Legierung eine ausreichende Duktilität bei mäßiger Festigkeit auf und kann durch Verformung verarbeitet werden. Die nach dem Abschrecken gebildete feste Lösung befindet sich jedoch nicht im Gleichgewicht, und es treten darin Prozesse zur Trennung intermetallischer Verbindungen auf, die mit einer Erhöhung der Festigkeit der Legierungen einhergehen. Bei Raumtemperatur erfolgt dieser Prozess innerhalb von 4-6 Tagen und wird als natürliche Alterung der Legierung bezeichnet. Die Beschleunigung des Alterungsprozesses des Materials wird durch die Aufrechterhaltung erhöhter Temperaturen gewährleistet; dieser Vorgang wird als künstliche Alterung bezeichnet.
Reis. 2.7. Zustandsdiagramm des Aluminium-Kupfer-Systems Eine weitere Gruppe von Aluminiumlegierungen, sogenannte Aluminiumgusslegierungen oder Silumine, sind Legierungen, die auf dem Aluminium-Silizium-System basieren. Das Zustandsdiagramm dieses Systems ist in Abb. dargestellt. 2.8.

Reis. 2.8.
Die eutektische Legierung enthält 11,7 % Silizium und hat einen Schmelzpunkt von 577 °C. In diesem System werden keine intermetallischen Verbindungen gebildet. Eutektische Legierungen zeichnen sich durch gute Gusseigenschaften und zufriedenstellende mechanische Eigenschaften aus, die durch die Zugabe von bis zu 1 % Natriumverbindungen in die Legierung verbessert werden.
Abhängig von der Herstellungsmethode werden industrielle Aluminiumlegierungen in gesinterte, gegossene und geknetete Aluminiumlegierungen unterteilt (Abb. 1).
Gusslegierungen unterliegen einer eutektischen Umwandlung, verformbare jedoch nicht. Letztere wiederum können thermisch nicht härtend (Legierungen, bei denen im festen Zustand keine Phasenumwandlungen stattfinden) und verformbar, thermisch härtend (durch Härten und Altern gehärtete Legierungen) sein.
Aluminiumlegierungen werden üblicherweise mit Cu, Mg, Si, Mn, Zn und seltener mit Li, Ni, Ti legiert.
Verformte Aluminiumlegierungen, die durch Wärmebehandlung nicht verstärkt werden können
Zu dieser Legierungsgruppe gehören technisches Aluminium und thermisch nicht aushärtende schweißbare korrosionsbeständige Legierungen (Legierungen aus Aluminium mit Mangan und Magnesium). AMts-Legierungen gehören zum Al-Mi-System (Abb. 1).
Abb.1. Zustandsdiagramm „Aluminium – Legierungselement“:
1–verformbare, thermisch nicht aushärtende Legierungen;
2–verformbare, thermisch härtbare Legierungen.

Abb.2. Zustandsdiagramm „Aluminium – Mangan“:
–Mn-Konzentration in Industrielegierungen.

Abb. 3. Mikrostruktur einer AMC-Legierung

Abb.6. Mikrostruktur von Duraluminium nach:
a) Abschrecken in Wasser ab Temperatur T2;
b) Härten und künstliches Altern bei T3
(rechts – schematisches Bild)
Die Struktur der Amts-Legierung besteht aus einer a-festen Lösung von Mangan in Aluminium und sekundären Ausscheidungen der MnAl-Phase (Abb. 3). In Gegenwart von Eisen wird anstelle von MnAl eine komplexe Phase (MnFe)Al gebildet, das in Aluminium praktisch unlöslich ist, weshalb die Amts-Legierung durch Wärmebehandlung verfestigt wird.
Die Zusammensetzung dieser Legierungen unterliegt sehr engen Grenzen: 1–1,7 % MP;
0,05 – 0,20 % Cu; Um Lochfraß zu reduzieren, wird Kupfer hinzugefügt.
Zulässig bis zu 0,6–0,7 % Fe und. n 0,6–0,7 % Si, was zu einer gewissen Verstärkung der Legierungen ohne nennenswerten Verlust der Korrosionsbeständigkeit führt.
Da die Temperatur sinkt, nimmt die Festigkeit schnell zu. Daher werden Legierungen dieser Gruppe häufig in der Kryotechnik eingesetzt.
AMg (Magnalium)-Legierungen gehören zum A1-Mg-System (Abb. 4). Magnesium bildet mit Aluminium eine a-Mischkristalllösung, und im Konzentrationsbereich von 1,4 bis 17,4 % Mg wird eine sekundäre b-Phase (MgAl) freigesetzt, aber Legierungen mit bis zu 7 % Mg ergeben bei der Wärmebehandlung nur eine sehr geringe Verfestigung Sie verstärkten sich durch plastische Verformung – Verfestigung.
Legierungen der A1–Mn-Systeme. und A1–Mg werden im geglühten, kaltverformten und halbverfestigten Zustand verwendet. Industrielegierungen enthalten Magnesium im Bereich von 0,5 bis 12... 13 %, Legierungen mit niedrigem Magnesiumgehalt haben die beste Formbarkeit, Legierungen mit hohem Magnesiumgehalt haben gute Gusseigenschaften (Tabelle 5) Anwendungen.
Auf Schiffen werden Rettungsboote, Davits, Außenbordleitern, praktische Gegenstände usw. aus Legierungen dieser Gruppe hergestellt.
Verformte Aluminiumlegierungen, durch Wärmebehandlung verstärkt
Zu dieser Legierungsgruppe gehören Legierungen mit hoher und normaler Festigkeit. Die Zusammensetzungen einiger verformbarer thermisch härtbarer Legierungen sind in Tabelle 6 des Anhangs aufgeführt. Typische verformbare Aluminiumlegierungen sind Duralumine (gekennzeichnet mit dem Buchstaben D) – Legierungen des Systems A1 – Cu – Mg. Sehr vereinfacht können die Vorgänge bei der verfestigenden Wärmebehandlung von Duraluminium anhand des Al-Cu-Diagramms (Abb. 5) betrachtet werden.

Abb.4. Diagramm des Zustands „Aluminium – Magnesium“.
‚ – Konzentration von Mg in Industrielegierungen.

Abb.5. Fragment des Zustandsdiagramms „Aluminium – Kupfer“:
T1 – Reflow-Temperatur;
Т2 – Härtetemperatur;
T3 – Temperatur der künstlichen Alterung.


Abb.7. Phasendiagramm Aluminium-Silizium:
a) Gesamtansicht;
b) nach Einführung des Modifikators.
Während des Abschreckens, das darin besteht, die Legierung über die Linie variabler Löslichkeit zu erhitzen, bei dieser Temperatur zu halten und schnell abzukühlen, entsteht die Struktur einer übersättigten a-festen Lösung (hell in Abb. 6a) und unlöslicher Einschlüsse von Eisen- und Manganverbindungen (dunkel). ) Ist repariert. Die Legierung hat im frisch abgeschreckten Zustand eine geringe Festigkeit s6 = 30 kg/mm3 (300 MPa); d = 18 %; Härte HB75.
Eine übersättigte feste Lösung ist instabil. Die höchste Festigkeit wird durch anschließende Alterung der gehärteten Legierung erreicht. Die künstliche Alterung besteht in der Einwirkung einer Temperatur von 150 bis 180 Grad. Dabei werden aus der übersättigten a-Mischkristalllösung die Verfestigungsphasen CuAl2, CuMgAl2, Al12Mn2Cu freigesetzt.
Die Mikrostruktur der gealterten Legierung ist in Abb. 6b dargestellt. Es besteht aus einer festen Lösung und Einschlüssen verschiedener der oben genannten Phasen.
Aluminiumverarbeitung
Alle Aluminiumlegierungen lassen sich in zwei Gruppen einteilen:
Verformbare Aluminiumlegierungen – bestimmt für die Herstellung von Halbzeugen (Bleche, Platten, Stangen, Profile, Rohre usw.) sowie von Schmiedestücken und gestanzten Rohlingen durch Walzen, Pressen, Schmieden und Stanzen.
a) Durch Wärmebehandlung gestärkt:
Duraluminium, „Duraluminium“ (D1, D16, D20*, Legierungen aus Aluminium, Kupfer und Mangan) – lässt sich im gehärteten und gealterten Zustand zufriedenstellend schneiden, im geglühten Zustand jedoch schlecht. Duraluminiumlegierungen lassen sich gut durch Punktschweißen schweißen und können aufgrund ihrer Neigung zur Rissbildung nicht durch Schmelzschweißen geschweißt werden. Die Legierung D16 wird zur Herstellung von Häuten, Rahmen, Stringern und Holmen von Flugzeugen, tragenden Rahmen, Gebäudestrukturen und Autokarosserien verwendet.
Die Avial-Legierung (AV) lässt sich nach dem Aushärten und Altern durch Schneiden zufriedenstellend verarbeiten und lässt sich durch Argon-Lichtbogen- und Widerstandsschweißen gut verschweißen. Aus dieser Legierung werden verschiedene Halbzeuge (Bleche, Profile, Rohre usw.) hergestellt, die für mäßig belastete Strukturelemente, aber auch Rotorblätter von Hubschraubern, geschmiedete Motorteile, Rahmen und Türen verwendet werden, die eine hohe Duktilität bei Kälte erfordern Wetter. und heiß.
Hochfeste Legierung (B95) hat eine Zugfestigkeit von 560–600 N/mm2, lässt sich gut durch Schneiden bearbeiten und durch Punktschweißen verschweißen. Die Legierung wird im Flugzeugbau für belastete Strukturen (Haut, Stringer, Spanten, Holme) und für tragende Rahmen in Gebäudestrukturen verwendet.
Legierungen zum Schmieden und Stanzen (AK6, AK8, AK4-1 [hitzebeständig]). Legierungen dieser Art zeichnen sich durch eine hohe Duktilität und zufriedenstellende Gießeigenschaften aus, die die Herstellung hochwertiger Barren ermöglichen. Aluminiumlegierungen dieser Gruppe lassen sich gut schneidend verarbeiten und können durch Widerstands- und Argon-Lichtbogenschweißen zufriedenstellend geschweißt werden.
b) Nicht durch Wärmebehandlung gehärtet:
Legierungen aus Aluminium mit Mangan (AMc) und Aluminium mit Magnesium (AMg2, AMg3, AMg5, AMg6) lassen sich leicht durch Druck verarbeiten (Stanzen, Biegen), sind gut schweißbar und weisen eine gute Korrosionsbeständigkeit auf. Das Schneiden ist schwierig, daher werden zur Herstellung von Gewinden spezielle spanlose Gewindebohrer (Rollen) ohne Schneidkanten verwendet.
Aluminiumgusslegierungen – für den Formguss bestimmt (in der Regel lassen sie sich durch Schneiden gut bearbeiten).
Aluminiumlegierungen mit Silizium (Silumine) Al-Si (AL2, AL4, AL9) zeichnen sich durch hohe Gusseigenschaften und Gussteile durch eine hohe Dichte aus. Silumine lassen sich relativ einfach durch Schneiden bearbeiten.
Legierungen aus Aluminium mit Kupfer Al-Cu (AL7, AL19) weisen nach der Wärmebehandlung hohe mechanische Eigenschaften bei normalen und erhöhten Temperaturen auf und lassen sich gut durch Schneiden bearbeiten.
Aluminiumlegierungen mit Magnesium Al-Mg (AL8, AL27) haben eine gute Korrosionsbeständigkeit, verbesserte mechanische Eigenschaften und sind leicht zu schneiden. Legierungen werden im Schiffbau und in der Luftfahrt eingesetzt.
Hitzebeständige Aluminiumlegierungen (AL1, AL21, AL33) lassen sich durch Schneiden gut bearbeiten.
Hinsichtlich des Fräsens, Gewindeschneidens und Drehens lassen sich Aluminiumlegierungen ebenfalls in zwei Gruppen einteilen. Je nach Zustand (gehärtet, gealtert, geglüht) können Aluminiumlegierungen unterschiedlichen Helligkeitsgruppen angehören
wird bearbeitet:
Weiche und duktile Aluminiumlegierungen, die beim Schneiden Probleme verursachen:
a) Geglüht: D16, AB.
b) Nicht durch Wärmebehandlung gehärtet: AMts, AMg2, AMg3, AMg5, AMg6.
Relativ harte und haltbare Aluminiumlegierungen, die sich durch Schneiden recht leicht bearbeiten lassen (in vielen Fällen, in denen keine höhere Produktivität erforderlich ist, können diese Materialien mit Standardwerkzeugen für den allgemeinen Gebrauch bearbeitet werden, wenn Sie jedoch die Geschwindigkeit und Qualität der Bearbeitung erhöhen müssen, es ist notwendig, spezielle Werkzeuge zu verwenden):
a) Gehärtet und künstlich gealtert: D16T, D16N, AVT.
b) Schmieden: AK6, AK8, AK4-1.
c) Gießereien: AL2, AL4, AL9, AL8, AL27, AL1, AL21, AL33.
Ein charakteristisches Merkmal von Aluminium ist seine geringe Dichte (2,7 g/cm3), sein niedriger Schmelzpunkt (660 °C) und sein relativ geringer elektrischer Widerstand, der nur 1,51-mal höher ist als der von Kupfer. Aluminium hat ein kubisch flächenzentriertes Gitter und ist in seiner reinen Form ein sehr weiches, duktiles Metall. Als chemisches Element sollte Aluminium Wasser wie Kalzium langsam zersetzen, der Oxidfilm auf seiner Oberfläche schützt das Metall jedoch zuverlässig vor Wechselwirkungen mit Wasser und Luftsauerstoff. Dank dieser haltbaren, sehr dünnen und transparenten Oxidschicht behält Aluminium lange Zeit sein glänzendes Aussehen.
Reinaluminium wird häufig als elektrisch leitfähiges Material verwendet; Auf Basis von Aluminium wurden zahlreiche Legierungen hergestellt, die hauptsächlich in der Luftfahrt verwendet werden. In den letzten Jahren wurden Aluminiumlegierungen aktiv in der Automobilindustrie, der Lebensmittelindustrie (Verpackungsmaterial) und Haushaltsgeräten eingeführt. Besonders rasant nimmt die Verwendung von Aluminium im Bauwesen als Veredelungs- und Dekorationsmaterial zu, das sehr beständig gegen atmosphärische Korrosion ist. Die weltweite Aluminiumproduktion nimmt sehr schnell zu: In 18 Jahren (von 1955 bis 1973) hat sie sich vervierfacht. Die Kosten für Aluminium sind etwa fünf- bis zehnmal höher als für Kohlenstoffstahl.
Die Industrie produziert verschiedene Aluminiumqualitäten, die sich im Gesamtgehalt an Verunreinigungen unterscheiden – von 0,001 bis 1,0 %. Die wichtigsten natürlichen Verunreinigungen in Aluminium sind Eisen und Silizium. Auf dem Aluminium-Silizium-Phasendiagramm (Abb. 55) liegt ein eutektischer Punkt bei 577 °C und 11,7 % Si. Die Löslichkeit von Silizium in festem Aluminium beträgt bei dieser Temperatur 1,6 %. Wenn die Temperatur auf 200 °C sinkt, sinkt sie auf 0,05 %. Das Aluminium-Eisen-Phasendiagramm ist komplex und weist mehrere Zwischenphasen auf. Die reichhaltigste Aluminiumverbindung ist FeAl 3 . Zwischen ihm und Aluminium liegt ein eutektischer Punkt bei 655°C und 1,8 % Eisen (Abb. 56). Die Löslichkeit von Eisen in festem Aluminium beträgt bei der eutektischen Temperatur 0,05 %, unter 400 °C sinkt sie auf Null. Dies bedeutet, dass in doppelt untereutektischen Legierungen aus Aluminium und Eisen letzteres immer in Form von Einschlüssen der FeAl 3 -Phase ausfällt, die entweder eutektischen Ursprungs sind oder durch die Zersetzung einer festen Lösung entstehen. Aufgrund der Nikönnen sich eutektische Niederschläge bei deutlich geringeren Eisenkonzentrationen als 0,05 % bilden.

In Aluminium, das sowohl Eisen als auch Silizium enthält, können zusätzlich zu den angegebenen Phasen, die für binäre Systeme charakteristisch sind, auch komplexe ternäre Verbindungen auftreten – α-FeAlSi und β-FeAlSi. Sie können bei hohen Verunreinigungsgehalten direkt während der Kristallisation oder als Folge der Zersetzung einer festen Lösung entstehen. Verunreinigungen von Eisen und Silizium im Aluminium sind schädlich, da sie dessen plastische Eigenschaften deutlich beeinträchtigen. Beide Verunreinigungen sind nicht nur im Primäraluminium enthalten, ihre Menge nimmt in Aluminiumlegierungen während des Umschmelzens aufgrund der Wechselwirkung mit Kieselsäure in feuerfesten Materialien und Stahlschmelzwerkzeugen (Löffel, Schaber) kontinuierlich zu. Allerdings gibt es viele Legierungen, bei denen Silizium und manchmal auch Eisen absichtlich eingebracht werden.

Die Besonderheit von Aluminium als Basis für Legierungen besteht darin, dass es mit keinem Metall kontinuierliche feste Lösungen bildet. Nur im System mit Zink (Abb. 57) gibt es bei erhöhten Temperaturen einen ausreichend großen Bereich fester Lösungen. In den allermeisten Fällen treten in Aluminium-Metall-Binärsystemen spröde Zwischenphasen auf. Eine Verfestigung von Aluminium durch die Bildung fester Lösungen ist daher nur bedingt möglich. Daher wird eine andere Art der Verstärkung genutzt – durch die Bildung von Verbundpartikeln in einer festen Lösungsmatrix. Dieser Weg bestimmt zwangsläufig den Einsatz von Härtung und Alterung. Die begrenzte Auswahl an festen Lösungen auf Aluminiumbasis zwingt uns dazu, für jede Legierungskomponente einen solchen Gehalt anzugeben, der nicht zum Auftreten einer übermäßigen Menge spröder Zwischenphasen führt.
Aluminiumknetlegierungen enthalten in der Regel 2 – 3 oder mehr Legierungsbestandteile in Mengen von jeweils 0,2 bis 2 – 4 %. Einzige Ausnahme bilden die Doppellegierungen AMts mit 1,0 – 1,6 % Mn. Mangan ist in der Zusammensetzung der meisten Aluminiumknetlegierungen in einer Menge von 0,2 bis 1,5 % enthalten. Sein Zweck besteht darin, die Rekristallisation erheblich zu verlangsamen, die Temperatur dieses Prozesses zu erhöhen und dadurch die Legierung bei erhöhten Temperaturen zu festigen, das rekristallisierte Korn zu verfeinern und Teil komplexer Verbindungen zu sein, die den Legierungen Hitzebeständigkeit verleihen.
Die meisten Aluminiumknetlegierungen können dem Härten (ohne polymorphe Umwandlung) und der Alterung standhalten und werden dadurch deutlich fester. Typische Legierungsbestandteile der betrachteten Legierungen sind neben Mangan Kupfer, Magnesium, Silizium, Zink. Spezielle hitzebeständige Legierungen enthalten Eisen, Nickel, Chrom, Titan in einer Menge von 0,2 - 1 %. Bei allen Aluminiumlegierungen führt die Zugabe von 0,1 – 0,2 % Titan zu einer starken Kornfeinung im Gusszustand. Dieser Effekt bleibt nach der Rekristallisation teilweise erhalten. Beryllium (0,001 – 0,002 %) wird einigen Legierungen zugesetzt, um die Oxidation beim Schmelzen zu reduzieren.

In Abb. Die Abbildungen 58 und 59 zeigen Dualphasendiagramme von Aluminium mit Kupfer und Magnesium. In beiden Fällen ist mit steigender Temperatur eine deutliche Veränderung der Löslichkeit der Legierungselemente im Aluminium zu beobachten. Eine ähnliche Änderung der Löslichkeit wird bei Mehrkomponentensystemen beobachtet, was die Möglichkeit einer verstärkten Wärmebehandlung bietet. In komplexen Legierungen befinden sich jedoch Phasen mit komplexer Zusammensetzung und Struktur gemäß den entsprechenden Phasendiagrammen im Gleichgewicht mit der Aluminiumlösung.

Typische Aluminiumknetlegierungen sind das sogenannte Duraluminium – Legierungen aus Aluminium mit Kupfer, Magnesium und Mangan. Die Zusammensetzungen einiger typischer Aluminiumknetlegierungen sind in der Tabelle aufgeführt. 5. Dort ist auch die Zusammensetzung der Verunreinigungen einer der Aluminiumsorten angegeben.
Tabelle 5. Zusammensetzung einiger Aluminium-Knetlegierungen
| Legierungssorte | Legierungsbestandteile, % Rest Al | Verunreinigungen, % nicht mehr | ||||||||
| Cu | Mg | Mn | Si | Zn | Andere | Fe | Si | Cu | Zn | |
| A5 | - | - | - | - | - | - | 0,3 | 0,3 | 0,02 | 0,06 |
| AMts | - | - | 1,0 - 1,6 | - | - | - | 0,7 | 0,6 | 0,2 | 0,1 |
| AMg6 | - | 5,8 - 6,8 | 0,5 - 0,8 | - | - | 0,1 Ti; 0,001 Ve | 0,7 | - | 0,1 | 0,2 |
| D16 (Duraluminium) | 3,8 - 4,9 | 1,2 - 1,8 | 0,3 - 0,9 | - | - | - | 0,2 | 0,25 | - | 0,1 |
| AK8 (Superduraluminium) | 3,9 - 4,8 | 0,4 - 0,8 | 0,4 - 1,0 | 0,6 - 1,2 | - | - | 0,3 | - | - | 0,1 |
| B95 | 1,4 - 2,0 | 1,8 - 2,8 | 0,2 - 0,6 | - | 5,0 - 7,0 | 0,1 - 0,25 Cr | 0,3 | 0,3 | - | - |
Die mechanischen Eigenschaften dieser Legierungen in verschiedenen Zuständen sind in der Tabelle angegeben. 6. Wie man sieht, ist es durch Legieren, Kalthärten und Wärmebehandlung möglich, die Festigkeit (von 100 auf 560 MPa) und die Härte HB (20 - 150) von Aluminium um ein Vielfaches zu erhöhen. Bei hochfesten Aluminiumlegierungen fällt die spezifische Festigkeit, also bezogen auf die Dichte, höher aus als bei Stählen und anderen Legierungen. Genau das prägte ihren Einsatz in Flugzeugen.
Verformbare Aluminiumlegierungen werden neben dem Härten und Altern häufig einer Glühhomogenisierung unterzogen. Dies wird durch die Tatsache erklärt, dass aufgrund der Niin den Legierungen eine sehr starke dendritische Entmischung auftritt und eutektische Nichtgleichgewichtskomponenten auftreten. Besonders stark abgereichert sind Magnesium und Kupfer. Dem Gleichgewichtszustandsdiagramm zufolge sollte der eutektische Anteil in Aluminium-Kupfer-Legierungen also erst bei 5,65 % Cu auftreten, er tritt jedoch bereits bei 1,6 - 2 % Cu auf. Ein Merkmal des Erhitzens zum Härten von Aluminiumlegierungen ist die Notwendigkeit, die Temperatur sehr streng einzuhalten (±5°), um ein Ausbrennen (Schmelzen) zu verhindern und den größten Effekt der Wärmebehandlung zu erzielen. So werden die Legierungen D16 und AK8 ab einer Temperatur von 495 – 505 °C und die Legierung V95 – von 465 – 480 °C gehärtet. Die Aushärtung erfolgt in Wasser. Nach dem Aushärten werden Aluminiumlegierungen einer natürlichen (20°C, 4 – 5 Tage) oder künstlichen Alterung unterzogen. Die künstliche Alterung erfolgt je nach Legierungszusammensetzung bei 120 – 195 °C für 6 – 12 Stunden. Das Rekristallisationsglühen erfolgt bei 300 – 350 °C (Reinaluminium) und bei 350 – 420 °C (Legierungen). ).
Wie bereits erwähnt, ist reines Aluminium sehr beständig gegen atmosphärische Korrosion. Aluminiumlegierungen, die Kupfer und Zink enthalten, schneiden in dieser Hinsicht deutlich schlechter ab. Doppellegierungen mit Mangan und Magnesium (AMts und AMg) widerstehen atmosphärischer Korrosion sehr gut.
Tabelle 6. Mechanische Eigenschaften von Aluminium und einigen Knetlegierungen in verschiedenen Zuständen
| Legierungssorte | Zustand | σ in, MPa | σ t, MPa | δ, % | ψ, % | NV |
| A5 | geglüht | 80 | 60 | 30 - 40 | 70 - 90 | 25 |
| Gehärtet | 150 | 120 | 5 - 10 | 50 - 60 | 35 | |
| AMts | geglüht | 130 | 50 | 20 | 70 | 30 |
| Gehärtet | 220 | 180 | 5 | 50 | 55 | |
| AMg6 | geglüht | 340 | 170 | 20 | - | 70 |
| D16 | geglüht | 210 | 110 | 18 | 55 | 42 |
| Temperiert und natürlich gealtert | 450 | 330 | 17 | 30 | 105 | |
| AK8 | 480 | 380 | 10 | 25 | 135 | |
| B95 | geglüht | 260 | 130 | 13 | - | - |
| Temperiert und künstlich gealtert | 560 | 530 | 8 | 12 | 150 |
Aluminiumgusslegierungen enthalten fast die gleichen Legierungsbestandteile wie Knetlegierungen, jedoch in viel größeren Mengen und in den entsprechenden Phasendiagrammen liegen Gusslegierungen näher an der eutektischen Konzentration. Wie in § 18 dargelegt wurde, verfügen nur solche Legierungen über die notwendigen gießtechnischen Eigenschaften, die es ermöglichen, aus ihnen formgesunde Gussteile zu gewinnen.
Viele Aluminiumgusslegierungen basieren auf dem Aluminium-Silizium-System (siehe Abb. 55) und heißen Silumine. Das doppelte Eutektikum Aluminium - Silizium hat eine sehr grobe Struktur, Silizium wird in Form großer Platten (in dünnen Abschnitten - in Form von Nadeln) freigesetzt (Abb. 60, a). Daher werden solche Legierungen einer Modifikation unterzogen, die darin besteht, vor dem Gießen Natrium in die Schmelze einzuführen, das durch eine Austauschreaktion mit einem Natriumfluorid enthaltenden Flussmittel entsteht. Unter dem Einfluss von Tausendstel Prozent Natrium werden Siliziumniederschläge stark zerkleinert (Abb. 60, b) und die Festigkeit und Duktilität der Legierung nehmen zu.

Eine bedeutende Gruppe von Aluminiumgusslegierungen basiert auf dem Ternärsystem Aluminium – Silizium – Kupfer und dem Doppelsystem Aluminium – Magnesium. Eine besondere Gruppe bilden hitzebeständige Aluminiumlegierungen mit 4 – 5 % Kupfer und geringen Zusätzen von Übergangsmetallen. Die Gießeigenschaften solcher Legierungen sind sehr schlecht.
Viele Aluminiumgusslegierungen werden verschiedenen Arten der Wärmebehandlung unterzogen. Folgende Bezeichnungen für Wärmebehandlungsarten werden akzeptiert: T1 – Alterung (nach dem Gießen ohne Härten), T2 – Glühen, T4 – Härten, T5 – Härten und teilweises Altern, T6 – Härten und vollständiges Altern bis zur maximalen Härte, T7 – Härten und stabilisierendes Anlassen, T8 – härtendes und erweichendes Anlassen. Die Eigenschaften von Aluminiumgusslegierungen hängen maßgeblich vom Gießverfahren ab, wobei die Abkühlgeschwindigkeit beim Erstarren des Gussstücks und beim Abkühlvorgang (bei aushärtungsfähigen Legierungen) eine entscheidende Rolle spielt. Im Allgemeinen führt eine Erhöhung der Wärmeabfuhr zu einer Erhöhung der Festigkeit und der plastischen Eigenschaften. Daher sind die mechanischen Eigenschaften von Gussteilen, die durch Gießen in Sand-Ton-Formen und unter Verwendung von Wachsausschmelzmodellen erhalten werden, geringer als beim Gießen in einer Kokillenform, und beim Gießen unter Druck erhöhen sich die Eigenschaften aufgrund der sehr starken Abkühlung erheblich dass es sich beispielsweise bei Siluminen um eine unnötige Modifikation mit Natrium handelt. Aus dem gleichen Grund ist beim Gießen in einer Kokille und unter Druck ein höherer Gehalt an schädlichen Eisenverunreinigungen zulässig.
Tabelle 7. Zusammensetzung einiger Aluminiumgusslegierungen
| Legierungssorte | Legierungsbestandteile, % (der Rest ist Al) | Verunreinigungen, % nicht mehr | ||||||||
| Si | Cu | Mn | Mg | Fe | Si | Mg | Cu | Zn | Summe | |
| AL2 | 10 - 13 | - | - | - | 0,8 - 1,5 | - | 0,1 | 0,6 | 0,3 | 2,2 - 2,8 |
| AL4 | 8 - 10 | - | 0,25 - 0,50 | 0,17 - 0,30 | 0,6 - 1,0 | - | - | 0,3 | 0,3 | 1,2 - 1,6 |
| AL8 | - | - | - | 9,5 - 11,5 | 0,3 | 0,3 | - | 0,3 | 0,1 | 2,2 |
| AL10V (AK8M7) | 4 - 6 | 5 - 8 | - | 0,2 - 0,5 | 1,2 - 1,3 | - | - | 0,5 Mio | 0,6 | 2,5 - 2,7 |
| AL19 | - | 4,5 - 5,3 | 0,6 - 1,0 | 0,15 - 0,35 Ti | 0,2 | 0,3 | 0,05 | - | 0,2 | 0,8 - 1,0 |
In der Tabelle Tabelle 7 zeigt die Zusammensetzungen einiger der häufigsten Aluminiumgusslegierungen und Tabelle. 8 - ihre mechanischen Eigenschaften.
Die Legierung AL2 ist ein einfaches Doppelsilumin mit eutektischer Zusammensetzung, das keine Aushärtung verträgt. Seine Wärmebehandlung beschränkt sich auf das Glühen nach dem Gießen, um Spannungen abzubauen. Bei der AL4-Legierung handelt es sich um Silumin mit einer untereutektischen Zusammensetzung, in die Magnesium eingebracht ist, was aufgrund der unterschiedlichen Löslichkeit der Mg 2 Si-Verbindung in Aluminium die Möglichkeit zur Härtung und Alterung bietet. Beide Legierungen sind mit Natrium modifiziert. Die Legierung AL10V (AK5M7) basiert auf dem Aluminium-Silizium-Kupfer-System mit Magnesiumzusätzen. Die Härtung und Alterung der Legierung wird durch die variable Löslichkeit komplexer Verbindungen in Aluminium gewährleistet, und gute Gusseigenschaften werden durch eine ausreichende Menge an zweifach eutektischem A1-Si und dreifach eutektischem A1-Si-Al 2 Cu gewährleistet. Bei der Legierung AL8 handelt es sich praktisch um eine Doppellegierung aus Aluminium und Magnesium. Seine Zusammensetzung liegt weit vom eutektischen Punkt entfernt, es weist einen großen Kristallisationsbereich auf und weist daher geringe Gießeigenschaften auf. Gute mechanische Eigenschaften – geringe Dichte (2,55 g/cm2), ausgezeichnete Korrosionsbeständigkeit – bestimmen jedoch seine recht breite Verwendung. Eine Erhöhung des Magnesiumgehalts und eine Annäherung an die eutektische Zusammensetzung würden die Gusseigenschaften verbessern, allerdings wird ein normales Schmelzen ohne Beschichtungsflussmittel unmöglich, da die Schmelze stark oxidiert ist. Die Legierung AL 19 ist ein typisches Hochtemperaturmaterial, das bei 300 °C eingesetzt werden kann.
Tabelle 8. Mechanische Eigenschaften von Aluminiumgusslegierungen
| Legierungssorte | Zustand | σ in, MPa | δ, % | NV |
| AL2 | Besetzung geändert | 150 | 4 | 50 |
| Modifiziert und wärmebehandelt gemäß T2 (Glühen bei 300 ± 10 °C für 3 Stunden) | 140 | 4 | 50 | |
| AL4 | Besetzung unverändert | 150 | 2 | 50 |
| Modifiziert und wärmebehandelt gemäß T6 (Abschrecken ab 535 ± 5 °C in Wasser, Glühen bei 175 ± 5 °C, 15 h) | 230 | 3 | 70 | |
| AL8 | Wärmebehandelt gemäß T4 (Aushärtung zu Öl nach Einwirkung von 430 ± 5 °C, 20 Stunden) | 290 | 9 | 60 |
| AL10V (AK5M7) | In Sand-Ton-Form gegossen | 130 | - | 80 |
| Chillige Besetzung | 160 | - | 80 | |
| In Sand-Ton-Form gegossen, wärmebehandelt nach T1 (Alterung bei 175°C, 10 Stunden) | 150 | - | 80 | |
| In eine Kokille gegossen, wärmebehandelt nach T1 (Alterung bei 175°C, 10 Stunden) | 170 | - | 90 | |
| AL19 | Wärmebehandelt nach T5 (Härtung ab 545 ± 5 °C nach 10-stündiger Einwirkung von Wasser und Alterung bei 175 ± 5 °C, 5 Stunden) | 340 | 4 | 90 |
Bei allen Aluminiumgusslegierungen sind 0,8 – 1,2 % Eisen als Verunreinigung zulässig, die beim Umschmelzen zwangsläufig in das Metall gelangt. Daher ist in allen Legierungen der Mangangehalt angegeben, der die schädliche Wirkung von Eisen abschwächt und die nadelförmigen Sekrete der Eisenkomponente in kompakte Sekrete umwandelt.
Es gibt eine sehr große Gruppe von Aluminiumlegierungen, die durch Schmelzen von Abfällen gewonnen und in Form von Barren hergestellt werden. Früher wurden diese Legierungen als sekundär bezeichnet. In der Zusammensetzung unterscheiden sie sich kaum von herkömmlichen Aluminiumgusslegierungen, enthalten jedoch einen erhöhten Eisenanteil und einige unkontrollierte Verunreinigungen, insbesondere Sauerstoff in Form von Aluminiumoxidfilmen. Diese Legierungen werden durch Markierungen mit dem Zusatz „ch“ (in Schweinen) gekennzeichnet.
In den letzten Jahren sind Antifriktions-Doppellegierungen auf Aluminiumbasis aufgetaucht, die Antimon, Zinn, Kupfer und Blei in Mengen von 3 - 6 % enthalten. Die Legierungen sind für Gleitlagerschalen vorgesehen. Aluminiumlegierungen dieser Art werden durch Druckverarbeitung in Form einer Schicht auf einem Stahlband erhalten. Einsätze aus einer Aluminium-Blei-Legierung werden pulvermetallurgisch hergestellt. Ein charakteristisches Merkmal von Antifriktions-Aluminiumlegierungen (wie auch von Antifriktionslegierungen im Allgemeinen) ist eine zweiphasige Struktur, wobei die Phasen deutlich unterschiedliche Härten aufweisen. Im Betrieb, bei der Reibung mit dem Zapfen einer Stahlwelle, entsteht die Weichphase stärker und die entstehenden Lücken dienen als natürliche Kanäle, durch die sich der Schmierstoff über die gesamte Reibfläche verteilt. In einer Legierung aus Aluminium mit Antimon und Kupfer besteht die harte Phase aus den Verbindungen AlSb und A1 2 Cu und die weiche Phase aus dem Aluminium selbst. In Legierungen mit Zinn und Blei bilden diese Metalle weiche Schichten entlang der Grenzen härterer Aluminiumkörner.