Infecții perinatale la gravide. Tipuri de infecții perinatale. Protocol clinic din îngrijirea obstetricală „Infecții perinatale”
– un grup de boli ale fătului și nou-născutului care se dezvoltă ca urmare a infecției în perioada prenatală sau în timpul nașterii. Infecțiile intrauterine pot duce la moartea fătului, avortul spontan, întârzierea creșterii intrauterine, nașterea prematură, formarea de defecte congenitale, afectarea organelor interne și a sistemului nervos central. Metodele de diagnosticare a infecțiilor intrauterine includ studii microscopice, culturale, imunoenzimatice și biologice moleculare. Tratamentul infecțiilor intrauterine se efectuează folosind imunoglobuline, imunomodulatoare, medicamente antivirale și antibacteriene.

Informații generale
Infecțiile intrauterine sunt procese patologice și boli cauzate de infecția antenatală și intrapartum a fătului. Prevalența reală a infecțiilor intrauterine nu a fost stabilită, însă, conform datelor generalizate, cel puțin 10% dintre nou-născuți se nasc cu infecții congenitale. Relevanța problemei infecțiilor intrauterine în pediatrie se datorează pierderilor mari de reproducere, morbidității neonatale precoce, care duc la dizabilități și deces postnatal a copiilor. Problemele de prevenire a infecțiilor intrauterine se află în domeniul obstetricii și ginecologiei, neonatologiei și pediatriei.

Cauzele infecțiilor intrauterine
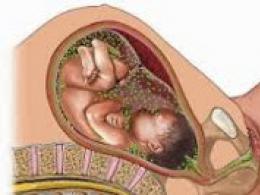
Infecțiile intrauterine se dezvoltă ca urmare a infecției fătului în perioada prenatală sau direct în timpul nașterii. În mod obișnuit, mama este sursa infecției intrauterine pentru copil, adică există un mecanism de transmitere vertical, care în perioada antenatală se realizează pe căi transplacentare sau ascendente (prin lichidul amniotic infectat), iar în perioada intranatală prin aspirație sau rute de contact.
Infecția iatrogenă a fătului apare mai rar în timpul sarcinii atunci când o femeie este supusă diagnosticului prenatal invaziv (amniocenteză, cordocenteză, biopsie vilozități coriale), introducerea produselor sanguine la făt prin vasele cordonului ombilical (plasmă, globule roșii, imunoglobuline). ), etc.
În perioada antenatală, infecția fătului este de obicei asociată cu agenți virali (rubeolă, herpes, citomegalie, virusuri hepatite B și Coxsackie, HIV) și agenți patogeni intracelulari (toxoplasmoză, micoplasmoză).
În perioada intranatală, are loc mai des contaminarea microbiană, a cărei natură și amploare depind de peisajul microbian al canalului de naștere al mamei. Dintre agenții bacterieni, cei mai des întâlniți sunt enterobacterii, streptococi de grup B, gonococi, Pseudomonas aeruginosa, Proteus, Klebsiella etc. Bariera placentară este impenetrabilă pentru majoritatea bacteriilor și protozoarelor, totuși, dacă placenta este deteriorată și se dezvoltă insuficiență fetoplacentară, prenatală. poate apărea infecție microbiană (de exemplu, cu agentul cauzal al sifilisului). În plus, infecția virală intrapartum nu poate fi exclusă.
Factorii care contribuie la apariția infecțiilor intrauterine sunt istoricul obstetric și ginecologic împovărat al mamei (colpita nespecifică, endocervicita, BTS, salpingoforită), cursul nefavorabil al sarcinii (amenințare de avort spontan, gestoză, desprinderea prematură a placentei) și morbiditatea infecțioasă a femeii pregnante. . Riscul de a dezvolta o formă manifestă de infecție intrauterină este semnificativ mai mare la copiii prematuri și în cazurile în care o femeie este infectată în principal în timpul sarcinii.
Severitatea manifestărilor clinice ale infecției intrauterine este influențată de momentul infecției și de tipul de agent patogen. Deci, dacă infecția apare în primele 8-10 săptămâni de embriogeneză, sarcina se termină de obicei cu avort spontan. Infecțiile intrauterine care apar la începutul perioadei fetale (înainte de 12 săptămâni de gestație) pot duce la nașterea mortii sau formarea de malformații grosolane. Infecția intrauterină a fătului în al doilea și al treilea trimestru de sarcină se manifestă prin afectarea organelor individuale (miocardită, hepatită, meningită, meningoencefalită) sau o infecție generalizată.
Se știe că severitatea manifestărilor procesului infecțios la o femeie însărcinată și la făt poate să nu coincidă. Un curs de infecție asimptomatic sau minim simptomatic la mamă poate provoca leziuni severe fătului, inclusiv moartea acestuia. Acest lucru se datorează tropismului crescut al agenților patogeni virali și microbieni față de țesuturile embrionare, în principal sistemul nervos central, inima și organul de vedere.
Clasificare
Structura etiologică a infecțiilor intrauterine sugerează împărțirea lor în:
Pentru a desemna grupul celor mai frecvente infecții intrauterine, este utilizată abrevierea sindromul TORCH, care combină toxoplasmoza, rubeola, citomegalovirusul și herpesul simplex. Litera O (altele) denotă alte infecții, inclusiv hepatită virală, infecție HIV, varicela, listerioză, micoplasmoză, sifilis, chlamydia etc.).
Simptomele infecțiilor intrauterine
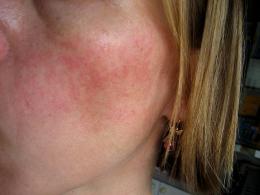
Prezența infecției intrauterine la un nou-născut poate fi suspectată deja în timpul nașterii. Infecția intrauterină poate fi indicată prin revărsarea lichidului amniotic tulbure, contaminat cu meconiu și cu miros neplăcut, precum și starea placentei (pletoră, microtroboză, micronecroză). Copiii cu infecție intrauterină se nasc adesea în stare de asfixie, cu malnutriție prenatală, mărirea ficatului, malformații sau stigmate de disembriogeneză, microcefalie, hidrocefalie. Încă din primele zile de viață se confruntă cu icter, elemente de piodermie, erupții cutanate rozoloase sau veziculoase, febră, convulsii, tulburări respiratorii și cardiovasculare.
Perioada neonatală timpurie cu infecții intrauterine este adesea agravată de pneumonie interstițială, omfalită, miocardită sau cardită, anemie, keratoconjunctivită, corioretinită, sindrom hemoragic etc. În timpul examinării instrumentale, cataracta congenitală, glaucom, malformații congenitale ale inimii și calcificari cerebrale pot fi . detectat la nou-născuți.
În perioada perinatală, copilul prezintă regurgitare frecventă și abundentă, hipotensiune musculară, sindrom de depresie a sistemului nervos central și culoarea gri a pielii. În etapele ulterioare, cu o perioadă lungă de incubație a infecției intrauterine, este posibilă dezvoltarea meningitei tardive, encefalitei și osteomielitei.
Să luăm în considerare manifestările principalelor infecții intrauterine care alcătuiesc sindromul TORCH.
Toxoplasmoza congenitala
După naștere în perioada acută, infecția intrauterină se manifestă prin febră, icter, sindrom edematos, exantem, hemoragii, diaree, convulsii, hepatosplenomegalie, miocardită, nefrită, pneumonie. În cursul subacut, domină semnele de meningită sau encefalită. Cu persistență cronică se dezvoltă hidrocefalie cu microcefalie, iridociclită, strabism și atrofie a nervului optic. Uneori apar forme monosimptomatice și latente de infecție intrauterină.
Complicațiile tardive ale toxoplasmozei congenitale includ retardul mintal, epilepsia și orbirea.
Rubeola congenitală
Infecția intrauterină apare din cauza rubeolei în timpul sarcinii. Probabilitatea și consecințele infecției fetale depind de vârsta gestațională: în primele 8 săptămâni riscul ajunge la 80%; Consecințele infecției intrauterine pot include avortul spontan, embriopatia și fetopatia. În al doilea trimestru, riscul de infecție intrauterină este de 10-20%, în al treilea – 3-8%.
Bebelușii cu infecție intrauterină se nasc de obicei prematur sau cu greutate mică la naștere. Perioada neonatală se caracterizează printr-o erupție hemoragică și icter prelungit.
Infecție herpetică congenitală
Infecția cu herpes intrauterin poate apărea într-o formă generalizată (50%), neurologică (20%), mucocutanată (20%).
Infecția herpetică congenitală intrauterină generalizată apare cu toxicoză severă, sindrom de detresă respiratorie, hepatomegalie, icter, pneumonie, trombocitopenie, sindrom hemoragic. Forma neurologică a herpesului congenital se manifestă clinic prin encefalită și meningoencefalită. Infecția cu herpes intrauterin cu dezvoltarea sindromului pielii este însoțită de apariția unei erupții veziculoase pe piele și mucoase, inclusiv organele interne. Când se dezvoltă o infecție bacteriană, se dezvoltă sepsisul neonatal.
Infecția cu herpes intrauterin la un copil poate duce la formarea de defecte de dezvoltare - microcefalie, retinopatie, hipoplazie a membrelor (nanism cortical). Complicațiile tardive ale herpesului congenital includ encefalopatia, surditatea, orbirea și dezvoltarea psihomotorie întârziată.
Diagnosticare
În prezent, diagnosticul prenatal al infecțiilor intrauterine este o sarcină urgentă. În acest scop, în stadiile incipiente ale sarcinii, se efectuează microscopia frotiului, cultura bacteriologică a vaginului pentru floră, examinarea PCR a răzuirii și examinarea complexului TORCH. Diagnosticele prenatale invazive (aspirația vilozităților coriale, amniocenteza cu examinarea lichidului amniotic, cordocenteza cu examinarea sângelui din cordonul ombilical) sunt indicate femeilor însărcinate cu risc crescut de dezvoltare a infecției intrauterine. detectează semne.
Tratamentul infecțiilor intrauterine
Principiile generale pentru tratamentul infectiilor intrauterine presupun imunoterapia, terapia antiviral, antibacteriana si sindromica.
Imunoterapia include utilizarea de imunoglobuline polivalente și specifice, imunomodulatoare (interferoni). Terapia antivirală direcționată se efectuează în principal cu aciclovir. Pentru terapia antimicrobiană a infecțiilor bacteriene intrauterine se folosesc antibiotice cu spectru larg (cefalosporine, aminoglicozide, carbapeneme) pentru infecții cu micoplasme și chlamidie, macrolide;
Terapia sindromică a infecțiilor intrauterine are ca scop ameliorarea manifestărilor individuale ale leziunilor sistemului nervos central perinatal, sindromului hemoragic, hepatitei, miocarditei, pneumoniei etc.
vaccinări împotriva rubeolei, trebuie vaccinat cu cel mult 3 luni înainte de sarcina preconizată. În unele cazuri, infecțiile intrauterine pot fi baza pentru artificialInfecția fătului în timpul dezvoltării în corpul unei femei însărcinate poate duce la diferite boli infecțioase, unite prin denumirea comună - infecție intrauterină Un copil se poate infecta o dată
agenți patogeni personali ai bolilor infecțioase în timpul nașterii (la trecerea printr-un canal de naștere infectat) sau după naștere (prin laptele matern și alte fluide biologice). Bolile infecțioase care s-au dezvoltat ca urmare a acestor motive se numesc infecții neonatale (intra și postnatale). Mulți nou-născuți care se infectează în timpul sau după naștere pot fi asimptomatici. Cu toate acestea, unii dintre ei, în special copiii prematuri, dezvoltă manifestări clinice severe ale bolii. Infecțiile perinatale sunt boli infecțioase care apar ca urmare a infecției fătului în timpul dezvoltării intrauterine, în timpul nașterii sau după naștere.
În ultimii ani, s-a înregistrat o creștere semnificativă a frecvenței infecțiilor congenitale, predominant de etiologie virală. Infecțiile virale provoacă până la 80% din malformațiile congenitale la copii, printre ele locul principal este ocupat de leziunile sistemului nervos central, precum și defectele congenitale ale inimii și rinichilor. Numeroase date științifice indică legătura etiologică a malformațiilor congenitale la copiii cu infecții virale suferite în timpul sarcinii, sau cu transmiterea transplacentară a virusurilor de la o femeie însărcinată cu o formă persistentă de infecție.
Cele mai frecvente infecții perinatale includ herpesul, CMV, infecțiile cu parvovirus și toxoplasmă, rubeola și chlamydia. Diagnosticul și tratamentul în timp util al acestor infecții la femei este o problemă urgentă în practica clinică modernă.
Examinarea virologică a nou-născuților și femeilor însărcinate face posibilă diagnosticarea unei infecții virale la marea majoritate a celor examinați (până la 98%).
Diagnosticul precoce și în timp util al infecției virale la femeile însărcinate și al infecției congenitale la copii ne permite să dezvoltăm tactici optime de management terapeutic și să folosim rațional medicamentele antivirale pentru a reduce probabilitatea defectelor de dezvoltare la copii.
Dacă se suspectează o infecție intrauterină, femeile însărcinate sunt cel mai adesea examinate pentru prezența markerilor de herpes, CMV, parvovirus, infecții cu chlamydia și toxoplasmă, precum și rubeola. Rezultatele negative ale testelor exclud în majoritatea cazurilor posibilitatea infecției fătului. Dacă există suspiciunea de infecție intra- și postnatală, este necesar să se efectueze un test de sânge paralel al mamei și al copilului. În acest caz, sunt posibile diverse situații care cauzează dificultăți medicilor la interpretarea rezultatelor. Cele mai comune dintre ele sunt date în tabel.
Atunci când se utilizează datele din tabel în evaluare, este necesar să se țină cont de faptul că detectarea numai a anticorpilor IgG la un nou-născut nu este foarte informativă din cauza pătrunderii transplantante a anticorpilor materni în corpul său în timpul dezvoltării intrauterine. Prin urmare, pentru a exclude infecția, este necesar să se determine dinamica anticorpilor IgG la un copil la 1, 3, 6 și 11-12 luni, iar când apar semne clinice ale bolii, se utilizează metode de detectare directă a agentului patogen (PCR). , detectarea Ag prin RIF sau ELISA).
În unele cazuri, la examinarea nou-născuților pentru prezența infecțiilor intrauterine, este posibil un rezultat serologic fals negativ.
studii datorită influenței unei concentrații mari de anticorpi materni din clasa IgG, „mascarea” prezenței anticorpilor IgM la copil sau toleranței imunologice (incapacitatea organismului de a răspunde și de a sintetiza anticorpi). În acest sens, în prezența manifestărilor clinice ale bolii, este necesar să se utilizeze metode de detectare directă a agentului patogen.
Tabel Interpretarea rezultatelor examinărilor de laborator ale mamei și copilului
Prezența anticorpilor la mamă și copil la același agent patogen(i)
Detectarea anticorpilor la mamă și absența acestora la nou-născut dacă acesta are un tablou clinic al bolii, precum și în timpul examinării unui copil născut dintr-o mamă infectată
Detectarea titrurilor mari de anticorpi IgG la un copil la scurt timp după naștere
Detectarea AT și/sau agenți patogeni (Ag) la un copil în absența AT la mamă
Titrul de anticorpi specifici IgG din serul sanguin al copilului depășește titrul de anticorpi similari la mamă (în absența anticorpilor IgM și IgA) Prezența anticorpilor IgM și/sau IgA (pentru chlamydia) la copil Aspectul IgM și/ sau anticorpi IgA (pentru chlamydia) împreună cu anticorpi IgG sau IgG numai la un copil anterior seronegativ (seroconversie)
Prezența anticorpilor IgM indică o infecție congenitală. Dacă titrul AT IgG este crescut, este necesar să se efectueze un studiu dinamic AT după 1-2 luni. Dacă este necesar, trebuie utilizate metode de detectare directă a agentului patogen (PCR, detectarea Ag prin RIF sau ELISA)
Utilizați metode de detectare directă a agentului patogen (PCR, detectarea Ag prin RIF sau ELISA) la un copil sau studiați titrul de anticorpi în timp în primul an de viață, deoarece infecția nu poate fi exclusă (poate exista toleranță imunologică la sinteza anticorpilor). Nu se produce)
Un conținut crescut de anticorpi IgG indică imunitatea pasivă primită de la mamă, mai degrabă decât o infecție congenitală. Pentru a clarifica situația, este necesar să se studieze titrul IgM AT sau să se monitorizeze dinamica IgG AT (dacă copilul nu este infectat, titrul lor scade brusc până la vârsta de 4-6 luni) Infecție intrauterină sau infecție în timpul nașterii; este posibil ca un copil să se infecteze prin laptele matern sau prin transfuzia de sânge și componentele acestuia; În unele cazuri, infecția de către personalul medical nu poate fi exclusă. Situația este posibilă la femeile care au fost tratate pentru o infecție, dacă sarcina apare în timpul tratamentului sau în primele luni după tratament. Rezultatele studiului nu pot indica faptul că copilul este infectat. Este necesar să se studieze titrul de anticorpi în timp și să se utilizeze metode de detecție directă a agentului patogen (PCR, detectarea Ag prin RIF sau ELISA) Indică faptul că copilul este infectat (anticorpii IgM nu pătrund în placentă) Indică o infecție primară
Un manual pentru medici și stagiari
Academia Medicală de Stat Iaroslavl
Secția Obstetrică și Ginecologie
Facultatea de Pregătire Avansată și Formare Profesională a Specialiștilor în Sănătate
Autori:
Doctor în științe medicale M.B.Okhapkin, Ph.D. M.V. Khitrov, I.N
(Departamentul de Obstetrică și Ginecologie al Academiei Medicale de Stat Yaroslavl - șef al departamentului Prof. M. B. Okhapkin.)
REFERENT:
Profesor asociat V.P Kiselev, șef al Departamentului de Boli Infecțioase ale Copiilor, Facultatea de Pediatrie a YSMA.
Manualul metodologic a fost aprobat de Comisia metodologică pentru învățământul postuniversitar a Academiei Medicale de Stat din Iaroslavl.
VIRUSURI.
I. Rubeola
Rubeola (Rubeola, rujeola germană) este o infecție aeriană și se transmite prin secreții nazofaringiene. Deși această boală este tipică pentru copilărie, mai mult de jumătate din toate cazurile din ultimii ani au trecut de 9 ani, iar la vârsta de 20-29 de ani, 19-31% dintre pacienți se îmbolnăvesc la vârsta de 30 de ani; sau mai vechi, 9-31%. Până la vârsta reproductivă, 75-85% dintre femei (jumătate în formă subclinică) au avut deja rubeolă și au imunitate pe viață la această boală.
Vaccinarea împotriva rubeolei a fost introdusă din 1969 și frecvența acesteia a scăzut semnificativ: la 1:100.000 din populație (conform SUA). Problema este incidența K. la femeile însărcinate în stadiile incipiente. Riscul de deformări fetale dacă mama este bolnavă în primul trimestru de sarcină este de aproximativ 20%(pana la 50% la 1 luna si 10% la 3 luni de sarcina). Deformarile posibile sunt: cataracta, ductus arteriosus permeabil, surditatea, iar in cativa ani se poate dezvolta diabetul.
Virusul este eliberat din sânge și faringe la 7-10 zile după infectare și eliberarea sa continuă timp de aproximativ 1 săptămână. Boala este însoțită de o erupție cutanată care începe pe față la 16-18 zile după infecție, artralgie, limfadenopatie și febră. Dar pentru a diagnostica boala, prezența unui tablou clinic nu este suficientă. Pentru confirmarea infecției sunt utilizate diferite teste serologice.
Reacția de inhibare a hemaglutinării(anticorpi Ig G). De la 5 la 15% dintre cei care s-au vindecat de K. au anticorpi la titruri mari: 1:256. În același timp, dovada imunității la K este un titru de 1:8-1:16. O creștere a titrului de anticorpi împotriva K în timpul unui test repetat de 4 ori sau mai mult indică o infecție acută. In ultimii ani, inhibarea hemaglutinarii a fost inlocuita de o serie de alte teste datorita acuratetei lor mai mari si a costului redus: aglutinarea latexului, anticorpii fluorescenti, hemaglutinarea pasiva, hemoliza in gel, testele imunitare enzimatica.
Un studiu cu Ig M specifică K confirmă o infecție „proaspătă” (poate dispărea din sânge în mai puțin de 4-5 săptămâni).
Administrarea imunoglobulinei G nu previne nici viremia sau boala ulterioară, ci doar ameliorează simptomele acesteia și, prin urmare, nu este recomandată după contactul cu un K. bolnav ca procedură de rutină. Doar pentru femeile care refuză să întrerupă sarcina, administrarea de Ig G poate fi o măsură de prevenire a infecției la făt.
Tabelul 1. Riscul de infecție fetală.
| Lungimea sarcinii (Săptămâni) | INFECȚIE FETALĂ (%) |
| <11 | 90 |
| 11-12 | 30 |
| 13-14 | 20 |
| 15-16 | 10 |
| > 16 | 5 |
Rezervorul infecției sunt copiii de vârstă preșcolară și primară. Vaccinarea cu un vaccin viu are ca rezultat protecția imunitară în 95% din cazuri. Persoanele vaccinate recent pot elimina virusul K, dar contactul lor cu femeile însărcinate „sensibile” la virus nu reprezintă un pericol pentru ele. Femeilor care sunt sensibile la virus (fără anticorpi) li se recomandă vaccinarea, dar este indicat să amâne sarcina cu 90 de zile. Daca insa vaccinul este administrat in timpul sarcinii, in primele 3 luni, virusul este depistat in tesuturile fetale doar in 3% din cazuri si nu provoaca deformari (1,7%). Vaccinarea este posibilă în perioada postpartum timpurie și nu reprezintă un obstacol în calea alăptării. Vaccinarea nu este recomandată pentru febră și imunosupresie.
II. Citomegalie.
Agentul cauzal este un virus care conține ADN aparținând grupului de virusuri herpetice. În prezent considerată cea mai frecventă cauză a infecției intrauterine. Conform datelor moderne, 0,5-2,5% din toți nou-născuții au virusul la naștere și alți 3-5% din toți nou-născuții îl primesc în perioada perinatală. Potențialul teratogen nu a fost stabilit. Deformări, cum ar fi cataracta sau defecte cardiace, sunt rare. Celule mari cu nuclei care conțin incluziuni, așa-numitele, caracteristice bolii. simptomul „ochi de bufniță” (patognomonic, dar rar întâlnit la indivizii infectați) este cunoscut încă de la începutul secolului al XX-lea, dar virusul în sine a fost izolat abia în 1956. După izolarea unei culturi a virusului, s-a constatat că majoritatea cazurile de infecție apar fără manifestări clinice.
Epidemiologie. Aproximativ 40% dintre femei rămân sensibile la infecția cu CMV în funcție de vârsta reproductivă: 45% dintre femeile cu un statut socioeconomic înalt și 15% cu unul scăzut. Cea mai mare seroconversie se observă la vârsta de 15-35 de ani. În fiecare an, 2% dintre femeile cu SSE ridicat și 6% cu SSE scăzut se infectează cu CMV.
Factorii de risc pentru infectia cu CMV sunt: SSE scăzut, sarcini repetate, vârstă înaintată, prima sarcină înainte de vârsta de 15 ani și numărul de parteneri sexuali. Absența factorilor de risc crește probabilitatea infecției cu CMV în timpul sarcinii: 1,6-2,2% dintre gravidele „sensibile” la CMV sunt infectate în timpul sarcinii. Contagiozitatea CMV este scăzută, astfel încât infecția necesită contact strâns cu un purtător al virusului: contact sexual, contact casnic (copii). Copiii care frecventează instituțiile preșcolare sunt infectați în proporție de 25-80% și elimină virusul timp de aproximativ 2 ani după infectare. Dacă un membru al familiei se infectează cu CMV, acesta infectează jumătate dintre membrii familiei.
In 90% din cazuri, infectia la adulti este subclinica, dar in 10% apar simptome asemanatoare mononucleozei: leuco-, limfocitoza, disfunctie hepatica, febra agitata, stare generala de rau, hepatosplenomegalie si icter. Complicațiile grave ale infecției la adulți sunt rare și se observă numai în stare de imunodeficiență sau cu imunosupresie medicamentoasă sunt mai probabil să apară la făt, în special cu o greutate mică la naștere (sub 1200,0). La persoanele bolnave, virusul este eliberat constant în mediul extern și poate prezenta un pericol de infecție pentru o lungă perioadă de timp: cu infecție intrauterină - 4 ani, cu infecție în timpul nașterii - 2 ani, la adulți este eliberat periodic (reinfecție, reactivare). , stări de imunosupresie). Femeile însărcinate cu infecție asimptomatică secretă virusul: colul uterin - 3-18%, tractul urinar - 3-9%, laptele matern - până la 27%, faringe - 1-2%, total - 2-28%. Frecvența izolării virusului crește odată cu cursul sarcinii: în primul trimestru - 2,6%, în trimestrul 3 - 7,6%. În același timp, nivelul de anticorpi împotriva CMV în sânge rămâne constant.
Infecția intrauterină cu CMV apare de obicei transplacentar, deși este posibilă și infecția ascendentă din colul uterin. Aproximativ 1% (0,5-2,5) din toți nou-născuții izolează CMV la naștere (de obicei din urină). Alți 3-5% din toți nou-născuții primesc CMV în timpul nașterii și ulterior (secreții cervicale, transfuzii transplacentare, lapte matern). Dacă mama are o infecție cu CMV în tractul genital în momentul nașterii, 30-50% dintre nou-născuți vor fi infectați. Dacă CMV este prezent în laptele matern, 2/3 dintre nou-născuți vor fi infectați în decurs de 3 luni.
Dacă mama are anticorpi împotriva CMV, infecția congenitală se observă la 1,4-1,9% dintre nou-născuți. Când o mamă este infectată cu CMV pentru prima dată în timpul sarcinii, până la 46-50% dintre fetuși sunt infectați in utero, complicațiile la nou-născut sunt mai frecvente (7-8% față de 25-35%): tulburări neuro-senzoriale - 5-13%, simptome clinice de infecție - 0- 11-18%, retard mintal - 0-13%, hipoacuzie bilaterală - 0-8%.
În ciuda frecvenței mari a CMV la mamă, nivelul de infecție la făt și nou-născut este de 3-4 ori mai mic. Cele mai grave consecințe ale infecției congenitale cu CMV se observă atunci când fătul este infectat în trimestrul I și II de sarcină. Când este infectat în al 3-lea trimestru, nou-născutul nu are simptome de infecție, dar Ig M este detectată în serul său de sânge duce la patologia sistemului nervos central și complicații neurologice, care sunt principalele consecințe infecții.
În prezența simptomelor de CMV (aproximativ 10% dintre cei infectați) la un nou-născut, mortalitatea ajunge la 20-30%, iar 90% dintre nou-născuții supraviețuitori au complicații tardive ale bolii: convulsii, diplegie spastică, atrofie a nervului optic, orbire, surditate, retard mintal. Dar la nou-născuții infectați fără simptome ale bolii (90%) sunt posibile și complicații tardive: retard mintal (microcefalie sau hidrocefalie) - 2%, surditate - 7%, coreretinită - 1%, dar mult mai rar - 10%. La jumătate dintre nou-născuții cu simptome ale bolii, este tipic, deși seamănă cu manifestările altor infecții cunoscute: hepatosplenomegalie, icter, purpură trombocitopenică, microcefalie, surditate, coreretinită, atrofie a nervului optic, calcificări ale țesutului cerebral (periventricular sau în zona subependimală), întârziere de creștere.
Diagnosticul gravidelor infectate cu CMV, de regulă, nu este diagnosticat din cauza absenței unui tablou clinic al bolii. Pentru confirmarea diagnosticului se folosesc metode serologice: hemaglutinare indirectă, imunofluorescență indirectă, imunosorbție (ELISA), demonstrând prezența seroconversiei. Deoarece cel puțin aproximativ 40% dintre adulți au anticorpi împotriva CMV, un singur rezultat nu indică relevanța infecției: veche sau „proaspătă”, acută. Prezența Ig M specifice indică infecție în următoarele 4-8 luni. Izolarea virusului în cultură (poate necesita între 2 și 6 săptămâni) nu face distincția între infecția primară și recurentă, dar izolarea virusului din urină sau colul uterin confirmă transportul asimptomatic al virusului, deoarece în timpul infecției recurente nivelul de anticorpi din corpul pacientului. nu se schimba. U nou-născuți Manifestările clinice ale infecției cu CMV, datorită nespecificității lor, nu sunt suficiente pentru diagnosticarea bolii, diagnosticul căreia necesită teste de laborator. Testele serologice sunt considerate teste auxiliare, iar izolarea virusului în cultura celulară este considerată cea mai precisă. Materialul pentru cercetare poate fi obținut din urină, nazofaringe, conjunctivă și lichidul cefalorahidian.
Diagnosticul prenatal posibil folosind ultrasunete, amniocenteză, cordocenteză. Ecografia evidențiază cel mai adesea micro- și hidrocefalie, modificări chistice sau focare de calcificare (necroză) în zona periventriculară a creierului, țesutul hepatic, placentă, restricție de creștere fetală, oligohidramnios, ascită fetală, revărsat pericardic sau pleural, intestin hipoecogen, hidrops fetal. . În sângele fetal obținut prin cordocenteză, este posibil să se detecteze un nivel crescut de Ig M specifică (sensibilitate 69%), să se detecteze anemie, trombocitopenie, hiperbilirubinemie și creșterea transaminazelor hepatice. Este posibil să se cultive AF, unde virusul este secretat de rinichii fetali și să se efectueze PCR. Dacă rezultatul testului este negativ, dar există un risc mare de infectare a mamei, se repetă după 4-8 săptămâni.
Tratament. Nu există un tratament specific. Este posibil să se utilizeze ganciclovir și foscarnet pentru retinita CMV la persoanele infectate cu HIV (SIDA). Se lucrează la un vaccin, pentru că... anticorpi la CMV, deși nu distrug virusul și nu exclud infecția intrauterină ( Majoritatea nou-născuților infectați in utero au avut mame cu anticorpi împotriva CMV), cu toate acestea reduc semnificativ riscul de infecție și consecințele sale grave pentru făt și nou-născut.
Screening pentru infecția cu CMV Nu se recomandă:
a) scump, b) majoritatea cazurilor de infecție congenitală cu CMV sunt înregistrate la femei cu anticorpi împotriva virusului, c) cel mai probabil rezultat al sarcinii complicate de infecția cu CMV este nașterea unui copil normal.
Izolarea pacienților infectați cu CMV, inclusiv nou-născuții nu este necesar. Este necesar să ne limităm la măsuri standard pentru a controla răspândirea bolilor infecțioase.
III. Varicela zoster (varicela).
Agentul cauzal este un virus care conține ADN din grupul herpesului. Se referă la infecțiile din „copilărie”. Este foarte contagioasă, dar apare la majoritatea populației (mai mult de 90%) înainte de vârsta reproductivă. Leziunile cutanate tipice sunt caracteristice: o erupție maculopapulară, care se transformă într-o erupție veziculoasă, apoi într-o erupție pustuloasă cu formare de cruste și zgârieturi. Procesul este autolimitat. Boala la adulți este reactivarea unei infecții virale latente, manifestată printr-o erupție veziculoasă dureroasă de-a lungul nervilor, caracteristică vârstnicilor și stărilor de imunosupresie.
Calea de răspândire este prin aer; este necesar un contact apropiat pentru infecție. Perioada de incubație este de 10-20 de zile (13-17). La copii, hipertermia și erupția cutanată apar simultan. La adulți, starea de rău și hipertermia apar cu câteva zile înainte de erupție. Erupția începe pe față și pe cap, se extinde pe trunchi și afectează rar extremitățile. Dezvoltarea sa este însoțită de mâncărime. Noi erupții apar după 2-5 zile, toate elementele erupției există simultan.
Contagiozitate: cu 1-2 zile înainte de erupție și până când crustele cad. Complicațiile includ infecția bacteriană secundară a pielii, precum și encefalita, meningita, miocardita, glomerulonefrita și artrita (rar). O complicație foarte gravă este pneumonia, care crește riscul de mortalitate: la adulți până la 5-10%, la copii - mai rar. Radiografia toracică arată infiltrate nodulare peribronșice larg răspândite și posibile semne de detresă respiratorie.
Incidența în rândul gravidelor este scăzută: 0,5-0,7 cazuri la 1000. Femeile însărcinate nu se îmbolnăvesc mai des sau mai grav decât femeile care nu sunt însărcinate, dar cu pneumonie (9-22%) rata mortalității poate ajunge la 14-30- 42%. Tratamentul este cu aciclovir 10-15 mg/kg IV * de 3 ori pe zi timp de 7 zile, sau 800 mg * de 5 ori per os.
La 2/3 dintre gravidele care neagă că au avut varicela în trecut, sunt detectați anticorpi împotriva virusului. În cazurile în care istoricul este neclar, anticorpii sunt detectați în 90%. Dacă există un contact cunoscut între o femeie însărcinată și un pacient cu V., este necesar să se determine prezența anticorpilor împotriva virusului (ELISA, ELISA). În absența acestora, este necesară administrarea imunoglobulinei specifice în 96 de ore de la contactul existent: 125 UI / 10 kg greutate corporală (până la 625 UI) IM.
Pentru prima dată, deteriorarea fătului în boala unei femei gravide a fost descrisă de LaForet și Lynch în 1947. Cu boala la începutul sarcinii, sunt descrise avorturi, nașteri morti și deformări: cicatrici ale pielii, hipoplazie a extremităților, atrofie a cortexul cerebral, retard mental, retard de creștere, microftalmie, cataractă. Deformările sunt foarte rare: aproximativ 1%, dar mortalitatea nou-născutului în aceste cazuri ajunge la 25%. Prin examinarea diferitelor părți ale ovulului, este posibil să se identifice virusul V. la făt, dar este imposibil să se determine cu exactitate amploarea leziunii sale. Metoda optimă de evaluare a posibilelor consecințe ale infecției este ecografia înainte de 20 de săptămâni de sarcină, unde este posibilă identificarea prezenței polihidramniosului, hidropsului fetal, focarelor hipoecogene în ficat, deformări ale membrelor, care însoțesc adesea leziuni ale sistemului nervos central fetal.
Anticorpii materni (Ig G), chiar dacă seroconversia a avut loc în timpul sarcinii, protejează fătul. Cel mai mare risc de îmbolnăvire la un nou-născut există atunci când mama este infectată cu 2 zile înainte de naștere și în decurs de 5 zile după naștere. Când mama este infectată cu 4-5 zile înainte de naștere, nivelul infecției congenitale la nou-născuți este de 10-20%, iar mortalitatea este de 20-30%. Când mama a fost infectată cu mai mult de 5 zile înainte de naștere, nou-născuții s-au născut cu forme ușoare de infecție sau fără manifestări ale acesteia. Dacă nașterea unei gravide infectate nu poate fi amânată cu 5-7 zile, imediat după naștere este necesară imunizarea pasivă a nou-născutului: 125 UI IM. Imunizarea nu protejează un nou-născut de infecție (până la 60% se infectează), dar previne moartea bolii. Există o opinie despre necesitatea imunizării unui nou-născut dacă mama este infectată în timpul săptămânii înainte și după naștere.
Se dezvoltă un vaccin pentru copiii mici. Utilizarea sa va face posibilă încetarea virusului V. ca sursă de morbiditate pentru gravide. Herpes zoster, fiind o reactivare a unei infecții latente în prezența anticorpilor la virusul B, nu reprezintă o amenințare pentru sănătatea fătului și a nou-născutului.
IV. Rujeola (rubeola).
Agentul cauzal este un virus care conține ARN aparținând paramixovirusurilor. Boala este caracteristică copilăriei și este cea mai contagioasă dintre toate infecțiile din copilărie însoțite de o erupție cutanată. Manifestări clinice: hipertermie, conjunctivită, tuse, erupții cutanate maculopapulare, care apar de obicei la 1-2 zile după apariția petelor patognomonice Koplik-Filatov în cavitatea bucală. Transmis prin picături în aer. Perioada de incubatie: 10-14 zile, cea mai mare contagiositate este in timpul prodromului si stadiul fenomenelor catarale (3/4 din cei in contact cu pacientul se imbolnavesc). Creșterea incidenței K. are o frecvență de 2-3 ani (înainte de începerea vaccinării). Vaccinul viu împotriva rujeolei este folosit din 1963. Complicațiile posibile sunt otita medie, crupa, encefalita (1:1000), miocardita. Incidenţa K. în rândul femeilor însărcinate este scăzută. Înainte de vaccinare, era 0,4-0,6/10.000. Complicațiile sunt rare la femeile însărcinate, cea mai periculoasa din punct de vedere al mortalitatii este pneumonia bacteriana.
Pentru fat, riscul de complicatii (avort, malformatii) nu a fost dovedit sau este foarte mic. Dacă există manifestări clinice ale rujeolei la un nou-născut în primele 10 zile de viață, infecția trebuie considerată congenitală dacă manifestările clinice ale bolii apar în a 14-a zi sau mai târziu, aceasta trebuie considerată dobândită postnatal. În cazul rujeolei congenitale, rata mortalității nou-născuților la termen înainte de utilizarea antibioticelor a fost de 20-30% (prematur - 56%). Cu terapia cu antibiotice și metodele moderne de resuscitare, mortalitatea este semnificativ mai mică.
Tratamentul pentru K. necomplicat este simptomatic pentru otita medie, pneumonie, trebuie prescrise antibiotice, ținând cont de flora sensibilă; Pentru prevenirea bolii la gravidele și nou-născuții nebolnavi se utilizează imunizarea pasivă: globulină serică imună (rujeolă) în doză de 0,25 ml/kg greutate corporală în decurs de 6 zile de la contact. Pentru nou-născuții născuți din mame care au contractat rujeolă cu 1 săptămână înainte sau după naștere, se recomandă imunizarea în aceeași doză. Deși există doar un risc teoretic pentru făt, nu se recomandă utilizarea vaccinului viu în timpul sarcinii sau cu 3 luni înainte de concepție (perioada minimă de la vaccinare până la sarcină este de 1 lună).
V. Porc.
Agentul cauzal este un virus din același grup cu agentul cauzal al rujeolei. Infecție generalizată acută cu afectare predominantă a parotidei și a altor glande salivare, în plus, pot fi afectate creierul, pancreasul și gonadele. Calea de transmitere a bolii este prin aer: prin picături de salivă. Virusul este izolat din salivă cu 7 zile înainte de apariția oreionului și timp de 9 zile după. Perioada de incubație: 14-18 zile. În cea mai mare parte, copiii sub 15 ani sunt afectați după această vârstă, se înregistrează doar 10% din cazurile de boală. O treime dintre adulți sunt imuni la boală ca o consecință a infecției clinice sau subclinice. Oreionul este mai puțin contagios decât varicela sau rujeola, dar este mai frecvent în rândul femeilor însărcinate: 0,8-10/10.000. Prodromul se manifestă sub formă de febră, stare de rău, mialgii, anorexie. După 24 de ore apar simptome de oreion, adesea bilaterale. Glandele submandibulare sunt afectate mai rar și întotdeauna cu oreion. Glandele sublinguale sunt rareori afectate. De obicei, boala nu provoacă complicații și se termină de la sine. Dar ocazional sunt încă posibile complicații: ooforită, meningită aseptică (întotdeauna cu rezultate favorabile), precum și pancreatită, mastită, tiroidita, miocardită, nefrită, artrită. La femeile însărcinate, infecția este ușoară și nu diferă de cursul la femeile care nu sunt însărcinate.. La contractarea oreionului în primul trimestru de sarcină, s-a observat o creștere de 2 ori a numărului de avorturi spontane. Nivelul de prematuritate, restricție de creștere fetală și mortalitate perinatală nu se modifică. Conexiune boli cu fibroelastoză endocardică a nou-născuților, cu anomalii congenitale de dezvoltare este considerată nedovedită. Diagnosticul se face pe baza manifestărilor clinice dacă tabloul clinic este neclar, sunt necesare izolarea virusului sau, mai des, teste serologice: fixarea complimentă, inhibarea hemaglutinării, titrul de anticorpi neutralizanți în seruri pereche (infecție acută - recuperare); . Tratamentul este simptomatic. Întreruperea sarcinii nu este necesară. Vaccinarea cu un vaccin viu este posibilă (95% dintre cei vaccinați dezvoltă anticorpi împotriva virusului). Durata protecției ulterioare împotriva infecției nu a fost stabilită. Deși riscul pentru făt este doar teoretic, imunizarea cu vaccin viu nu este recomandată în timpul sarcinii.
VI. Gripa (gripa).
Agentul cauzal este un mixovirus. Pe baza compoziției lor antigenice, se disting trei tipuri de virus. Tipul A este cauza celor mai multe epidemii și a celor mai severe cazuri de boală. Tipul B este mai puțin probabil să provoace epidemii și se caracterizează prin forme ușoare ale bolii. Tipul C este cel mai rar agent patogen.
Frecvența și severitatea bolii sunt asociate cu modificări ale structurii antigenice a virusului. Schimbările semnificative care apar la intervale de 10-30 de ani duc la o evoluție severă a infecției, modificări minore anuale în structura antigenică a virusului nu au astfel de consecințe. Perioada de incubație durează 1-4 zile. Manifestările clinice încep brusc și durează aproximativ 3 zile. Diagnosticul este confirmat prin izolarea virusului din tampoane faringiene (perioada acută) sau o creștere de 4 ori a titrului de anticorpi în seruri pereche: perioadă acută - convalescență. Pot fi efectuate teste de fixare a complementului sau de inhibare a hemaglutinării.
Cea mai periculoasă complicație la femeile însărcinate este pneumonia care pune viața în pericol. Conform datelor obținute în timpul epidemilor din 1918 și 1957, femeile însărcinate constituiau cel mai mare grup dintre cei care au murit de gripă. Mortalitatea maternă prin gripă în timpul pandemiei din 1918 a fost de aproximativ 30%, iar în cazurile complicate de pneumonie - până la 50%. În timpul pandemiei din 1957, până la 50% din toate decesele gripale au avut loc la femei însărcinate.
Efectul asupra fătului este neglijabil. Informațiile despre deformările fetale sunt contradictorii: acolo unde se constată o legătură cu deformările fetale, acestea sunt cel mai probabil să apară în primul trimestru de sarcină (5,3%), iar cele mai frecvente sunt defectele cardiace. Dar o serie de studii neagă legătura dintre gripă și anomaliile fetale. Același lucru este valabil și pentru alte complicații ale sarcinii. Majoritatea femeilor însărcinate care fac gripă au un rezultat perinatal normal.
Tratamentul gripei este simptomatic, cu semne de pneumonie, care este mai severă la femeile însărcinate, necesitând spitalizare și terapie cu antibiotice. Utilizarea amantadinei în timpul sarcinii nu este recomandată, deoarece efectul său teratogen a fost observat la animale. Este posibil să se vaccineze cu preparate virale ucise, care sunt sigure pentru femeile însărcinate și la fel de eficiente ca și în afara sarcinii.
VII. Enterovirusuri
Ele sunt reprezentate de trei subgrupe de picornovirusuri care conțin ARN:
1. Poliovirusurile sunt reprezentate de virusul poliomielitei. La femeile însărcinate poate provoca avort, nașterea mortii, întârzierea creșterii fetale, iar la nou-născuți - poliomielita. Virusul poate fi transmis la făt prin placentă, dar 2/3 dintre gravidele cu manifestări clinice de poliomielita dau naștere la nou-născuți sănătoși. Nu a fost observat niciun efect teratogen pentru virusul poliomielitei.
2. Ecovirusurile, există aproximativ 33 de specii, pot provoca boli respiratorii, gastroenterite, conjunctivite, meningite și pericardite. Nu au existat complicații ale sarcinii: avorturi, nașteri premature, nașteri morti, deformări. Poate provoca infecții la nou-născuți (posibil congenitale): febră, splenomegalie, PAW, erupții cutanate, diaree, vărsături, otită medie, pneumonie, meningită, icter. Nu există tratament sau vaccin specific.
3. Virușii Coxsackie sunt reprezentați de două grupe: A (23 tipuri) și B (6 tipuri). Virușii din grupa A, cu rare excepții, nu provoacă morbiditate perinatală. Virușii din grupa B pot provoca meningoencefalită, miocardită și, rar, hepatită, pneumonie și sindrom hemolitic-uremic. Sunt posibile deformări fetale. S-a dovedit transmiterea virusului la făt prin placentă. Riscul pentru făt nu a fost determinat. Majoritatea cazurilor de infecție la mamă nu provoacă complicații ale sarcinii și trec fără consecințe pentru făt.
Diagnosticul este posibil prin izolarea virusului din faringe sau rect, înregistrarea unei creșteri a titrului de anticorpi în timpul perioadei de recuperare, teste de inhibare a hemaglutinării și fixarea complimentului.
VIII. Papilomavirus uman.
La persoanele cu citologie cervicală normală, virusul a fost izolat în 6% din cazuri, în cazurile de displazie cervicală - în 60% din cazuri. Negii genitali, care sunt o consecință a infecției, pot provoca disconfort extrem, dificultăți la defecare și urinare și pot provoca sângerări. Principala cale de transmitere este cea sexuală (contactul cu pielea), dar sunt posibile și alte căi: prin lenjerie intimă. Contagiozitatea este relativ mare. Papilomatoza respiratorie este posibilă la nou-născuți. Condiloamele în timpul nașterii au fost observate la 60% dintre mamele lor.
Cel mai adesea, infecția apare între 16-25 de ani. Perioada de incubație este de 3-8 luni. Diagnosticul se bazează pe manifestările clinice ale bolii: condiloamele au aspectul unor excrescențe moi de câțiva mm diametru, înălțimea lor este adesea mai mare decât lățimea și pot fi unice sau de grup. „Giant” K. mai rar de 3 cm în diametru se găsesc. Ele se găsesc cel mai adesea în locuri umede ale corpului: vestibulul vaginului, vaginul. Creșteri foarte mici, plate, vizibile doar în timpul colposcopiei, sunt adesea localizate pe colul uterin. Este necesar să se facă distincția între condiloamele late care apar cu sifilis (efectuați teste serologice). Formele atipice pot necesita o biopsie pentru a exclude cancerul.
Papilomatoza respiratorie la copii în 1/3-1/2 din cazuri se manifestă la vârsta de 5 ani.
Cel mai adesea sunt afectate corzile vocale, simptomul caracteristic fiind răgușeala. Pot să apară simptome de obstrucție a căilor respiratorii. În 90% din cazuri, HPV tipurile 6 și 11 sunt izolate La 60% dintre femeile ai căror copii au papilomatoză respiratorie, ADN-ul HPV este izolat. 2-5% dintre toți nou-născuții sunt expuși riscului de contact perinatal cu HPV. Dar infecția respiratorie este rară: 0,04% din toate nașterile vaginale, sau 1:80-1:1500 dacă mama are HPV. Transmiterea virusului are loc în timpul nașterii, dar este posibilă și infecția intrauterină. Riscul de a contracta HPV este de 10 ori mai mic decât virusul herpes simplex. Având în vedere raritatea transmiterii bolii, posibilitatea infecției intrauterine, Operația cezariană nu este considerată o metodă de prevenire a infecției cu HPV la nou-născuți.
Tratamentul femeilor însărcinate. Nu trebuie utilizat în timpul sarcinii podofilină (toxică, posibilă teratogeneză), podofilox 0,5%, 5-fluorouracil (intoxicație a fătului, posibile deformări la utilizarea în primul trimestru), interferoni (ineficace). Este posibilă utilizarea locală a acizilor tri- și bicloroacetici. O singură aplicare duce la vindecare doar în 20-30% din cazuri, deci sunt necesare proceduri repetate după 7-10 zile. Este posibilă combinarea cu tratamentul cu laser. Criochirurgia este utilizată pentru leziunile vulvei, vaginului și colului uterin. Pentru condiloamele mari este posibilă excizia chirurgicală în combinație cu electrocoagularea și chiuretajul.
IX. Parvovirus uman.
Se referă la virusuri care conțin ADN. Doar tipul B 19 este un agent patogen pentru oameni. Are o tendință spre sistemul hematopoietic și este toxic pentru celulele eritroide. Provoacă anemie aplastică tranzitorie, cea mai frecventă manifestare este o boală caracteristică copilăriei: eritemul infecțios (a cincea boală). S-a dovedit posibilitatea infecției intrauterine și a hidropsului fetal non-imun.
Virusul este răspândit în întreaga lume la copiii de 5-14 ani. Prezența anticorpilor împotriva virusului (Ig G) depinde de vârstă: în 1-5 ani - 2-15%, în 5-19 ani - 15-60%, la adulți - 30-60%. Aproximativ 50-75% dintre femeile de vârstă reproductivă au anticorpi împotriva virusului.
Manifestările clinice ale bolii sunt tipice pentru copilărie: se observă o creștere sezonieră a incidenței (iarnă-primăvară), clinica este „ușoară”, manifestată prin febră urmată de o erupție eritematoasă pe față („semn palmă”), răspândindu-se la membrele. La adulți, boala este adesea asimptomatică, dar sunt posibile artrita și adenopatia fără erupție cutanată. Contagiozitatea virusului este mare: până la 60-80% dintre membrii familiei care au avut contact cu pacientul sunt infectați, riscul de infectare în rândul asistenților sociali (profesori, educatori) este de 20-30%.
În afara epidemiei, rata anuală de seroconversie este de 0,42% pentru lucrătorii din domeniul sănătății și de 2,93% pentru lucrătorii din școală. În timpul unei epidemii, rata de seroconversie crește la 20-40%. Pentru o persoană, riscul de infectare la locul de muncă este de 2 ori mai mare decât atunci când sta acasă. Femeile însărcinate care nu au anticorpi împotriva virusului trebuie să evite contactul cu pacienții cu anemie hemolitică însoțită de febră sau criză aplastică.
Diagnosticare efectuate pe baza tabloului clinic, teste serologice (Ig G și Ig M prin ELISA), metodă de cultură, PCR, precum și prin identificarea modificărilor tipice în celulele precursoare de eritrocite.
Când se transmite la făt, se poate dezvolta anemie aplastică (distrugerea globulelor roșii din sânge) și, ca urmare, la 4-6 săptămâni după infectarea mamei (1-12 săptămâni) - hidrops fetal non-imun. Incidența hidropsului este de aproximativ 26%, mortalitatea fetală este de 10-16%. Dar în cele mai multe cazuri, infecția maternă nu afectează rezultatul sarcinii pentru făt. Conform unor studii recente, mortalitatea fetală în rândul gravidelor infectate a fost de 5,9%. Infecția femeilor însărcinate nu a fost însoțită de o creștere a numărului de nașteri premature, deformări fetale și o scădere a greutății sale. De aceea, Conform conceptelor moderne, riscul pentru făt atunci când mama este infectată cu parvovirus este scăzut.
Femeile care au avut contact cu paciente cu eritem infecțios în timpul sarcinii trebuie examinate cu ajutorul testelor serologice pentru prezența anticorpilor (Ig G și Ig M) la parvovirus. Dacă sunt prezenți anticorpi (imunitate), se efectuează monitorizarea de rutină. În lipsa acestora, este necesar să se avertizeze gravida împotriva posibilului contact, mai ales în timpul celei de-a cincea epidemii de boală (profesori, asistenți sociali). În absența Ig G, dar în prezența Ig M (infecție acută), este necesar să se evalueze posibilitatea dezvoltării hidrops fetalis. Este necesar să se măsoare în serie nivelul alfa-fetoproteinei la mamă (creștere înainte de dezvoltarea hidropsului), iar dacă acesta crește, se efectuează o ecografie.
Odată cu dezvoltarea hidrops fetalis, există două opțiuni pentru gestionarea unei femei însărcinate.
Primul— efectuarea transfuziei de sânge intrauterin prin cordocenteză;
al doilea— management conservator, deoarece S-a observat că hidropsul fetal dispare de la sine după 4-6 săptămâni. Este indicat să se efectueze transfuzii de sânge la fetuși cu o vârstă gestațională de până la 20-22 de săptămâni, când există riscul decesului fetal intrauterin. Fetușii mai în vârstă, cu un sistem imunitar mai dezvoltat funcțional, sunt mai capabili să tolereze infecția cu parvovirus, ceea ce permite gestionarea conservatoare a sarcinii.
Nu există tratament sau vaccin împotriva infecției cu parvovirus. Singura metodă de prevenire este evitarea contactului cu pacientul.
Riscul de deces fetal la gravidele cu status serologic neclar este de 1:500-1:4000. Dincolo de epidemie riscul de efecte adverse asupra fătului este atât de scăzut încât screening-ul serologic și modificarea stilului de viață pentru femeia însărcinată nu sunt necesare. Dar în timpul unei epidemii, când nivelul de infecție crește de 5-20 de ori, aceste măsuri sunt justificate, mai ales pentru grupurile cu risc de îmbolnăvire: asistente medicale, profesori de școală primară, lucrători din spitale unde se tratează pacienții cu anemie aplastică, persoane de la domiciliu. mediul unui copil bolnav. Pentru majoritatea femeilor, sursa de infecție este un copil bolnav de vârstă școlară acasă.
X. INFECȚIA HIV ÎN TIMPUL SARCINII
Efectul sarcinii asupra evoluției infecției cu HIV rămâne neclar. Pe de o parte, există dovezi ale unei accelerări a progresiei bolii în timpul sarcinii: intervalul de la infecție la manifestările SIDA se reduce de la 6 ani la 2-4 ani. Pe de altă parte, nu există diferențe semnificative în ceea ce privește mortalitatea și incidența SIDA la femeile care au și nu au avut o sarcină.
Când s-au studiat rezultatele sarcinii la femeile însărcinate infectate cu HIV, fără SIDA, nu s-au dovedit a fi semnificativ diferite de rezultatele sarcinii la femeile neinfectate. Au fost observate spitalizări mai frecvente pentru pneumonie bacteriană. În același timp, în prezența SIDA, când numărul de celule DM 4 (+) devine mai mic de 30%, se înregistrează mai des nașterea prematură, nașterea mortii, greutatea fetală mică, corioamnionita și endometrita postpartum. În general, cu cât boala este mai gravă, cu cât stadiul ei este mai înalt, cu atât sunt mai probabile complicațiile sarcinii.
Transmiterea verticală a HIV este un fapt stabilit. Dar ceea ce rămâne neclar este timpul, frecvența transmiterii și factorii determinanți ai acesteia. În timpul avorturilor la femeile infectate cu HIV, infecția fetală a fost observată la 17%. Are loc transmiterea HIV de la mamă la nou-născut: a) transplacentar, b) în timpul nașterii, prin inoculare sau ingestia de sânge sau lichid amniotic infectat, c) după naștere prin laptele matern. Dacă un nou-născut are semne de infecție cu HIV în primele zile și săptămâni de viață (cultură, PCR, serologie), atunci cel mai probabil infecția a avut loc antenatal (aproximativ 50%). Dacă HIV este depistat în zilele 7-90 de viață și nu există alăptare, trebuie presupus că transmiterea virusului a avut loc în timpul nașterii. Conform datelor actuale, nivelul transmiterii HIV perinatale este de 20-50%. A existat o probabilitate mai mare de infecție la primul făt la gemeni (25% față de 8%). Calea principală în transmiterea verticală este calea de transmitere a virusului în timpul nașterii (50-60%). Operația cezariană nu oferă protecție fiabilă fătului împotriva infecției cu HIV.
A treia modalitate de transmitere a virusului unui nou-născut este alăptarea, care dublează riscul de infectare cu HIV. Mamele care au primit virusul printr-o transfuzie de sânge infectat au un număr semnificativ mai mare de particule ale acestuia în sânge și lapte și reprezintă un pericol mai mare pentru nou-născut decât mamele cu o infecție cronică și asimptomatică. Dacă aveți SIDA, probabilitatea de infecție prin laptele matern crește semnificativ. Se crede că dacă hrănirea artificială este posibilă, o femeie infectată cu HIV aflată în travaliu nu ar trebui să-și alăpteze copilul. Trebuie remarcat faptul că HIV este sensibil la căldură, astfel încât încălzirea laptelui matern reduce riscul de infecție.
Detectarea nou-născuților infectați cu HIV până la 18 luni de viață este posibilă numai prin determinarea antigenului p24 folosind PCR sau cultură, deoarece IgG primite de făt de la mamă pot fi detectate în sângele acestuia până la 15 luni după naștere. Utilizarea IgA neutră placentară este semnificativ mai puțin precisă decât metodele de mai sus.
Factorii de transmitere HIV sunt: stadiul bolii, viremie în timpul infecției acute, număr de limfocite DM 4 (+) (cu un număr de limfocite mai mic de 500 celule/μl și antigenemie, probabilitatea transmiterii virusului crește de 10 ori), livrare înainte de 34 de săptămâni, metodă de naștere (operația CS reduce probabilitatea de transmitere, dar pentru a preveni un caz de infecție perinatală, este necesar să se opereze 16 femei în travaliu), afectarea pielii capului fetal, hipertermie la femeia în travaliu. Tratamentul antiviral reduce rata de transmitere perinatală. Dar cel mai bun mod de a reduce transmiterea perinatală a HIV este prevenirea infectării femeilor.
MANAGEMENTUL FEMEIILOR CU HIV CU HIV. Toate femeile care plănuiesc să rămână însărcinate ar trebui să fie testate pentru HIV. Este important să se acorde atenție factorilor de risc: parteneri dependenți de droguri, antecedente de transfuzii de sânge, ITS cu leziuni ulcerative la nivelul organelor genitale. Dar mai mult de 50% dintre femeile infectate cu HIV nu au factori de risc. Atunci când este detectată infecția cu HIV, este necesară o consultare detaliată cu pacienta în fazele incipiente ale sarcinii, este indicat să discutăm despre posibilitatea întreruperii acesteia.
Activități necesare:
— acordați atenție posibilelor manifestări ale infecției cu HIV sub formă de boli ale diferitelor organe: PAW, pneumonie, sarcom Kaposi, mărire a ficatului și a splinei.
— identificarea posibilelor ITS: sifilis, chlamydia, hepatita B, herpes, anticorpi la CMV și toxoplasmă (titrul inițial pentru diagnosticul ulterior de recădere).
— depistarea tuberculozei (o papulă egală sau mai mare de 5 mm este considerată un test pozitiv).
- examen citologic al colului uterin pentru prezența modificărilor maligne ( frotiu cu colorație Papanicolaou).
— controlul stării imunologice: determinarea numărului de limfocite T (DM 4 și DM 8).
— este utilă numărarea celulelor sanguine, trombocitelor, VSH, teste ale funcției hepatice, monitorizarea creșterii imunoglobulinelor în serul sanguin.
Tratament. Primul medicament înregistrat pentru tratamentul infecției cu HIV a fost ZIDOVUDINE (azidotimidină). La gravide, Z. pătrunde rapid în placentă, iar farmacodinamia sa nu diferă de cea a femeilor care nu sunt însărcinate. Același lucru este valabil și pentru dozele de medicamente. Zidovudina este relativ sigură pentru făt: nivelul deformărilor (2%) nu depășește faptul că în populația generală nu au fost observate semne de hematointoxicație. Poate exista o ușoară creștere a numărului de nou-născuți cu anemie și semne de RCIU. În stadiile incipiente ale bolii, Z. reduce transmiterea verticală a HIV de 3 ori (25,5% și 8,3%).
Tratamentul gravidelor cu zidovudină.
| NUMĂR DE SD 4 (+) CL. | TACTICA | RE-TESTARE |
| mai mult de 600 / µl (mm 3) | tratamentul nu este indicat | h/w 6 luni |
| 500 – 600 / µl | tratamentul poate fi discutat, observația întărită | h/w 3 luni |
| 300 – 500 / µl | Luați în considerare tratamentul; acesta poate fi amânat până după sarcină. Consultație cu un specialist în boli infecțioase. | h/w 6 luni |
| 200 – 300 / µl | este indicat prevenirea infectiei cu Pneumocystis cu trimetoprim. Creșteți supravegherea. | h/w 3 luni |
| mai puțin de 200/µl | tratamentul Z. şi prevenirea infecţiei cu pneumocystis | depinde de o situație |
Regimul de tratament aproximativ pentru Z. în timpul sarcinii 14-34 de săptămâni şi DM4 (+) mai mult de 200/pl: 100 mg 5 r. pe zi per os, în timpul travaliului - 2 mg/kg IV timp de 1 oră, apoi 1 mg/kg/oră IV până la naștere. Nou-născuți: 2 mg/kg la fiecare 6 ore pe cale orală timp de 6 săptămâni.
Management în timpul nașterii. Livrarea este conservatoare. K.S. pentru a reduce riscul transmiterii perinatale – nerecomandat. Utilizarea pensei obstetricale si extractia vacuum creste riscul transmiterii perinatale a virusului.
După naștere .
Măsurile de precauție de mai sus. Nou-născutul rămâne cu mama. Conform celor mai recente date, nivelul complicațiilor infecțioase postpartum la femeile postpartum infectate cu HIV nu îl depășește pe cel al femeilor neinfectate. Când îngrijiți un nou-născut, folosiți mănuși, spălați-vă des pe mâini, evitați intervențiile chirurgicale și nu vaccinați cu un vaccin viu până când nu se confirmă faptul că a fost infectat. Monitorizați prezența și nivelul anticorpilor HIV: până când aceștia dispar sau până la 15 luni de viață. Izolarea unei culturi virale, datele PCR pozitive sau prezența unui antigen sunt dovezi ale infecției cu HIV la orice vârstă.
BACTERII
I. SIFILIS (aspecte perinatale).
Jumătate din cazurile de sifilis congenital sunt observate la mamele care nu au avut supraveghere medicală prenatală. Spirochetele pătrund în făt în orice stadiu al sarcinii și nu după 16-18 săptămâni, așa cum se credea anterior, dar în primele etape ale sarcinii nu se observă modificări la făt din cauza lipsei unui răspuns imun. Principalii factori care determină riscul de infecție fetală sunt concentrația de spirochete în sângele mamei și stadiul bolii. Cu sifilisul netratat cu o durată a bolii mai mică de 2 ani, 50% dintre nou-născuți se nasc normali, 38% au sifilis congenital, 8,7% sunt născuți morți, 4,4% mor în decurs de 2 luni de la naștere. Pentru sifilisul netratat cu o durată a bolii de 2-5 ani, aceste cifre sunt respectiv: 75% -14% -7% -4%. Pentru sifilisul netratat cu o durată a bolii mai mare de 5 ani după 3 luni de viață, respectiv: 81% -6% -6% -7% (1937).
Conform datelor mai moderne (1952) primar si secundar sifilisul netratat în jumătate din cazuri duce la nașterea mortii, prematuritatea sau moartea nou-născutului. O altă jumătate din cazuri au sifilis congenital. La latentă timpurie sifilis, prematuritatea a fost de 20%, nașterea mortii -16%, mortalitatea nou-născutului -4%, sifilisul congenital -40%. Doar 20% dintre nou-născuți s-au născut fără abateri de la normă. La sifilis tardiv La mamă, sifilisul congenital a fost de numai 10% nu a existat o creștere a prematurității și a mortalității perinatale.
Cercetările din anii 1980 au confirmat efectele adverse ale sifilisului asupra rezultatelor sarcinii. Cu sifilisul congenital, rata nașterii mortii a fost de 35%, iar rata mortalității perinatale a fost de 46,4% (1989). În același timp, prematuritatea și întârzierea creșterii intrauterine, ajungând la 21%, rămân o complicație frecventă a sarcinii.
Manifestari clinice sifilisul la femeile însărcinate nu diferă de cel la femeile care nu sunt însărcinate. Marea majoritate a gravidelor cu sifilis nu prezintă simptome ale bolii, care se află în faza latentă, iar durata acesteia este mai mare de 1 an. Sifilisul congenital are două faze. Cu S. congenital precoce, manifestările clinice ale bolii apar în primul an de viață. Cu S. congenital tardiv, simptomele apar dupa 2 ani de viata.
Cu sifilisul congenital precoce, nou-născuții nu au de obicei simptome ale bolii, ale căror singure semne sunt testele serologice pozitive. După 2-6 săptămâni apar leziuni cutanate care seamănă cu cele ale S. secundare: sunt localizate în zona anogenitală, pe picioare și palme. O erupție maculopapulară este tipică, dar sunt posibile erupții veziculoase și buloase, ceea ce nu este tipic la adulți. Mai frecvente sunt hemoragiile punctiforme ale mucoaselor și condiloamele late, care dau un rezultat pozitiv pentru treponem atunci când sunt examinate într-un câmp întunecat. Se observă rinită cu secreție mucoasă purulentă și congestie nazală. Sunt foarte frecvente crăpăturile pe buze și zona anogenitală care, la vindecare, formează cicatrici. La vârsta de 4 luni, sunt posibile osteocondrita (pseudoparalizia lui Parro), osteita și periostita oaselor lungi. Aproximativ 2/3 dintre nou-născuții cu S. congenital precoce au hepatosplenomegalie și aproximativ jumătate au simptome de meningită. În plus, cu sifilisul congenital precoce pot fi detectate anemie, febră, PAP, pneumonie „albă”, irită și nasul de șa.
Pentru congenital tardiv S. se caracterizează prin două grupe principale de simptome. Primul grup (stigmate sifilitice) include manifestări de S. care sunt rezultatul cicatrizării manifestărilor S. precoce sau tulburări de dezvoltare cauzate de acesta: perforarea septului nazal, nasul șei, îngroșarea oaselor frontale, dinții lui Hutchinson (crestătură). pe incisivii permanenți), molari sub formă de dude, tibie, cicatrici (buze, anus). Al doilea grup de simptome este rezultatul inflamației active în curs: cheratită interstițială, neurosifilis, surditate neuronală, hidrartroză bilaterală, gume.
Diagnosticare S. se realizează după principii generale. S congenital precoce. trebuie suspectat la orice nou-născut cu hidrops de origine necunoscută, placentă mare, rinită persistentă (muci), erupție cutanată persistentă cu model, icter inexplicabil cu hepatosplenomegalie sau anemie. Leziunile pielii, mucoaselor și secrețiilor nazale care conțin spirochete trebuie verificate pentru prezența lor în timpul examinării în câmp întunecat. Cu S. congenital târziu. Manifestări tipice suficiente pentru diagnosticul său sunt triada lui Hutchinson (dinți, cheratită interstițială, surditate prin afectarea celei de-a 8-a perechi de nervi cranieni), o formă specială de molari și hidrartroză. Diagnosticul final se pune atunci când spirochetele sunt detectate în timpul examinării în câmp întunecat sau al examenului histologic.
Pentru un diagnostic prezumtiv este necesar: a) rezultate pozitive crescătoare sau de lungă durată ale testelor serologice, b) teste serologice pozitive în prezența scurgerii nazale, condiloame late, leziuni osoase, c) teste serologice pozitive în prezența a două sau mai multe manifestări clinice ale S.: hepatosplenomegalie , PAP, anemie, hidrops fetal non-imun, leziuni ale pielii și mucoaselor, pseudoparalizia papagalului, glomerulonefrita, afectarea sistemului nervos central.
Diagnostic probabil (suspiciune de S.) este plasat în prezența unor teste serologice pozitive în absența manifestărilor clinice ale S. Deoarece testele serologice pozitive pot reflecta prezența anticorpilor materni în sângele nou-născutului, este necesar să se efectueze studii în serie (o creștere a titrului sau persistența sa confirmă prezența S. congenital) sau determinarea Ig M specifice.
Tratament. Penicilina este medicamentul de elecție pentru tratamentul atât al femeilor însărcinate, cât și al celor care nu sunt însărcinate. Fiecare nou-născut cu suspiciune de S. congenital trebuie să fie supus unei pungii spinării înainte de tratament. Dacă datele de examinare a lichidului cefalorahidian se încadrează în limite normale, se administrează o injecție intramusculară de penicilină benzatină în doză de 50 mii unități/kg. Dacă rezultatele sunt patologice sau nu există puncție, nou-născutului trebuie să i se prescrie o soluție apoasă de penicilină cristalină: 50 mii unități/kg/zi timp de 10 zile.
Tratamentul femeilor însărcinate
Sifilis precoce(primar, secundar și latent cu durata bolii mai mică de 1 an):
Penicilină benzatină G 2,4 milioane de unități. intramuscular, o injecție
Pe durata bolii mai mult de 1 an:
Penicilină benzatină G 2,4 milioane de unități. intramuscular săptămânal, trei injecții
Neurosifilis:
Soluție apoasă de penicilină cristalină G 2-4 milioane de unități. intravenos după 4 ore timp de 10-14 zile, urmată de o injecție intramusculară de benzatină penicilină G în doză de 2,4 milioane de unități. sau
Soluție apoasă de procaină penicilină G 2,4 milioane de unități. intramuscular zilnic cu probenecid 500 mg de 4 ori pe zi per os timp de 10-14 zile, urmată de o injecție intramusculară de benzatină penicilină G în doză de 2,4 milioane de unități.
II. LISTERIOZA.
Infecția este cauzată de bacteria Listeria monocytogenes: o baghetă mobilă, care nu formează spori, gram-pozitivă. Au fost identificate șapte specii, este exclusiv un agent patogen uman. Morfologic imposibil de distins de difteroizi, prin urmare este adesea „vizibil” în timpul cercetărilor de laborator. Au fost identificate 16 serotipuri, dar 90% din toate cazurile de infecție aparentă clinic sunt asociate cu trei serotipuri: 46, 1/2b, 1/2a. Microorganismul este ușor de izolat dintr-un mediu normal steril (placentă, lichid amniotic, sânge), dar foarte greu de izolat din asociațiile microbiene.
Persoanele cu imunitate afectată, precum și femeile însărcinate și nou-născuții lor, sunt cele mai susceptibile la infecție. O preocupare deosebită este impactul infecției asupra incidenței prematurității și asupra stării fătului. În cazurile de listerioză la gravide se observă morbiditate și mortalitate perinatală ridicată..
Dacă este posibilă o infecție ascendentă, principala cale de infectare a fătului este răspândirea infecției de la mama bolnavă la placentă, de unde agentul patogen ajunge la făt, determinând septicemie care implică mai multe organe. Lichidul amniotic se infectează prin trecerea bacteriilor prin urina fetală. Aspirația lichidului amniotic infectat poate duce la deteriorarea căilor respiratorii fetale.
Listerioza există sub două forme: epidemică și sporadică. Forma epidemică este asociată cu consumul de produse alimentare contaminate.
În timpul unei epidemii, rata mortalității în rândul adulților și nou-născuților este de aproximativ 27-33%. Boala L. apare mai des și este mai periculoasă la persoanele cu imunitate afectată: gravide, nou-născuți, transplant de organe, boli maligne, insuficiență renală, lupus eritematos sistemic, terapie cu steroizi, infecție cu HIV. Cu cât infecția apare mai devreme în timpul sarcinii, cu atât este mai mare riscul de moarte fetală (sistem imunitar imatur). Vârsta medie de gestație la care a apărut infecția a fost de 26 de săptămâni pentru fetușii morți și de 34 de săptămâni pentru fetușii supraviețuitori. Formele sporadice (endemice) ale bolii apar mai des. Persoanele infectate cu L. prin consumul de alimente contaminate nu prezintă simptome ale bolii și devin purtători cronici ai agentului patogen în tractul lor gastrointestinal. Ulterior, femeile devin colonizate cu Listeria în vagin și col uterin. Multe femei însărcinate infectate nu au simptome ale bolii. Mai des (2/3 din cazuri), infecția este însoțită de manifestări clinice (prodrom): febră, frisoane, cefalee, mialgii, dureri de spate, afectarea căilor respiratorii superioare, mai rar sunt posibile diaree și dureri abdominale. Prodromul reprezintă stadiul bacteriemiei când este probabil să apară infecția sacului gestațional. La 3-7 zile după acest prodrom, se poate dezvolta amnionita, urmată de naștere prematură, avort septic, infecție fetală și naștere morta. Infecția maternă nu este severă; sepsisul general este rareori posibil. Mai des L. se observă în al treilea trimestru de sarcină. Din păcate, L. nu prezintă manifestări clinice specifice care să-l deosebească de alte infecții, așadar Femeile însărcinate cu simptome similare la sfârșitul celui de-al 2-lea - începutul celui de-al 3-lea trimestru trebuie examinate pentru prezența L.. Spre deosebire de mamă, L. la nou-născuți este mai gravă și poate fi fatală (3-50%).
Listerioza la nou-născuți este reprezentată de două tipuri diferite serologic și clinic. L. precoce (serotipurile Ia și IVb) apare sub formă de sepsis general cu afectare multiorganică: plămâni, ficat, sistem nervos central, duce la nașteri morti crescute și mortalitate neonatală, copiii cu greutate mică la naștere sunt mai des afectați. Infecția fătului are loc înainte de naștere (în timpul prodromului mamei). Boala se manifestă în primele ore și zile de viață. Caracterizat prin granuloame multiple, care se găsesc adesea în placentă și ficat. Ele pot fi cheia diagnosticului de sepsis neonatal în primele zile de viață.
Late L. apare la nou-născuții la termen în timpul sarcinii necomplicate. Consecințele frecvente ale bolii sunt hidrocefalie, retardul mintal, iar mortalitatea se apropie de 40%. Nou-născuții par sănătoși la naștere, dar boala se manifestă la câteva zile sau săptămâni după naștere: meningita este mai frecventă decât sepsisul. Se crede că infecția apare în timpul sau după naștere: în timpul trecerii fătului prin canalul de naștere sau în secția de nou-născuți a unei maternități.
Având în vedere rata mare de mortalitate în boala L. nou-născutului, toate gravidele cu febră trebuie evaluate pentru infecție: cultura secretiilor din canalul cervical si sange (se tine cont de asemanarea cu difteroizii la colorarea cu Gram: baghete pleiomorfe gram-pozitive cu capete rotunjite). Este posibilă efectuarea amniocentezei și testarea prezenței agentului patogen L.
Tratament efectuată cu penicilină sau ampicilină. Astăzi, combinația de ampicilină și aminoglicozide este considerată optimă. Tratament matern: ampicilină IV 1-2,0 la 4-6 ore și gentamicina 2 mg/kg IV la 8 ore timp de o săptămână. Tratament pentru nou-născut: ampicilină 200-300 mg/kg/zi în 4-6 injecții pe o săptămână. Tratamentul început în timpul sarcinii poate avea succes, iar sarcina se încheie cu nașterea unui nou-născut sănătos.
III. TUBERCULOZĂ.
Conform datelor SUA, în perioada 1985-1992. La femeile aflate la vârsta fertilă s-a înregistrat o creștere a incidenței T. cu 41%, iar la gravide, de 8 ori (95:100.000 nașteri). Diagnosticul se bazează pe prezența micobacteriilor în spută sub microscopie, dar un diagnostic definitiv necesită izolarea agentului patogen în cultură. Mai mult de jumătate dintre femeile însărcinate experimentează o stare de anergie cu testele cutanate negative. Sarcina nu crește frecvența infecției și nu provoacă exacerbarea bolii nici măcar la persoanele infectate cu HIV, deși T. este mai frecvent la acestea.
T. congenital este foarte rar: Mai puțin de 300 de cazuri publicate. Mai mult de jumătate dintre mame nu prezintă simptome ale bolii. Vârsta medie de debut este de 24 de zile de viață (1-84), iar cele mai frecvente semne sunt: hepatosplenomegalie (76%), detresă respiratorie (72%), febră (48%), PAW (38%), abdominală. mărire de volum (24%), depresie sau excitabilitate (21%), secreții din urechi (17%), erupții cutanate papulare (14%). Majoritatea nou-născuților au rezultate anormale la radiografia toracică, iar testele cutanate sunt de obicei negative. Rata mortalității este ridicată: 38%, în rândul nou-născuților care primesc tratament - 22%.
Tratament. Este necesar să se evite utilizarea streptomicinei (deteriorarea celei de-a 8-a perechi de nervi cranieni până la 15%) și a etionamidei (teratogen). Tratamentul trebuie să înceapă cu izoniazidă, rifampicină, etambutol. Acesta din urmă poate fi înlocuit cu acid para-aminosalicilic (PAS), care este mai bine tolerat. Alăptarea este permisă.
Următoarele sunt supuse tratamentului preventiv:
— infectat cu HIV cu un test tuberculină mai mare de 5 mm
— Persoane care au contact strâns cu un caz nou identificat de T. (papulă mai mare de 5 mm)
— Persoane cu infecție nou diagnosticată: test tuberculină mai mare de 10 mm în ultimii doi ani (pentru persoanele peste 35 de ani - mai mult de 15 mm)
— Persoane cu date radiografice care indică un proces fibrotic în plămâni (papulă mai mare de 5 mm)
— Persoanele care iau medicamente intravenoase, cu un test cutanat mai mare de 10 mm
— Persoane cu boli care cresc riscul de T., cu un test cutanat mai mare de 10 mm
Regimul obișnuit de terapie preventivă este izoniazida în doză de 300 mg/zi (dacă este necesar, de două ori pe zi la o doză de 15 mg/kg, dar nu mai mult de 900 mg pe zi) timp de 6-12 luni: tratament timp de un an se asigură persoanelor infectate cu HIV iar în cazul datelor patologice cu raze X, în alte cazuri, tratamentul se efectuează timp de 6 luni. În cazul sarcinii de peste 28 de săptămâni, tratamentul preventiv poate fi amânat până la naștere în timpul sarcinii în primul trimestru, până în al doilea trimestru; Indiferent dacă se efectuează sau nu un tratament preventiv, toate gravidele cu test tuberculinic pozitiv (papulă mai mare de 5 mm) sunt supuse unei radiografii toracice pentru a identifica o posibilă tuberculoză activă. Acest lucru este necesar pentru inițierea în timp util a tratamentului bolii și pentru prevenirea infecției nou-născutului de către o mamă cu T. activă a plămânilor.
PROTOZOOARE.
I. TOXOPLASMOZA
Semnele serologice ale unei infecții anterioare sunt observate la 20-40% dintre rezidenții din SUA și până la 84% la rezidenții din Paris. Rata de seroconversie în timpul sarcinii este de 1-2/1000. Aproximativ în 1/3 din cazuri (până la 60%) apare infecția fetală: o treime dintre nou-născuți au forme clinice, 2/3 au forme subclinice ale bolii. Rata infecțiilor fetale crește odată cu vârsta gestațională, în care s-a produs infecția, fiind minimă în perioada imediat după concepție: pentru primul trimestru - 14% (forme clinice aproximativ 11%), pentru al doilea trimestru - 29%, pentru al treilea trimestru - 59% (cifre mai mici pot se găsesc în literatură). in orice caz severitatea infecției la făt și mortalitatea perinatală sunt mai mari atunci când gravida se îmbolnăvește în primul trimestru. Riscul de T. congenital este în timpul sarcinii (după menstruație): 0-2 săptămâni - 0%, 3-10 săptămâni - 2%, 27-30 săptămâni - 22%, 31-34 săptămâni - 67%. Pentru orice femeie, un singur copil poate avea T. În ciuda a 20 de ani de cercetare, rolul T. ca posibilă cauză a avorturilor repetate rămâne neclar.
De regulă, o formă subclinică a bolii este observată atât la adulți, cât și la nou-născuți. Manifestările clinice evidente includ: PAW (gât), febră, durere în gât, erupții cutanate maculopapulare, hepatosplenomegalie (rar), limfocitoză. Tabloul clinic seamănă cu „gripa” sau mononucleoza infecțioasă. În unele cazuri, adulții pot prezenta modificări ale vederii: „ceață”, durere, fotofobie și erupții cutanate galben-albe pe fund (retinocoroidită locală necrozantă).
Majoritatea nou-născuților cu toxoplasmoză congenitală (55%) au doar semne serologice ale bolii. În manifestările clinice ale T., ocazional se întâlnește o triadă: calcificări ale țesutului cerebral (11%), corioretinită (22%), hidrocefalie (apare mai târziu, în 4% din cazuri). Pentru T. acută la gravide sunt posibile avorturile spontane, nașterea prematură și întârzierea creșterii fetale.
Diagnosticare:
1. Examinarea histologică a ganglionilor limfatici cu identificarea agentului patogen: laborios și insensibil,
2. Izolarea T. în cultură: cultura tisulară (fibroblaste de șoarece) este o metodă mai rapidă, iar inocularea intraperitoneală la șoareci (6 săptămâni urmată de determinarea anticorpilor specifici) este o metodă mai sensibilă,
3. Determinarea antigenului T. prin imunofluorescență (sensibilitatea este limitată),
4. Teste serologice (8 metode). Ig G apare la 1-2 luni după infectare și este detectată în titruri scăzute timp de câțiva ani. Absența Ig M și prezența Ig G în titruri peste 1:1000 indică prezența infecției în trecut. Diagnosticul de T. acut la o gravidă se bazează pe apariția Ig G specifice în sânge (seroconversie) sau pe o creștere a titrului acesteia după 3 sau mai multe săptămâni.
5. Determinarea ADN-ului patogen: PCR în lichidul amniotic este o metodă precisă și rapidă de diagnosticare a infecției fetale,
6. Teste nespecifice (la nou-născut): leucocitoză, ecografie, enzime hepatice. Ultrasunete: extinderea ventriculilor creierului, ecogenitatea crescută a țesutului cerebral, ficatul, îngroșarea și ecogenitatea crescută a placentei, hepatomegalie, ascită, revărsat pericardic și pleural.
Prevenirea. Constă în promovarea măsurilor de igienă personală care, din păcate, are un efect redus. Pentru gravida:
- nu mâncați carne crudă
- spală-te pe mâini după ce ai atins pisica
- nu ridicați fecalele de pisică
- ținerea pisicilor acasă (infecție de la șoareci)
- nu hrăni pisica cu carne crudă
- nu atingeți pisicile fără stăpân și nu le lăsați în casă
Fezabilitatea screening-ului de rutină pentru T. este discutabilă: Cu rate de incidență scăzute, este foarte scump.
Management și tratament. Dacă mama este bolnavă de T. în primul trimestru, este necesar să se diagnosticheze T. la făt și, dacă rezultatul este pozitiv, să se ofere întreruperea sarcinii. Pentru boala T. în stadiile ulterioare ale sarcinii este posibil tratament: sulfadiazină cu trimetoprim (toxică pentru măduva osoasă), acid folic. Prescrierea spiramicinei nu exclude infectarea fătului. La tratarea T. acută, 77% dintre copii se nasc fără semne de boală, iar tabloul clinic al bolii se manifestă la 5% dintre nou-născuți. În absența tratamentului, aceste cifre sunt de 39%, respectiv 14%. Și totuși, tratamentul mamei rămâne controversat: eficacitate incompletă, teratogenitate a unor medicamente (pirimetamina). Dar tratamentul nou-născuților cu T. confirmat este obligatoriu: pirimetamina, sulfadiazină, acid folic, eventual spiramicină. Tratamentul și observarea continuă timp de un an. Fără tratament, leziunile oculare și ale sistemului nervos central au fost observate la 40% dintre nou-născuții infectați cu tratament, doar la 2%.
| Toxoplasmoza | Rubeolă | Citomegalovirus | Virusul herpes simplex | |
| Metoda de transfer | Fecale de pisică, lapte și carne crudă de capră, | Picătură în aer | Secretele corpului | |
| 10-40% | 85-90% | 50-80% | 50% | |
| Tratamentul femeilor însărcinate | Pirimetamina, sulfadiazina | Nu | Ganciclovir | Aciclovir |
| Nevoia de screening | Nu | da | Nu | Nu |
| Imunitatea pe viață | Imunitatea pe viață | Purtător pe viață | Purtător pe viață | |
| Da (pentru infecția primară) | Da (pentru infecția primară) | da | Da (pentru infecția primară) | |
| Nu | Nu | Rareori | da | |
| Metoda de livrare | vaginale | vaginale | vaginale | Operație cezariană (erupție pe organele genitale) |
| Nu | Da (activ) | Nu | Nu |
| Sifilis | Hepatita B | HIV | streptococi din grupa B | |
| Metoda de transfer | Contact cu mucoasele și pielea | Secretele corpului | Secretele corpului | Sexual, oral-fecal |
| Seropozitivitatea în populația generală | — | 1% purtători cronici | 0,1%(?) | 35% colonizare a tractului genital |
| Tratamentul femeilor însărcinate | Penicilina benzatinica (retarpen, extensilina) | Imunoglobulina specifica | Zidovudină (azido-timidină) | Penicilină |
| Nevoia de screening | da | da | da | Nu |
| Starea după boală | Purtător pe viață (netratat) | Imunitate pe tot parcursul vieții (dacă purtător) | Proces infecțios pe tot parcursul vieții | Colonizarea de-a lungul vieții |
| Risc de transmitere transplacentară (antenatală) | da | Rareori | da | Rareori |
| Risc de infecție fetală în timpul nașterii | Nu | da | da | da |
| Metoda de livrare | vaginale | vaginale | vaginale | vaginale |
| Nevoia de imunizare a mamei și a nou-născutului | Nu | Da (activ și pasiv) | Nu | Nu |
Literatură.
- Obstetrică. Ed. K. Niswander, A. Evans (tradus în engleză - 1999).
- Davis P. A., Gotefors L. A. Infecții bacteriene ale fătului și nou-născutului (trad. engleză - M., 1987).
- Patologia clinică a sarcinii și a nou-născutului. Ed. M. N. Kochi, G. L. Gilbert, J. B. Brown (tradus în engleză - M., 1986).
- Epidemie necunoscută: herpes. Ed. L. N. Khakhalina.-Smolensk, 1997
- Sănătate reproductivă. Ed. L. G. Klein, G. S. Berger, D. A. Edelman (trad. engleză - 1988).
- Complicatii ale sarcinii: medicale, chirurgicale, ginecologice, psihosociale si perinate l. -ediția a IV-a.-Ed. de către Sh. H. Cherry, I. R. Merkatz.-1991.
- Sweet R. L., Gibbs R. S. Boli infecțioase ale tra ctului genital feminin.-Ediția a III-a.-1995.
(Vizitat de 116 ori, 1 vizite astăzi)
Infecțiile perinatale (IP) sunt infecții care se pot transmite de la mamă la făt cu posibila implementare ulterioară a infecției intrauterine în cursul nefavorabil și sfârșitul sarcinii, patologia fătului și a nou-născutului. IP este una dintre principalele cauze de morbiditate perinatală și mortalitate infantilă. Incidența morbidității și mortalității neonatale precoce din cauza infecției intrauterine variază de la 5,3 la 27,4%, iar ratele de naștere mortii ajung la 16,8%. Patologia infecțioasă congenitală este cauza directă a mortalității perinatale în 36-39% din cazuri.
Este necesar să se facă distincția între termenii „infecție intrauterină” și „infecție intrauterină”.
Termenul „infecție intrauterină” se referă la faptul infecției intrauterine și, în special, la pătrunderea agenților infecțioși la făt, dar la absența semnelor unei boli infecțioase a fătului. Infecția intrauterină este procesul de răspândire a agenților infecțioși în corpul fetal care provoacă tulburări morfofuncționale în diferite organe și sisteme inerente acestei boli infecțioase, survin ante- sau intranatal și manifestându-se perinatal sau după nașterea copilului.
Infecția mamei nu înseamnă infecția embrionului, a fătului și a bolii nou-născutului, deoarece frecvența infecției intrauterine este de aproximativ 10% din toate sarcinile, iar frecvența formelor pronunțate clinic de infecții intrauterine este de 0,5-1% în timp util. nașterile și 3,5-16% la nașterile premature.
Factori de risc pentru infecția intrauterină.
Femeile cu următorii factori de risc trebuie considerate cu risc crescut de infecție intrauterină: vârsta gravidei și a soțului ei (partenerului) este de 35 de ani sau mai mult, prezența factorilor și obiceiurilor dăunătoare profesionale;
predispoziție genetică la boli;
date de istorie somatică (prezența proceselor inflamatorii cronice ale sistemului urinar, respirator și alte boli extragenitale);
debutul precoce al activității sexuale, schimbarea frecventă a partenerilor sexuali;
istoric de boli inflamatorii ale uterului, anexe uterine, colpită;
contracepția intrauterină pe termen lung;
întrerupere artificială repetată a sarcinii;
întreruperea artificială a sarcinii cu o perioadă post-avort complicată;
întreruperea spontană a sarcinii în momente diferite, sarcină fără progresie;
malformații și moarte fetală antenatală;
curs complicat al perioadei postpartum la nașterile anterioare;
insuficiență placentară, suferință cronică și/sau sindrom de restricție a creșterii fetale (FGR)
ruperea prematură a lichidului amniotic, anomalii ale travaliului și separarea placentei, traumatisme severe ale țesuturilor moi ale canalului de naștere;
colpită și vaginoză bacteriană diagnosticate în timpul sarcinii;
corectarea chirurgicală a insuficienței istmico-cervicale în timpul sarcinii reale;
polihidramnios, oligohidramnios sau insuficiență placentară (IP).
De asemenea, acordă atenție bolilor nou-născutului (veziculoză, conjunctivită, pneumonie, sindrom de detresă respiratorie, boli inflamatorii ale creierului, malnutriție, pustomegalie și hepatosplenomegalie, sepsis etc.), prezența în familie a copiilor care au fost invalidi de atunci. copilărie, cu paralizie cerebrală ( paralizie cerebrală) sau alte boli ale sistemului nervos central de severitate variabilă, cu întârziere în dezvoltare.
Clasificare
În funcție de calea de intrare a agentului infecțios în corpul matern și apoi la embrion și/sau făt, se disting următoarele infecții perinatale: ascendent;
hematogen (cale transplacentară);
transcidual (cale transmurală);
Coborât (prin trompele uterine);
infecții transmise prin laptele matern;
infecții transmise prin sânge și componente ale acestuia;
infecții spitalicești;
mixt (două sau mai multe căi de infecție);
Infecții iatrogene.
În funcție de agent patogen: bacterian, viral, spirohetal, protozoar, mixt.
Patogeneza
Patogenia IUI este diversă și depinde de tipul de agent patogen, de interacțiunea acestuia cu embrionul (fătul), precum și de vârsta gestațională. Sunt posibile următoarele consecințe ale infecției fetale: patologie congenitală, moarte fetală antenatală, naștere prematură, infecție a fătului în timpul nașterii etc. Clinica
Manifestările clinice și severitatea infecțiilor perinatale depind de: tipul de agent patogen, virulența acestuia, specificitatea acțiunii, masivitatea contaminării și, de asemenea, dacă infecția este primară sau cronică;
homeostazia imună a corpului femeii;
etapele procesului infecțios la o femeie însărcinată;
perioada de sarcină în care a apărut infecția;
căile de intrare a agentului patogen în corpul unei femei însărcinate.
Caracteristicile clinice ale IP ar trebui să fie considerate semnele generale ale manifestării lor la mamă și făt.
Semne generale de IUI la mamă Alături de forma acută, există forme șterse, latente ale bolii sau boli asimptomatice.
Manifestările clinice nu depind întotdeauna de tipul de agent patogen, de virulența acestuia sau de nivelul de reactivitate imunologică a organismului.
Infecția fătului și a nou-născutului poate apărea din cauza infecției acute a mamei sau din cauza activării unei infecții cronice, persistente, în timpul sarcinii.
Activarea unei infecții persistente este posibilă în cazul oricărei perturbări a homeostaziei în corpul gravidei (hipotermie, stres, infecții respiratorii).
Infecțiile anterioare nu lasă imunitate de durată, astfel încât se observă reinfecții și recidive.
Bolile cu transmitere sexuală cresc semnificativ riscul de infecție cu HIV, hepatită B și C și cancer de col uterin.
Semne generale de IUI la făt.
Similitudinea manifestărilor depinde de durata infecției.
Algoritm pentru examinarea femeilor însărcinate cu risc crescut de infecție
După evaluarea factorilor de risc pentru infecția intrauterină, se formează grupuri de gravide cu risc infecțios ridicat pentru a fi examinate. Examinare clinică și de laborator
Examinarea clinică și de laborator a gravidelor cu risc infecțios ridicat constă în metode de cercetare standard, specifice și suplimentare.
Metode standard de cercetare
În cazul unei sarcini necomplicate de până la 28 de săptămâni, examinarea se efectuează o dată pe lună, din a 28-a până în a 36-a săptămână - o dată la 2 săptămâni, iar după a 36-a săptămână - săptămânal (în prezența unui virus și/sau infecție bacteriană, observație Femeile însărcinate sunt monitorizate mai des, conform indicațiilor). Greutatea corporală a gravidei, poziția sa, înălțimea fundului uterin, circumferința abdominală sunt determinate în mod regulat, se măsoară pulsul și tensiunea arterială. După 18-20 săptămâni de gestație se determină mobilitatea fetală.
Determinarea grupei sanguine, a factorului Rh și a titrului de anticorpi, teste serologice pentru antigenele R/L/, HB5 și NSL, analize de urină și sânge, analize biochimice, reologice de sânge la gravide, microscopia frotiurilor vaginale, colpocitograma, culturi din nas, faringele și canalul cervical către floră. Testarea sângelui unei femei însărcinate pentru titrul de anticorpi la fosfolipide, deoarece la acest grup de pacienți sindromul antifosfolipidic poate fi cauza directă a avorturilor spontane și a avortului spontan recurent.
Ecografia cu placentometrie și biometria embrionului și fătului trebuie efectuată la sfârșitul primului trimestru, în al doilea trimestru - la 16-22 săptămâni de sarcină, iar în trimestrul al treilea - la 33 și 36-38 de săptămâni de sarcină.
Examinarea cu ultrasunete Doppler a sistemului mama-placenta-fat din saptamana 19-20 de sarcina (daca circulatia feto-uteroplacentara este normala, se repeta la fiecare 3-4 saptamani, pentru tulburari hemodinamice - in timpul si imediat dupa tratament).
Din 32-33 de săptămâni de sarcină se prescrie CTG al fătului și se determină profilul biofizic al acestuia. CTG trebuie repetat în timp după un curs de tratament pentru suferința cronică a fătului și înainte de naștere.
Metode specifice de examinare de laborator. Folosesc metode bacterioscopice, bacteriologice, virologice, citologice, serologice și biologice moleculare (reacția în lanț a ligazei, reacția în lanț a polimerazei).
Metode suplimentare de cercetare. Metodele suplimentare de cercetare includ biopsia trofoblastului și corionului, cordocenteza, amniocinteza, consilierea genetică medicală etc.
Astfel de materiale biologice ar trebui investigate.
Examinarea conținutului canalului cervical, vaginului, uretrei:
bacterioscopic;
bacteriologice (calitative și cantitative) în prezența bacteriouriei;
virusologic.
Examinarea urinei:
bacterioscopic;
bacteriologice (calitative și cantitative)
virusologic;
biochimic (determinarea nitriților).
Examenul de urină are ca scop identificarea bacteriuriei asimptomatice sau confirmarea diagnosticului formelor manifeste de infecție a tractului urinar (uretrită, cistita, pielonefrită).
Bacteriurie asimptomatică - prezența agenților patogeni microbieni în 1 ml de urină medie într-o cantitate > 105 (100.000) colonii Unități de formare (CFU) în absența oricăror manifestări clinice. Leucocituria este, de asemenea, posibilă (nu este necesară).
Test de sânge pentru prezența anticorpilor specifici. Cel mai adesea, metodele serologice sunt utilizate pentru testarea sângelui. Astfel, testul imunosorbent legat de enzime (ELISA) determină prezența anticorpilor IgM și IgG specifici. Sensibilitate - 99%, specificitate - 95%. Acest lucru este necesar pentru detectarea în timp util a anticorpilor IgM sau pentru o creștere a concentrației totale de IgM și IgG.
Pentru a crește fiabilitatea rezultatelor, reacția într-o probă de material trebuie efectuată cu două tipuri de antiseruri (IgIg clasa M și G).
Ținând cont de un eventual supradiagnostic, infecția trebuie verificată prin cel puțin două metode (ELISA și PCR). Cele mai precise informații despre prezența infecției intrauterine și starea „pacientului” intrauterin în timpul sarcinii de la 16-18 la 32 de săptămâni pot fi obținute în spitalele obstetricale moderne folosind studii bacteriene și/sau virusologice ale lichidului amniotic (obținute prin amniocenteză transabdominală). ) și sânge fetal (prin cordocenteză). Nivelul a-FP este determinat și în lichidul amniotic (abaterile de la normă, începând din săptămâna 17-18 de gestație, indică un risc ridicat de patologie perinatală).
Indicații pentru examinare pentru identificarea PI.
Indicații pentru examinare pentru identificarea agenților patogeni ai gonoreei, chlamydia, trichomoniaza, candidoza, vaginoza bacteriană este prezența semnelor clinice de vaginită.
Indicațiile pentru examinarea pentru depistarea virusului herpesului sunt prezența erupțiilor cutanate caracteristice.
Indicații pentru screening-ul pentru rubeolă: contactul cu un pacient cu rubeolă în absența imunitații la rubeolă la o femeie însărcinată;
suspiciunea sau prezența simptomelor bolii (erupție cutanată).
Indicațiile pentru examinarea pentru detectarea streptococilor B includ următoarele situații:
perioadă anhidră mai mare de 18 ore;
febră în timpul nașterii (mai mult de 38o);
infecția copiilor mai mari cu streptococi de grup B;
bacteriurie cu streptococ de grup B.
Tactica medicului în timpul sarcinii
Următoarele abordări recomandate pentru examinarea femeilor însărcinate, tratamentul și consecințele anumitor infecții perinatale Infecțiile perinatale sunt infecții cauzate de bacterii sau viruși care pot fi transmise de la mamă la copil în timpul sarcinii sau al nașterii. Infecțiile perinatale includ boli bacteriene sau virale și, în unele cazuri, pot provoca complicații în timpul nașterii. Unele infecții perinatale se transmit pe cale sexuală.
Transmiterea multor infecții perinatale are loc în timpul nașterii, mai ales când se folosesc tehnici invazive precum epiziotomia sau ruptura artificială a membranei. În alte cazuri, transmiterea poate avea loc în timpul sarcinii dacă agentul infecțios traversează bariera placentară poate apărea și în timpul alăptării dacă agentul patogen se află în laptele matern.
Frecvența infecțiilor perinatale depinde de tipul de agent patogen. De exemplu, transmiterea perinatală a CMV are loc în 2-24 de cazuri din 1000 de născuți vii. Transmiterea herpesului genital în timpul sarcinii este estimată la una până la două la fiecare 2.000 de sarcini; transmiterea grupului beta-streptococ provoacă infecție neonatală la unul până la cinci din 1000 de născuți vii, iar rubeola - 0,02 la fiecare 1000 de copii. HIV se transmite de la mamă la copil în 25-40 la sută din cazuri.
Tipuri de infecții perinatale
Următoarele sunt câteva dintre cele mai frecvente infecții care se pot transmite perinatal.
Chlamydia
Chlamydia este cea mai frecventă boală bacteriană cu transmitere sexuală. Majoritatea femeilor cu infecție cu chlamydia nu au simptome evidente. Infecția afectează tractul reproducător și provoacă boli inflamatorii pelvine, infertilitate și sarcină ectopică. Această infecție poate provoca ruperea prematură a membranei și nașterea prematură. Chlamydia poate fi transmisă unui copil în timpul nașterii și poate duce la blenoree neonatală (o infecție oculară) în prima lună de viață și pneumonie în decurs de una până la trei luni. Simptomele pneumoniei cu chlamydia includ tusea și respirația rapidă. Dispneea și febra sunt rare.
Citomegalie
 Citomegalovirusul (CMV) este un virus comun din familia herpesului. Se găsește în salivă, urină și alte fluide corporale și poate fi transmisă prin contact sexual sau alte forme de contact fizic. La adulți, CMV poate provoca simptome ușoare ale glandelor limfatice umflate, febră și oboseală. Mulți oameni care poartă acest virus nu prezintă niciun simptom. Un copil se poate infecta cu CMV dacă mama se îmbolnăvește sau dezvoltă o recidivă a infecției în timpul sarcinii. CMV interferează cu dezvoltarea normală a fătului și poate duce la retard mental, orbire, surditate sau epilepsie.
Citomegalovirusul (CMV) este un virus comun din familia herpesului. Se găsește în salivă, urină și alte fluide corporale și poate fi transmisă prin contact sexual sau alte forme de contact fizic. La adulți, CMV poate provoca simptome ușoare ale glandelor limfatice umflate, febră și oboseală. Mulți oameni care poartă acest virus nu prezintă niciun simptom. Un copil se poate infecta cu CMV dacă mama se îmbolnăvește sau dezvoltă o recidivă a infecției în timpul sarcinii. CMV interferează cu dezvoltarea normală a fătului și poate duce la retard mental, orbire, surditate sau epilepsie.
Herpes genital
Herpesul genital, de obicei cauzat de virusul herpes simplex tip 2 (HSV-2), este o boală cu transmitere sexuală care provoacă răni dureroase la nivelul organelor genitale. Femeile care au primele focare de herpes genital în timpul sarcinii au un risc mare de avort spontan sau greutate mică la naștere a copilului. Infecția se poate transmite de la mamă la copil în timpul nașterii dacă mama are boală activă. Cel mai grav risc pentru un copil este posibilitatea de a dezvolta encefalita, cu inflamatie a creierului, simptome de iritabilitate si pofta de mancare.
Hepatita B
Hepatita B este un virus infecțios care provoacă leziuni hepatice și este o cauză principală a bolilor hepatice cronice și a cirozei. Copilul prezintă un risc crescut de a dezvolta infecție cu hepatită prin contactul cu sângele unei mame infectate în timpul nașterii.
Virusul imunodeficienței umane (HIV)
Abonați-vă la nostru Canalul canalului YouTube !
HIV este un virus grav, contagios, care provoacă sindromul imunodeficienței dobândite (SIDA). Aproximativ 25-40% dintre femeile însărcinate cu HIV transmit infecția nou-născuților. Simptomele infecției cu HIV la copiii mici includ semne de întârziere a dezvoltării, afte cronice și diaree.
Papilomavirus uman
 Virusul papiloma uman (HPV), o boală cu transmitere sexuală care provoacă veruci genitale și poate crește riscul de a dezvolta anumite tipuri de cancer. HPV poate fi transmis de la mamă la copil în timpul nașterii și poate provoca îngustarea traheei.
Virusul papiloma uman (HPV), o boală cu transmitere sexuală care provoacă veruci genitale și poate crește riscul de a dezvolta anumite tipuri de cancer. HPV poate fi transmis de la mamă la copil în timpul nașterii și poate provoca îngustarea traheei.
Rubeola (rujeola germană)
Rubeola este un virus care provoacă erupții cutanate, febră și simptome ale unei infecții ale tractului respirator superior. Majoritatea oamenilor sunt expuși la rubeolă în copilărie și dezvoltă anticorpi împotriva virusului. Rubeola la începutul sarcinii poate traversa placenta și poate provoca malformații congenitale grave, inclusiv anomalii cardiace, retard mintal, orbire și surditate.
Grupul Beta Streptococcus
Streptococul beta de grup (GBS) este cea mai frecventă cauză bacteriană de deces la nou-născuți din cauza infecțiilor, deși ratele au scăzut oarecum odată cu apariția antibioticelor. La femei, GBS poate provoca vaginită și infecții ale tractului urinar. Ambele infecții pot provoca travaliu prematur, iar bacteriile pot fi transmise copilului în uter sau în timpul nașterii. GBS provoacă pneumonie, meningită și alte infecții grave la sugari.
Sifilis
Sifilisul este o boală cu transmitere sexuală care poate fi transmisă de la mamă la copil prin placentă înainte de naștere. Până la 50% dintre copiii născuți de mame cu sifilis sunt prematuri sau născuți morți sau mor la scurt timp după naștere. Sugarii infectați pot avea malformații congenitale grave. Acei copii care supraviețuiesc copilăriei pot avea simptome de sifilis până la doi ani mai târziu.
Refuzarea răspunderii: Informațiile prezentate în acest articol despre infecțiile perinatale au scopul de a informa doar cititorul. Nu este destinat să înlocuiască sfatul unui profesionist din domeniul sănătății.